摘要: 为了证明“燃素说 的错误.18世纪法国化学家Lavaisier在密闭的曲颈瓶中进行了锡.硫.磷等物质的燃烧实验.每次实验他都要称量:1)燃烧前密闭的曲颈瓶.2)燃烧后密闭的曲颈瓶.3)燃烧后被打开的曲颈瓶.其中质量最大的是 ,根据实验结果.Lavaisier断言可燃物之所以能实现燃烧并非由于物质内部含有“燃素 .而是由于 .Lavaisier通过上述实验.同时发现了 定律.类似的实验英国科学家 Boyle在100年前就做过.但Boyle并未发现这一定律.原因是Boyle没有对 进行称量.
网址:http://m.1010jiajiao.com/timu3_id_435058[举报]
普利斯特里(Joseph Priestley)在拉瓦锡之前发现了氧气,但由于受“燃素说”的影响,他把氧气当作了“燃素”。拉瓦锡正是在普利斯特里研究的基础上,破除了“燃素说”的束缚,确认氧气是由一种元素形成的纯净物。普利斯特里在一次加热浓硫酸的实验中,由于不慎,造成了倒吸,将水槽中的水银(Hg)倒吸进加热后的浓硫酸中,并且烧坏了手。偶然中他发现热的浓H2SO4与水银发生了反应并生成了一种气体。这种气体就是由他发现的SO2。根据以上叙述判断下列说法不正确的是( )
A.浓H2SO4具有强腐蚀性,操作应格外小心
B.为防止倒吸,实验结束时应先从水槽中取出导气管,后撤酒精灯
C.实验中应仔细观察,不放过任何异常现象
D.普利斯特里是一位失败的科学家,不值得尊敬
查看习题详情和答案>>
普利斯特里(Joseph Priestley)在拉瓦锡之前发现了氧气,但由于受“燃素说”的影响,他把氧气当作了“燃素”。拉瓦锡正是在普利斯特里研究的基础上,破除了“燃素说”的束缚,确认氧气是由一种元素形成的纯净物。普利斯特里在一次加热浓硫酸的实验中,由于不慎,造成了倒吸,将水槽中的水银(Hg)倒吸进加热后的浓硫酸中,并且烧坏了手。偶然中他发现热的浓H2SO4与水银发生了反应并生成了一种气体。这种气体就是由他发现的SO2。根据以上叙述判断下列说法不正确的是( )
A.浓H2SO4具有强腐蚀性,操作应格外小心
B.为防止倒吸,实验结束时应先从水槽中取出导气管,后撤酒精灯
C.实验中应仔细观察,不放过任何异常现象
D.普利斯特里是一位失败的科学家,不值得尊敬
查看习题详情和答案>>(2011?上海模拟)为了证明化学反应有一定的限度,进行了如下探究活动:
(Ⅰ)取5mL0.1mol?L-1的KI溶液,滴加0.1mol?L-1的FeCl3溶液5~6滴
(Ⅱ)继续加入2mLCCl4振荡
(Ⅲ)取萃取后的上层清液,滴加KSCN溶液
(1)探究活动(Ⅰ)和(Ⅱ)的实验现象分别为
(2)在探究活动(Ⅲ)中,活动设计者的意图是通过生成血红色的Fe(SCN)3,验证有Fe3+残留,从而证明化学反应有一定的限度,但在实验中,却未见溶液呈血红色,对此同学们提出了下列两种猜想.
猜想一:Fe3+已全部转化为Fe2+
猜想二:生成Fe(SCN)3浓度极小,其颜色肉眼无法观察
为了验证猜想,在查阅资料后,获得下列信息:
信息一:乙醚微溶于水,Fe(SCN)3在乙醚中的溶解度比在水中大
信息二:Fe3+可与[Fe(CN)6]4-反应生成蓝色沉淀,用K4[Fe(CN)6]溶液检验Fe3+的灵敏度比用KSCN更高
结合新信息,请你设计以下实验验证猜想
①请将相关的实验操作、现象和结论填入下表
②写出操作“步骤一”中发生反应的离子方程式
查看习题详情和答案>>
(Ⅰ)取5mL0.1mol?L-1的KI溶液,滴加0.1mol?L-1的FeCl3溶液5~6滴
(Ⅱ)继续加入2mLCCl4振荡
(Ⅲ)取萃取后的上层清液,滴加KSCN溶液
(1)探究活动(Ⅰ)和(Ⅱ)的实验现象分别为
溶液呈棕黄色
溶液呈棕黄色
、溶液分层,下层CCl4层呈紫色
溶液分层,下层CCl4层呈紫色
.(2)在探究活动(Ⅲ)中,活动设计者的意图是通过生成血红色的Fe(SCN)3,验证有Fe3+残留,从而证明化学反应有一定的限度,但在实验中,却未见溶液呈血红色,对此同学们提出了下列两种猜想.
猜想一:Fe3+已全部转化为Fe2+
猜想二:生成Fe(SCN)3浓度极小,其颜色肉眼无法观察
为了验证猜想,在查阅资料后,获得下列信息:
信息一:乙醚微溶于水,Fe(SCN)3在乙醚中的溶解度比在水中大
信息二:Fe3+可与[Fe(CN)6]4-反应生成蓝色沉淀,用K4[Fe(CN)6]溶液检验Fe3+的灵敏度比用KSCN更高
结合新信息,请你设计以下实验验证猜想
①请将相关的实验操作、现象和结论填入下表
| 实验操作 | 现象 | 结论 |
| 步骤一: 取萃取后的上层清液滴加2-3滴 K4[Fe(CN)6]溶液 取萃取后的上层清液滴加2-3滴 K4[Fe(CN)6]溶液 |
产生蓝色沉淀 | 猜想一不成立 猜想一不成立 |
| 步骤二: 往探究活动III溶液中加入乙醚,充分振荡 往探究活动III溶液中加入乙醚,充分振荡 |
乙醚层呈血红色 乙醚层呈血红色 |
“猜想二”成立 |
4Fe3++3[Fe(CN)6]4-═Fe4[Fe(CN)6]3↓
4Fe3++3[Fe(CN)6]4-═Fe4[Fe(CN)6]3↓
.某化学小组为了证明SO2和Cl2的漂白性,设计了如图所示的实验装置:

(1)他们制备Cl2依据的原理是:MnO2+4HCl(浓)
MnCl2+2H2O+Cl2↑,应选用上图A、E装置中的
(2)反应开始后,发现B、D两个试管中的品红溶液都褪色,停止通气后,给B、D两个试管中的液体加热,B试管中的现象是
(3)NaOH溶液分别与两种气体反应的离子方程式是
(4)该小组同学将两种气体混合后通入品红溶液,一段时间后,品红溶液几乎不褪色.查阅资料得知:两种气体按体积比1:1混合,再与水反应可生成两种常见的酸,因而失去漂白作用,该反应的化学方程式是
查看习题详情和答案>>

(1)他们制备Cl2依据的原理是:MnO2+4HCl(浓)
| ||
E
E
(填序号)制Cl2,反应中浓盐酸所表现出的性质是酸性
酸性
、还原性
还原性
.(2)反应开始后,发现B、D两个试管中的品红溶液都褪色,停止通气后,给B、D两个试管中的液体加热,B试管中的现象是
溶液由无色变为红色
溶液由无色变为红色
.(3)NaOH溶液分别与两种气体反应的离子方程式是
Cl2+2OH-=Cl-+ClO-+H2O
Cl2+2OH-=Cl-+ClO-+H2O
、SO2+2OH-=SO32-+H2O
SO2+2OH-=SO32-+H2O
.(4)该小组同学将两种气体混合后通入品红溶液,一段时间后,品红溶液几乎不褪色.查阅资料得知:两种气体按体积比1:1混合,再与水反应可生成两种常见的酸,因而失去漂白作用,该反应的化学方程式是
Cl2+SO2+2H2O=H2SO4+2HCl
Cl2+SO2+2H2O=H2SO4+2HCl
. (1)向蓝色石蕊试纸上滴加几滴饱和氯水,发现试纸先变红后变白.要确证使石蕊褪色的物质是次氯酸,还必须要做的实验是
(1)向蓝色石蕊试纸上滴加几滴饱和氯水,发现试纸先变红后变白.要确证使石蕊褪色的物质是次氯酸,还必须要做的实验是a.干燥的氯气能否使试纸变白b.水能否使试纸变白c盐酸能否使试纸变白
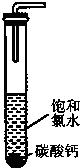
(2)饱和氯水与石灰石的反应是制取较浓HClO溶液的方法之一.如图所示在试管中加入过量的块状碳酸钙.再加入约20ml饱和氯水充分反应,有少量气泡产生,溶液浅黄绿色褪去:过滤,将滤液滴在蓝色石蕊试纸上发现其漂白性比饱和氯水的更强:已知饱和氨水中存在Cl2+H2O?H++Cl-+HClO.反应后所得的溶液漂白性增强的原因是
(3)碳酸钙与氯水反应生成的含钙的化合物除氯化钙外,有人提出如下猜想
a.含次氯酸钙b.含碳酸氢钙c.含次氯酸钙和碳酸氢钙.
有人认为不可能含有次氯酸钙.他的理由可能是
①第一份与澄清石灰水混合,立即产生大量白色沉淀:此实验
②第二份与稀盐酸混合,立即产生大量无色气体:
③将第三份加热,看到溶液变浑浊且有大量无色气体产生.反应的化学方程式为
④除上述实验外,你能设计的确证碳酸氢钙存在的实验方案是