摘要: 络(配)离子[ MA4B2]a的空间构型为八面体.它的异构体有 种,络(配)离子[ MA3B2]a的空间构型为六面体.它的异构体有 种.
网址:http://m.1010jiajiao.com/timu3_id_435056[举报]
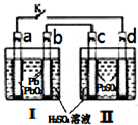 飞机、汽车、拖拉机、坦克,都是用蓄电池作为照明光源是典型的可充型电池,总反应式为:
飞机、汽车、拖拉机、坦克,都是用蓄电池作为照明光源是典型的可充型电池,总反应式为:Pb+PbO2+4H++2SO42-
| ||
| 充电 |
(1)当K闭合时,a电极的电极反应式是
PbO2+2e-+4H++SO42-=PbSO4+2H2O
PbO2+2e-+4H++SO42-=PbSO4+2H2O
;放电过程中SO42-向b
b
极迁移.当K闭合一段时间后,再打开K,Ⅱ可单独作为原电池使用,此时c电极的电极反应式为Pb-2e-+SO42-=PbSO4
Pb-2e-+SO42-=PbSO4
.(2)铅的许多化合物,色彩缤纷,常用作颜料,如铬酸铅是黄色颜料,碘化铅是金色颜料(与硫化锡齐名),室温下碘化铅在水中存在如下平衡:PbI2(S)?Pb2+(aq)+2I-(aq).
①该反应的溶度积常数表达式为Ksp=
c(Pb2+)?c2(I-)
c(Pb2+)?c2(I-)
.②已知在室温时,PbI2的溶度积Ksp=8.0×10-9,则100mL 2×10-3mol/L的碘化钠溶液中,加入100mL2×10-2mol/L的硝酸铅溶液,通过计算说明是否能产生PbI2沉淀
Qc=10-2?(10-3)2=10-8>Ksp,能产生PbI2沉淀
Qc=10-2?(10-3)2=10-8>Ksp,能产生PbI2沉淀
.③探究浓度对碘化铅沉淀溶解平衡的影响
该化学小组根据所提供试剂设计两个实验,来说明浓度对沉淀溶解平衡的影响.
提供试剂:NaI饱和溶液、NaCl饱和溶液、FeCl3饱和溶液、PbI2饱和溶液、PbI2悬浊液;
信息提示:Pb2+和Cl-能形成较稳定的PbCl42-络离子.
请填写下表的空白处:
| 实验内容 | 实验方法 | 实验现象及原因分析 |
| ①碘离子浓度增大对平衡的影响 | 取PbI2饱和溶液少量于一支试管中,再加入少量NaI饱和溶液, 取PbI2饱和溶液少量于一支试管中,再加入少量NaI饱和溶液, |
溶液中出现黄色浑浊. 原因是溶液中c(I-)增大,使Qc大于了pbI2的Ksp 溶液中出现黄色浑浊. 原因是溶液中c(I-)增大,使Qc大于了pbI2的Ksp |
| ②铅离子浓度减小对平衡的影响 | 取PbI2悬浊液少量于一支试管中,再加入少量NaCl饱和溶液 取PbI2悬浊液少量于一支试管中,再加入少量NaCl饱和溶液 |
黄色浑浊消失 原因是形成PbCl42-,导致溶液中c(Pb2+)减小,使Qc小于了pbI2的Ksp 黄色浑浊消失 原因是形成PbCl42-,导致溶液中c(Pb2+)减小,使Qc小于了pbI2的Ksp |
| ③ 铅离子和碘离子浓度都减小对平衡的影响 铅离子和碘离子浓度都减小对平衡的影响 |
在PbI2悬浊液中加入少量FeCl3饱和溶液 | PbI2 +2Fe3++4Cl-=PbCl42-+2Fe2++I2 PbI2 +2Fe3++4Cl-=PbCl42-+2Fe2++I2 |
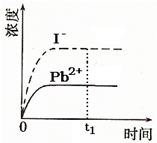 ④已知室温下PbI2的Ksp=8.0×10-9,将适量PbI2固体溶于 100mL水中至刚好饱和,该过程中Pb2+和I-浓度随时间变化关系如图(饱和PbI2溶液中c(I-)=0.0025mol?L-1).若t1时刻在上述体系中加入100mL.、0.020mol?L-1 NaI 溶液,画出t1时刻后Pb2+和I-浓度随时间变化关系图.
④已知室温下PbI2的Ksp=8.0×10-9,将适量PbI2固体溶于 100mL水中至刚好饱和,该过程中Pb2+和I-浓度随时间变化关系如图(饱和PbI2溶液中c(I-)=0.0025mol?L-1).若t1时刻在上述体系中加入100mL.、0.020mol?L-1 NaI 溶液,画出t1时刻后Pb2+和I-浓度随时间变化关系图.⑤至于碳酸铅,早在古代就被用作白色颜料.考古工作者发掘到的古代壁画或泥俑,其中人脸常是黑色的.经过化学分析和考证,证明这黑色的颜料是铅的化合物--硫化铅(已知PbCO3的
Ksp=1.46×10-13,PbS的Ksp=9.04×10-29)试分析其中奥妙
PbCO3的Ksp=1.46×10-13 >PbS的Ksp=9.04×10-29 故PbCO3与S2-接触时,转化为更难溶的黑色的PbS了
PbCO3的Ksp=1.46×10-13 >PbS的Ksp=9.04×10-29 故PbCO3与S2-接触时,转化为更难溶的黑色的PbS了
.(2013?肇庆一模)铜是一种重要的金属元素,位于元素周期表第ⅠB族,+1价的铜与氯离子结合的生成的CuCl是一种难溶物质,但它可与过量的Cl-形成可溶于水的络离子[CuCl2]-.含铜最丰富的天然资源是黄铜矿(CuFeS2).
(1)目前有一种湿法冶炼技术,以黄铜矿为主要原料来生产铜、铁红颜料和可用于橡胶硫化的硫单质,原料的综合利用率较高.其主要流程如下:
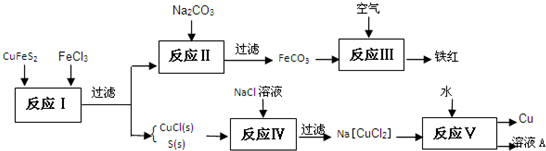
①请完成反应Ⅰ中FeCl3与CuFeS2反应的化学方程式:
CuFeS2+
②写出反应Ⅳ中发生反应的离子方程式:
③反应Ⅲ是FeCO3在空气中煅烧,其化学方程式是
④已知Cu+ 在反应V中发生自身氧化还原反应,歧化为Cu2+和Cu.则反应Ⅴ所得溶液A中含有的溶质有
(2)传统工艺从黄铜矿冶炼粗铜的技术,是将精选后的富铜矿砂与空气在高温下煅烧,使其转变为铜.与上面湿法冶炼技术方法比较,新方法的优点是
查看习题详情和答案>>
(1)目前有一种湿法冶炼技术,以黄铜矿为主要原料来生产铜、铁红颜料和可用于橡胶硫化的硫单质,原料的综合利用率较高.其主要流程如下:

①请完成反应Ⅰ中FeCl3与CuFeS2反应的化学方程式:
CuFeS2+
3
3
FeCl3=CuCl
CuCl
+4FeCl2
FeCl2
+2S.②写出反应Ⅳ中发生反应的离子方程式:
Cl-+CuCl=[CuCl2]-
Cl-+CuCl=[CuCl2]-
.③反应Ⅲ是FeCO3在空气中煅烧,其化学方程式是
4FeCO3+O2
+2Fe2O3
| ||
4FeCO3+O2
+2Fe2O3
.
| ||
④已知Cu+ 在反应V中发生自身氧化还原反应,歧化为Cu2+和Cu.则反应Ⅴ所得溶液A中含有的溶质有
CuCl2、NaCl
CuCl2、NaCl
.(2)传统工艺从黄铜矿冶炼粗铜的技术,是将精选后的富铜矿砂与空气在高温下煅烧,使其转变为铜.与上面湿法冶炼技术方法比较,新方法的优点是
不会产生SO2污染大气
不会产生SO2污染大气
、不用煅烧黄铜矿从而节约热能
不用煅烧黄铜矿从而节约热能
. 某研究性学习小组为证明2Fe3++2I-?2Fe2++I2为可逆反应(即反应存在一定的限度),设计如下几种方案.已知FeF63-是一种无色的稳定的络离子.
某研究性学习小组为证明2Fe3++2I-?2Fe2++I2为可逆反应(即反应存在一定的限度),设计如下几种方案.已知FeF63-是一种无色的稳定的络离子.按要求回答下列问题.
方案甲:
取5mL 0.1mol/L KI溶液,滴加2ml 0.1mol/L 的FeCl3溶液,再继续加入2mL CCl4,充分振荡.静置、分层,再取上层清液,滴加KSCN溶液.
(1)甲方案中能证明该反应为可逆反应的现象是
(2)有同学认为该方案设计不够严密,即使该反应为不可逆反应也可能出现上述现象,其原因是
方案乙:
取5mL 0.1mol/L KI溶液,滴加2ml 0.1mol/L 的FeCl3溶液,溶液呈棕黄色,再往溶液中滴加NH4F溶液,若看到
方案丙:
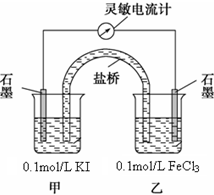
设计如图原电池装置,接通灵敏电流计,指针向右偏转(注:灵敏电流计指针总是偏向电源正极),随着时间进行电流计读数逐渐变小,最后读数变为零.
当指针读数变零后,在乙烧杯中加入1mol/L FeCl2溶液,若观察到灵敏电流计的指针向
(2013?绍兴一模)工业催化剂K3[Fe(C2O4)3]?3H2O是翠绿色晶体,在421~553℃时,分解为Fe2O3、K2CO3、CO、CO2、H2O.实验室由草酸亚铁晶体(FeC2O4?2H2O)、草酸钾(K2C2O4)、草酸(H2C2O4)和双氧水(H2O2)混合制备.
请回答下列问题:
(1)写出H2O2的电子式
 ;[Fe(C2O4)3]3-的名称是
;[Fe(C2O4)3]3-的名称是
(2)配平以下总反应方程式:
(3)制备过程中要防止草酸被H2O2氧化,请写出草酸被H2O2氧化的化学反应方程式
(4)配合物的稳定性可以用稳定常数K来衡量,如Cu2++4NH3?[Cu(NH3)4]2+,其稳定常数表达式为k=
.已知K[Fe(C2O4)3]3-=1020,K[Fe(SCN)3]=2×103,能否用KSCN溶液检验K3[Fe(C2O4)3]?3H2O中的铁元素?
(5)铁元素可以形成多种配合物,其中一种配合物钾盐A是有争议的食品添加剂.经组成分析A中仅含K、Fe、C、N四种元素.取36.8gA加热至400℃,分解成KCN、Fe3C、C、N2,生成的氮气折合成标准状况下的体积为2.24L,Fe3C质量是C质量的3倍.Fe3C的物质的量是氮气物质的量的
.则A的化学式为
查看习题详情和答案>>
请回答下列问题:
(1)写出H2O2的电子式


[Fe(C2O4)3]3-为络离子,名称为三草酸合铁(Ⅲ)离子(或三草酸合铁离子,或三草酸合铁酸根)
[Fe(C2O4)3]3-为络离子,名称为三草酸合铁(Ⅲ)离子(或三草酸合铁离子,或三草酸合铁酸根)
.(2)配平以下总反应方程式:
2
2
FeC2O4?2H2O+1
1
H2O2+3
3
K2C2O4+1
1
H2C2O4=3
3
K3[Fe(C2O4)3]?3H2O(3)制备过程中要防止草酸被H2O2氧化,请写出草酸被H2O2氧化的化学反应方程式
H2C2O4+H2O2=2CO2↑+2H2O
H2C2O4+H2O2=2CO2↑+2H2O
.(4)配合物的稳定性可以用稳定常数K来衡量,如Cu2++4NH3?[Cu(NH3)4]2+,其稳定常数表达式为k=
c[Cu(NH3
| ||
| c(Cu2+)?c4(NH3) |
否
否
(填“是”“否”)若选“否”,请设计检验铁元素的方案取适量晶体加热,取固体残留物溶解在H2SO4中,取上层清液于试管中,滴加KSCN溶液.若溶液呈血红色则有铁元素,反之则无
取适量晶体加热,取固体残留物溶解在H2SO4中,取上层清液于试管中,滴加KSCN溶液.若溶液呈血红色则有铁元素,反之则无
.(5)铁元素可以形成多种配合物,其中一种配合物钾盐A是有争议的食品添加剂.经组成分析A中仅含K、Fe、C、N四种元素.取36.8gA加热至400℃,分解成KCN、Fe3C、C、N2,生成的氮气折合成标准状况下的体积为2.24L,Fe3C质量是C质量的3倍.Fe3C的物质的量是氮气物质的量的
| 1 |
| 3 |
K4Fe(CN)6
K4Fe(CN)6
.(2009?汕头二模)间接碘量法测定胆矾中铜含量的原理和方法如下:
已知:在弱酸性条件下,胆矾中Cu2+与 I-作用定量析出 I2;I2溶于过量的KI溶液中:I2+I-═I3-;且在溶液中:Fe3++6F-=[FeF6]3-( 六氟合铁(III)络离子 )
又知:微粒的氧化性强弱顺序为:Fe3+>Cu2+>I2>FeF63-
析出I2可用cmol/LNa2S2O3标准溶液滴定:2S2O32-+I3-═S4O62-+3I-.
现准确称取ag胆矾试样,置于250mL碘量瓶(带磨口塞的锥形瓶)中,加50mL蒸馏水、5mL3mol/LH2SO4溶液,加少量NaF,再加入足量的10%KI溶液,摇匀.盖上碘量瓶瓶盖,置于暗处5min,充分反应后,加入1~2mL0.5%的淀粉溶液,用Na2S2O3标准溶液滴定到蓝色褪去时,共用去VmL标准液.
(1)实验中,在加KI前需加入少量NaF,推测其作用可能是
(2)实验中加入稀硫酸,你认为硫酸的作用是
(3)本实验中用碘量瓶而不用普通锥形瓶是因为
(4)硫酸铜溶液与碘化钾溶液反应生成白色沉淀(碘化亚铜)并析出碘,该反应的离子方程式为:
(5)根据本次实验结果,该胆矾试样中铜元素的质量分数ω(Cu)=
×100
×100%.
查看习题详情和答案>>
已知:在弱酸性条件下,胆矾中Cu2+与 I-作用定量析出 I2;I2溶于过量的KI溶液中:I2+I-═I3-;且在溶液中:Fe3++6F-=[FeF6]3-( 六氟合铁(III)络离子 )
又知:微粒的氧化性强弱顺序为:Fe3+>Cu2+>I2>FeF63-
析出I2可用cmol/LNa2S2O3标准溶液滴定:2S2O32-+I3-═S4O62-+3I-.
现准确称取ag胆矾试样,置于250mL碘量瓶(带磨口塞的锥形瓶)中,加50mL蒸馏水、5mL3mol/LH2SO4溶液,加少量NaF,再加入足量的10%KI溶液,摇匀.盖上碘量瓶瓶盖,置于暗处5min,充分反应后,加入1~2mL0.5%的淀粉溶液,用Na2S2O3标准溶液滴定到蓝色褪去时,共用去VmL标准液.
(1)实验中,在加KI前需加入少量NaF,推测其作用可能是
掩蔽Fe3+,防止造成偏大的误差
掩蔽Fe3+,防止造成偏大的误差
; (2)实验中加入稀硫酸,你认为硫酸的作用是
提供酸性条件,抑制Cu2+的水解
提供酸性条件,抑制Cu2+的水解
; (3)本实验中用碘量瓶而不用普通锥形瓶是因为
防止空气中的氧气与碘化钾反应
防止空气中的氧气与碘化钾反应
; (4)硫酸铜溶液与碘化钾溶液反应生成白色沉淀(碘化亚铜)并析出碘,该反应的离子方程式为:
2Cu2++4I-=2CuI↓+I2
2Cu2++4I-=2CuI↓+I2
;(5)根据本次实验结果,该胆矾试样中铜元素的质量分数ω(Cu)=
| 64cV |
| 1000a |
| 64cV |
| 1000a |