摘要:2.写出高锰酸钾与Na2C2O4反应的离子方程式,
网址:http://m.1010jiajiao.com/timu3_id_434550[举报]
(2013?临沭县模拟)塑化剂对人类健康影响较大,甚至会毒害人类基因.最近“酒鬼”酒因检测出塑化剂超标2.6倍,引起人们对塑化剂的恐慌.DBP是一种常用的塑化剂,学名叫“邻苯二甲酸二正丁酯”,可由石油产品乙烯和芳香烃A为原料经多步反应生成.下面是制作(DBP)的简易流程图:

已知:① (R、R′可以是烃基或H原子)
(R、R′可以是烃基或H原子)
②烯烃可以直接氧化生成醛类
请按照要求填写下列空白:
(1)实验室中完成由A到B的反应可以选用的试剂是
(2)已知B分子在核磁共振氢谱中能呈现三组峰,其峰面积之比为1:1:1,则B的结构简式为
 ,B分子所含官能团是
,B分子所含官能团是
(3)由乙烯到E最少需要经过四步化学反应,所涉及到的反应类型除加成反应外还有
(4)DBP的同分异构体中符合支链相同的邻苯二甲酸酯的共
(5)写出B与E生成DBP的化学方程式
 .
.
(6)F是B的一种同分异构体,具有如下特征:
a.是苯的间位二取代物; b.遇FeCl3溶液显示特征颜色;c.能与碳酸氢钠溶液反应.
写出F的结构简式
 .
.
查看习题详情和答案>>

已知:①
 (R、R′可以是烃基或H原子)
(R、R′可以是烃基或H原子)②烯烃可以直接氧化生成醛类
请按照要求填写下列空白:
(1)实验室中完成由A到B的反应可以选用的试剂是
酸性高锰酸钾溶液
酸性高锰酸钾溶液
(2)已知B分子在核磁共振氢谱中能呈现三组峰,其峰面积之比为1:1:1,则B的结构简式为


羧基
羧基
(填名称)(3)由乙烯到E最少需要经过四步化学反应,所涉及到的反应类型除加成反应外还有
氧化反应和消去反应
氧化反应和消去反应
(4)DBP的同分异构体中符合支链相同的邻苯二甲酸酯的共
3
3
种(不包括DBP本身)(5)写出B与E生成DBP的化学方程式


(6)F是B的一种同分异构体,具有如下特征:
a.是苯的间位二取代物; b.遇FeCl3溶液显示特征颜色;c.能与碳酸氢钠溶液反应.
写出F的结构简式


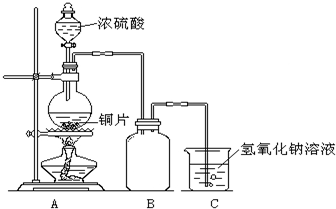 某化学课外兴趣小组为探究铜与浓硫酸的反应,用右图所示的装置进行实验:
某化学课外兴趣小组为探究铜与浓硫酸的反应,用右图所示的装置进行实验:请回答下列问题:
(1)B是用来收集实验中产生气体的装置,但未将导管画全,请将装置图补充完整.
(2)实验中他们取6.4g铜片和12mL18mol?L-1浓硫酸放在圆底烧瓶中共热,直到反应停止,最后发现烧瓶中还有铜片剩余,该小组中的同学认为还有一定量的硫酸剩余.
①写出铜与浓硫酸反应的化学方程式:
Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O
| ||
Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O
,
| ||
实验中若有m g铜参加了反应,则有
| m |
| 64 |
| m |
| 64 |
还原
还原
(填“氧化”或“还原”),转移电子的物质的量为| m |
| 32 |
| m |
| 32 |
②下列试剂中,能证明反应停止后烧瓶中有硫酸剩余的是
D
D
(填写字母编号).A.硫酸钠溶液 B.氯化钡溶液 C.银粉 D.碳酸钠溶液
③为什么有一定量的硫酸剩余但未能使铜片完全溶解?你认为的原因是
稀硫酸不与铜反应
稀硫酸不与铜反应
(3)为了测定剩余硫酸的物质的量浓度,该兴趣小组设计了三个实验方案:
方案一:将装置A产生的气体缓缓通过已称量过的装有碱石灰的干燥管,反应停止后再次称量,两次质量差即是吸收的二氧化硫.
方案二:将装置A产生的气体缓缓通入足量的用硫酸酸化的高锰酸钾溶液,再加入足量的氯化钡溶液,过滤、洗涤、干燥,称得沉淀的质量即是二氧化硫转化为硫酸钡沉淀的质量.
方案三:当铜和浓硫酸的反应结束后,在装置A中加入足量的锌粉,用排水法测得产生氢气的体积为V L(已换算为标准状况).
实际上,以上方案一、二均不可取,请你说出原因?
方案一
产生的气体中含有水蒸气,干燥管中的质量差不仅仅是SO2的质量(或烧瓶中的二氧化硫不能完全排出)
产生的气体中含有水蒸气,干燥管中的质量差不仅仅是SO2的质量(或烧瓶中的二氧化硫不能完全排出)
;方案二
沉淀的质量一部分是高锰酸钾溶液中起酸化作用的硫酸与氯化钡反应而产生的
沉淀的质量一部分是高锰酸钾溶液中起酸化作用的硫酸与氯化钡反应而产生的
.方案三:写出剩余硫酸的物质的量浓度的计算式(假设反应后溶液的体积仍为12mL)
| V |
| 22.4×0.012 |
| V |
| 22.4×0.012 |
(2011?内江三模)高锰酸钾是锸的重要化合物和常用的氧化剂.以下是工业上用软锰矿制备高锰酸钾的一种工艺流程.
(1)KMn04是
(2)写出K2Mn04溶液中通入CO2时发生的主要反应的离子方程式
(3)上述流程图中:①可以循环使用的物质有生石灰、二氧化碳.Mn02和
(4)实际生产中,常用硫酸工业的废气(含S02)与该厂的废水(含KMnO4)按一定比例混合,以减少工业“三废”对环境的污染.写出KMnO4与SO2反应的离子方程式为
(5)若不考虑物质循环与制备过程中的损失,则1mol MnO2可制得
查看习题详情和答案>>

(1)KMn04是
深紫色
深紫色
(填颜色)的晶体,其稀溶液是一种常用的消毒剂.其消毒机理与下列BD
BD
(填序号)物质相似.A.75%酒精 B.双氧水 C.苯酚 D.84消毒液(NaClO溶液)(2)写出K2Mn04溶液中通入CO2时发生的主要反应的离子方程式
3MnO42-+2CO2=2MnO4-+2CO32-+MnO2
3MnO42-+2CO2=2MnO4-+2CO32-+MnO2
(3)上述流程图中:①可以循环使用的物质有生石灰、二氧化碳.Mn02和
KOH
KOH
(写化学式);②KMn04粗晶体变为KMnO4纯晶伴,需经过步骤R,R为重结晶
重结晶
(填实验操作名称).(4)实际生产中,常用硫酸工业的废气(含S02)与该厂的废水(含KMnO4)按一定比例混合,以减少工业“三废”对环境的污染.写出KMnO4与SO2反应的离子方程式为
5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+
5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+
(5)若不考虑物质循环与制备过程中的损失,则1mol MnO2可制得
0.67
0.67
mol KMn04.
利用海水脱硫是处理火力发电排放出SO2的一种有效的方法,其工艺流如图所示:
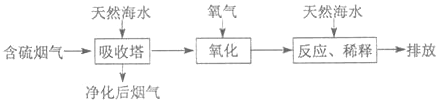
(1)天然海水呈碱性,写出SO2与OH-反应的离子方程式 .
(2)天然海水吸收了含硫烟气后会溶有H2SO3分子,使用氧气将其氧化的化学原理是 (用化学方程式表示).氧化后的“海水”需要引入大量的天然海水与之混合后才能排放,该操作的主要目的是 .
(3)为了测定炉气中SO2的体积百分含量,把500mL的炉气通入20mL 0.05mol/L的高锰酸钾溶液中,恰好使紫色刚好褪去.请回答:
①配平方程式: KMnO4-+ SO2+ H2O═ Mn2++ SO42-+
②测定结果炉气中SO2的含量为 .
(4)已知工业上利用可逆反应2SO2+O2
2SO3,△H<0,来制备硫酸,下列对该反应的说法正确的是 .
A.当单位时间内消耗2mol SO2的同时生成2mol SO3,说明该反应达到平衡
B.升高温度,可以增大正反应速率
C.恒容,通入氩气增大压强,促使平衡向右移动
D.工业上通过鼓入大量的空气而提高SO2的转化率
(5)某科研小组利用SO2、O2和稀H2SO4设计成原电池,该电池的负极反应为: .
查看习题详情和答案>>

(1)天然海水呈碱性,写出SO2与OH-反应的离子方程式
(2)天然海水吸收了含硫烟气后会溶有H2SO3分子,使用氧气将其氧化的化学原理是
(3)为了测定炉气中SO2的体积百分含量,把500mL的炉气通入20mL 0.05mol/L的高锰酸钾溶液中,恰好使紫色刚好褪去.请回答:
①配平方程式:
②测定结果炉气中SO2的含量为
(4)已知工业上利用可逆反应2SO2+O2
| 加热 | △ |
A.当单位时间内消耗2mol SO2的同时生成2mol SO3,说明该反应达到平衡
B.升高温度,可以增大正反应速率
C.恒容,通入氩气增大压强,促使平衡向右移动
D.工业上通过鼓入大量的空气而提高SO2的转化率
(5)某科研小组利用SO2、O2和稀H2SO4设计成原电池,该电池的负极反应为:
原子序数由小到大排列的四种短周期元素X、Y、Z、W,它们的原子序数之和为26,在同周期中W的原子半径最大,W和Z可形成W2Z和W2Z2;X、Y、Z三种元素中的任意两种之间可以组成甲、乙、丙…等许多种化合物.
(1)这四种元素的符号分别是X
 .
.
(2)甲是一种气体,通入紫色石蕊试液中,溶液变红.甲的分子式为
(3)乙是一种化石燃料,其分子呈正四面体构型,写出它的电子式
 ;560mL(标准状况下)乙完全燃烧生成液态水,产生热量22.25kJ.写出乙燃烧热的热化学方程式为
;560mL(标准状况下)乙完全燃烧生成液态水,产生热量22.25kJ.写出乙燃烧热的热化学方程式为
(4)丙是X和Z按原子个数比1:1组成的化合物.已知丙的溶液能使酸性高锰酸钾溶液褪色.将含有0.5mol丙的溶液滴加到100mL 2mol?L-1酸性高锰酸钾溶液中,溶液紫色恰好褪色.该反应的离子方程式为:
查看习题详情和答案>>
(1)这四种元素的符号分别是X
H
H
、YC
C
、ZO
O
、WNa
Na
,用电子式表示W2Z形成过程

(2)甲是一种气体,通入紫色石蕊试液中,溶液变红.甲的分子式为
CO2
CO2
,写出甲与W2Z2反应的化学方程式2CO2+2Na2O2=2Na2CO3+O2
2CO2+2Na2O2=2Na2CO3+O2
.(3)乙是一种化石燃料,其分子呈正四面体构型,写出它的电子式


CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H═-890kJ?mol-1
CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H═-890kJ?mol-1
.(4)丙是X和Z按原子个数比1:1组成的化合物.已知丙的溶液能使酸性高锰酸钾溶液褪色.将含有0.5mol丙的溶液滴加到100mL 2mol?L-1酸性高锰酸钾溶液中,溶液紫色恰好褪色.该反应的离子方程式为:
2MnO4-+5H2O2+6H+=2Mn2++8H2O+502 ↑
2MnO4-+5H2O2+6H+=2Mn2++8H2O+502 ↑
.