摘要:金属铌能与卤素形成簇状化合物.下图所示为三种NbaXb的结构单元.它们的共同特点是六个Nb原子形成八面体骨架.卤原子通过双桥基(-X-)或三桥基()与Nb原子相连.结构单元之间通过双桥基相连.请据图写出以下三个物质的化学式:
网址:http://m.1010jiajiao.com/timu3_id_434516[举报]
有一元素能与卤素形成卤化物,经测定此气态卤化物对空气的相对密度是6.55,该元素在此卤化物中占25.2%,而此元素在同价态的氧化物中占60%(均为质量百分数),此元素原子核中,质子数与中子数之比为11∶13.求:
(1)此元素的原子序数;
(2)该元素卤化物的分子式.
查看习题详情和答案>>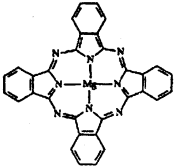 能源问题日益成为制约国际社会经济发展的瓶颈,越来越多的国家开始实行“阳光计划”,开发太阳能资源,寻求经济发展的新动力.
能源问题日益成为制约国际社会经济发展的瓶颈,越来越多的国家开始实行“阳光计划”,开发太阳能资源,寻求经济发展的新动力.(1)太阳能热水器中常使用一种以镍或镍合金空心球为吸收剂的太阳能吸热涂层.
①请写出基态镍原子的核外电子排布式
1S22S22P63S23P63d84s2
1S22S22P63S23P63d84s2
.②NiO、FeO的晶体结构类型均与氯化钠相同,Ni2+和Fe2+的离子半径分别为69pm和78pm,则熔点NiO
>
>
(填“<”或“>”)FeO;③Ni、Fe、Co等金属都能与CO反应形成配合物,Fe(CO)5常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)5晶体属于
分子晶体
分子晶体
(填晶体类型);配位体是CO
CO
.(2)金属酞菁配合物在硅太阳能电池中有重要作用,一种金属镁酞菁配合物的结构如下图,请在下图中用箭头表示出配位键.
(3)CO与N2互为等电子体.CO的总键能大于N2的总键能,但CO比N2容易参加化学反应.根据下表数据,说明CO比N2活泼的原因是
反应中,CO中首先断裂的那个π键的键能比N2的小很多,所以CO更容易发生反应
反应中,CO中首先断裂的那个π键的键能比N2的小很多,所以CO更容易发生反应
.| A-B | A=B | A≡B | ||
| CO | 键能(kJ?mol-1) | 357.7 | 798.9 | 1071.9 |
| 键能差值(kJ?mol-1) | 441.2 273 | |||
| N2 | 键能(kJ?mol-1) | 154.8 | 418.3 | 941.7 |
| 键能差值(kJ?mol-1) | 263.6 523.3 | |||
1
1
个σ键、2
2
个π键.