摘要:(一)必考题 26.2由于在空气中易被氧化.制取时很难观察到白色沉淀现象.只能看到灰绿色.采用右图装置使用Fe.H2SO4(稀).NaOH溶液可在还 原性气氛中制取Fe(OH)2白色沉淀.且较长时间内不变色.其 中C为弹簧夹.(提示:还原性气氛如氢气环境) (1)则锥形瓶A中应加入的药品为 . (2)锥形瓶B中应加入的药品为 . (3)容器A中的反应开始后.请简单写出完成制备Fe(OH)2 的后续操作步骤. ① ② . (4)若在反应开始之前先关闭弹簧夹C.则实验现象为: , 请写出此时B瓶中发生的化学反应的离子方程式: , 27.下列图中A-F是中学化学常见化合物,且A﹑B﹑E﹑F均含有相同一种金属元素.G是一种常见单质. ①A B + C + D ②C + E → B + G; ③ D + E → F + G ④A→B + C + D → A (1)写出A﹑B﹑C﹑E﹑F的化学式:A B C E F (2)写出反应①②④⑤的化学方程式: ① ② ④ ⑤ (3)请写出化合物E的两种重要用途: 28.现有浓度各为1 mol/L的FeCl3.FeCl2.CuCl2的混合溶液100mL.加入一定量的铁粉.按下列情况填空: ①充分反应后铁粉有剩余.则溶液中一定含有 阳离子,一定没有 阳离子.有关反应的离子方程式是 . ②充分反应后铁粉无剩余.有铜生成.则反应后的溶液中一定含有 阳离子,溶液中可能含有 阳离子.该阳离子在溶液中物质的量的可能存在范围是: . ③充分反应后.无固体沉淀物存在.反应后的溶液中一定含有 和 阳离子. (2)现有AlCl3和FeCl3的混合溶液.其中Al3+ 和Fe3+ 的物质的量之和为0.1 mol.在此溶液中加入90 mL 4 mol / L的NaOH溶液.使其充分反应;设Al3+ 的物质的量与总物质的量的比值为x. ①根据反应的化学方程式计算x=0.4时.溶液中产生的沉淀是 ;物质的量是 mol. ②计算沉淀中只有Fe(OH)3时的x的取值范围: .
网址:http://m.1010jiajiao.com/timu3_id_434090[举报]
(2013?浙江模拟)必考题二甲醚(CH3OCH3)和甲醇(CH3OH)被称为21世纪的新型燃料.以CH4和H2O为原料制备二甲醚和甲醇的工业流程如下:请填空:

(1)在一定条件下,反应室1中发生反应:CH4(g)+H2O(g) CO(g)+3H2(g)△H>0.在其它条件不变的情况下降低温度,逆反应速率将
CO(g)+3H2(g)△H>0.在其它条件不变的情况下降低温度,逆反应速率将
(2)在一定条件下,已知反应室2的可逆反应除生成二甲醚外还生成了气态水,其化学方程式为
(3)在压强为0.1MPa条件下,反应室3(容积为VL)中amolCO与2amolH2在催化剂作用下反应生成甲醇:CO(g)+2H2(g) CH3OH(g),CO的平衡转化率与温度、压强的关系如图所示,则:
CH3OH(g),CO的平衡转化率与温度、压强的关系如图所示,则:
①P1
②在其它条件不变的情况下,反应室3再增加amolCO与2amolH2,达到新平衡时,CO的转化率
③在P1压强下,100℃时,CH3OH(g) CO(g)+2H2(g)反应的平衡常数为
CO(g)+2H2(g)反应的平衡常数为
(用含a、V的代数式表示).
查看习题详情和答案>>

(1)在一定条件下,反应室1中发生反应:CH4(g)+H2O(g)
 CO(g)+3H2(g)△H>0.在其它条件不变的情况下降低温度,逆反应速率将
CO(g)+3H2(g)△H>0.在其它条件不变的情况下降低温度,逆反应速率将减小
减小
(填“增大”、“减小”或“不变”).将1.0molCH4和2.0molH2O通入反应室1(假设容积为100L),10min末有0.1molCO生成,则10min内反应的平均速率V(H2)=0.0003mol?L-1?min-1
0.0003mol?L-1?min-1
.(2)在一定条件下,已知反应室2的可逆反应除生成二甲醚外还生成了气态水,其化学方程式为
2CO+4H2 CH3OCH3+H2O
CH3OCH3+H2O
 CH3OCH3+H2O
CH3OCH3+H2O2CO+4H2 CH3OCH3+H2O
CH3OCH3+H2O
. CH3OCH3+H2O
CH3OCH3+H2O(3)在压强为0.1MPa条件下,反应室3(容积为VL)中amolCO与2amolH2在催化剂作用下反应生成甲醇:CO(g)+2H2(g)
 CH3OH(g),CO的平衡转化率与温度、压强的关系如图所示,则:
CH3OH(g),CO的平衡转化率与温度、压强的关系如图所示,则:①P1
<
<
P2 (填“<”、“>”或“=“).②在其它条件不变的情况下,反应室3再增加amolCO与2amolH2,达到新平衡时,CO的转化率
增大
增大
(填“增大”、“减小”或“不变”.下同.),平衡常数不变
不变
.③在P1压强下,100℃时,CH3OH(g)
 CO(g)+2H2(g)反应的平衡常数为
CO(g)+2H2(g)反应的平衡常数为| a2 |
| V2 |
| a2 |
| V2 |
【必考题】
过氧化尿素[CO(NH2)2?H2O2]是一种无毒、无味的白色结晶粉末,具有尿素和过氧化氢双重性质,是一种新型的氧化剂和消毒剂,广泛应用于漂白、纺织、医药、农业、养殖业等领域.其合成如下:

试回答下列问题:
(1)实际生产中需控制n(H2O2):n(CO(NH2)2)]=1.2:1,并控制合成温度在25-30℃,其主要原因是
(2)从母液中分离出H2O2和尿素,采用的操作是
(a)盐析 过滤 (b)分液 过滤 (c)减压蒸馏 结晶 (d)常压蒸馏 萃取
(3)为测定产品中活性氧的含量(活性氧16%,相当于H2O234%),称取干燥样品12.000g,溶解,在250mL容量瓶中定容.准确量取25.00mL于锥形瓶中,加入1mL 6mol/L的硫酸,然后用0.2000mol/L KMnO4 标准溶液滴定,至滴入最后一滴时,溶液显浅红色且半分钟内不褪色,三次滴定平均消耗KMnO4溶液20.00mL(KMnO4溶液与尿素不反应).
①KMnO4溶液应盛放在
②完成并配平方程式:
③根据滴定结果,可确定产品中活性氧的质量分数为:
④若滴定前滴定管尖嘴处有气泡,滴定后消失,会使测得的活性氧含量
⑤根据本次实验测得的活性氧含量,可判断该实验产品所含的一种主要杂质为
查看习题详情和答案>>
过氧化尿素[CO(NH2)2?H2O2]是一种无毒、无味的白色结晶粉末,具有尿素和过氧化氢双重性质,是一种新型的氧化剂和消毒剂,广泛应用于漂白、纺织、医药、农业、养殖业等领域.其合成如下:

试回答下列问题:
(1)实际生产中需控制n(H2O2):n(CO(NH2)2)]=1.2:1,并控制合成温度在25-30℃,其主要原因是
H2O2在实验过程中会有部分分解,增大过氧化氢的量可提高过氧化尿素的纯度
H2O2在实验过程中会有部分分解,增大过氧化氢的量可提高过氧化尿素的纯度
.(2)从母液中分离出H2O2和尿素,采用的操作是
c
c
.(a)盐析 过滤 (b)分液 过滤 (c)减压蒸馏 结晶 (d)常压蒸馏 萃取
(3)为测定产品中活性氧的含量(活性氧16%,相当于H2O234%),称取干燥样品12.000g,溶解,在250mL容量瓶中定容.准确量取25.00mL于锥形瓶中,加入1mL 6mol/L的硫酸,然后用0.2000mol/L KMnO4 标准溶液滴定,至滴入最后一滴时,溶液显浅红色且半分钟内不褪色,三次滴定平均消耗KMnO4溶液20.00mL(KMnO4溶液与尿素不反应).
①KMnO4溶液应盛放在
酸
酸
式(选填:“酸”、“碱”)滴定管中.②完成并配平方程式:
2
2
MnO4-+5
5
H2O2+6
6
H+=2
2
Mn2++8
8
H2O+5O2
5O2
③根据滴定结果,可确定产品中活性氧的质量分数为:
13.3%
13.3%
.④若滴定前滴定管尖嘴处有气泡,滴定后消失,会使测得的活性氧含量
偏高
偏高
(选填:“偏高”、“偏低”或“不变”).⑤根据本次实验测得的活性氧含量,可判断该实验产品所含的一种主要杂质为
尿素
尿素
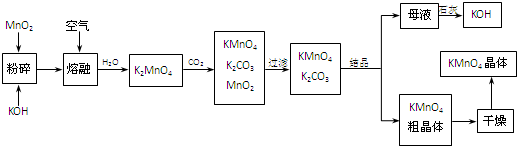
.必考题高锰酸钾是锰的重要化合物和常用的氧化剂.以下是工业上用软锰矿制备高锰酸钾的一种工艺流程.

(1)KMnO4稀溶液是一种常用的消毒剂.其消毒机理与下列
A.75%酒精 B.双氧水 C.苯酚 D.84消毒液(NaClO溶液)
(2)写出MnO2、KOH的熔融混合物中通入空气时发生的主要反应的化学方程式:
(3)向K2MnO4溶液中通入CO2以制备KMnO4,该反应中的还原剂是:
(4)上述流程中可以循环使用的物质有石灰、二氧化碳、
(5)若不考虑物质循环与制备过程中的损失,则1mol MnO2可制得
mol KMnO4.
查看习题详情和答案>>

(1)KMnO4稀溶液是一种常用的消毒剂.其消毒机理与下列
BD
BD
(填序号)物质相似.A.75%酒精 B.双氧水 C.苯酚 D.84消毒液(NaClO溶液)
(2)写出MnO2、KOH的熔融混合物中通入空气时发生的主要反应的化学方程式:
2MnO2+4KOH+O2
2K2MnO4+2H2O
| ||
2MnO2+4KOH+O2
2K2MnO4+2H2O
.
| ||
(3)向K2MnO4溶液中通入CO2以制备KMnO4,该反应中的还原剂是:
K2MnO4
K2MnO4
.(4)上述流程中可以循环使用的物质有石灰、二氧化碳、
KOH
KOH
和MnO2
MnO2
(写化学式).(5)若不考虑物质循环与制备过程中的损失,则1mol MnO2可制得
| 2 |
| 3 |
| 2 |
| 3 |