摘要: 已知: CH3CH2OH CH3COOCH2CH3 自动失水 R CH OH RCH=O+H2O OH 现在只含C.H.O的化合物A─F.有关它们的某些信息.已注明在下面的方框内. (1)在A─F化合物中.含有酯的结构的化合物是 . (2)写出化合物A和F结构简式 . (3)写出化学方程式: B→C D→E
网址:http://m.1010jiajiao.com/timu3_id_409661[举报]
科学家发现某药物M能治疗心血管疾病,是因为它在人体内释放出一种“信使分子D”。并阐明了D在人体内的作用原理。为此他们荣获了1998年诺贝尔生理学或医学奖。
(1)已知M的分子量为227,由C、H、O、N四种元素组成,C、H、N的质量分数依次为15.86%、2.20%、18.50%,则M的分子式是____,D是双原子分子,相对分子质量为30,则D的分子式是____。
(2)油脂A经下列途径可制得M
(1)已知M的分子量为227,由C、H、O、N四种元素组成,C、H、N的质量分数依次为15.86%、2.20%、18.50%,则M的分子式是____,D是双原子分子,相对分子质量为30,则D的分子式是____。
(2)油脂A经下列途径可制得M

图中②的提示:CH3CH2OH+HO-NO2(硝酸) CH3CH2O-NO2(硝酸乙酯)+H2O
CH3CH2O-NO2(硝酸乙酯)+H2O
反应①的化学方程式是_________________,反应②的化学方程式是________________。
(3)C是B与乙酸在一定条件下反应生成的化合物,相对分子质量为134,写出C所有可能的结构简式__________。
(4)若将0.1 mol B与足量Na反应,则需消耗_______g Na。
查看习题详情和答案>>
 CH3CH2O-NO2(硝酸乙酯)+H2O
CH3CH2O-NO2(硝酸乙酯)+H2O 反应①的化学方程式是_________________,反应②的化学方程式是________________。
(3)C是B与乙酸在一定条件下反应生成的化合物,相对分子质量为134,写出C所有可能的结构简式__________。
(4)若将0.1 mol B与足量Na反应,则需消耗_______g Na。
(2009?泰安模拟)有关元素X、Y、Z、D、E的信息如下:
(1)画出Y的离子结构示意图
 ;
;
(2)写出D的最高价氧化物的水化物电离出的阴离子的电子式
 ;
;
(3)D2ZX3的溶液与Y的单质可能发生反应,其反应的离子方程式为
(4)用化学符号表示D2EX3的水溶液中各离子的浓度关系(列等式)
(5)已知ZX2与X2可发生反应:2ZX2(g)+X2(g)?2ZX3(g)△H<0;
当反应达到平衡时不断改变条件(不改变ZX2、X2、ZX3的量),反应速率随时间的变化如图:
其中表示平衡混合物中ZX3含量最高的一段时间是
(填“大于”、“等于”或“小于”).
查看习题详情和答案>>
| 元素 | 有关信息 |
| X | 元素主要化合价为-2,原子半径为0.074nm |
| Y | 所在主族序数与所在周期序数之差为4 |
| Z | 原子半径为0.102nm,其单质在X的单质中燃烧,发出明亮的蓝紫色火焰 |
| D | 最高价氧化物对应的水化物,能按1:1电离出电子数相等的阴、阳离子 |
| E | 其单质有多种同素异形体,一种为自然界中硬度最大 |


(2)写出D的最高价氧化物的水化物电离出的阴离子的电子式


(3)D2ZX3的溶液与Y的单质可能发生反应,其反应的离子方程式为
SO32-+Cl2+H2O=SO42-+2Cl-+2H+;
SO32-+Cl2+H2O=SO42-+2Cl-+2H+;
;(4)用化学符号表示D2EX3的水溶液中各离子的浓度关系(列等式)
c(Na+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-)
c(Na+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-)
;(5)已知ZX2与X2可发生反应:2ZX2(g)+X2(g)?2ZX3(g)△H<0;
当反应达到平衡时不断改变条件(不改变ZX2、X2、ZX3的量),反应速率随时间的变化如图:

其中表示平衡混合物中ZX3含量最高的一段时间是
t0~t1
t0~t1
;如t0~t1平衡常数为K1,t2~t3平衡常数为K2,则K1大于
大于
K2(填“大于”、“等于”或“小于”).
(2011?龙岩模拟)甲、乙、丙、丁均为中学常见物质,且甲、乙、丙均含有同一种元素.一定条件下四种物质之间有如图甲所示的转化关系.请回答问题:
(1)若甲、丁分别为铁和氯气中的一种,则丙的酸性溶液露置于空气中将变质.变质过程所发生反应的离子方程式为
(2)已知乙、丁均为空气中含量最多的两种单质,且由甲、丁和NaOH溶液构成的新型燃料电池放电时甲与丁作用转化为乙(同时生成一种对生命活动有重要意义的物质),负极反应式为
(3)图示转化关系对应的反应既可以是非氧化还原反应,也可以是氧化还原反应.
①若丁为盐酸且反应均为非氧化还原反应,则甲的水溶液的pH比丙的水溶液的pH
②若丁为单质,下列关于物质乙、丙所含的同一元素的价态的推断,正确的是
a、乙一定更高 b、丙一定更高 c、乙和丙一样高 d、无法确定
(4)高温下,利用天然气生产合成气的过程涉及上述图示转化关系(生成的H2未标出),且丙能使石灰水变浑浊、“甲→乙”对应的反应为:CH4+H2O-CO+H2(未配平,条件略).
①当1mol甲与丁反应转化为乙时吸收206.1kJ的热量,1mol乙与丁反应转化为丙时放出41.2kJ的热量.则甲与丁直接转化为乙的热化学方程式为
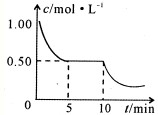
②将甲与丁混合于容积不变密闭容器中,甲将转化为乙,且反应过程中甲浓度变化情况如图所示.试推测:反应10min时,改变的外界条件可能是
③t℃时,乙转化为丙反应化学平衡常数K=1.0,某时刻测得该温度下的密闭容器中乙、丁、丙和氢气的物质的量依次为0.5mol、8.5mol、2.0mol和2.0mol.此时反应正、逆反应速率的关系式是
a.v(正)>v(逆) b.v(正)<v(逆) c.v(正)=v(逆) D.无法判断.
查看习题详情和答案>>
(1)若甲、丁分别为铁和氯气中的一种,则丙的酸性溶液露置于空气中将变质.变质过程所发生反应的离子方程式为
4Fe2++O2+4H+═4Fe3++2H2O
4Fe2++O2+4H+═4Fe3++2H2O
.(2)已知乙、丁均为空气中含量最多的两种单质,且由甲、丁和NaOH溶液构成的新型燃料电池放电时甲与丁作用转化为乙(同时生成一种对生命活动有重要意义的物质),负极反应式为
2NH3+6OH-═N2+6H2O+6e-
2NH3+6OH-═N2+6H2O+6e-
.(3)图示转化关系对应的反应既可以是非氧化还原反应,也可以是氧化还原反应.
①若丁为盐酸且反应均为非氧化还原反应,则甲的水溶液的pH比丙的水溶液的pH
大
大
(填“大”或“小”).②若丁为单质,下列关于物质乙、丙所含的同一元素的价态的推断,正确的是
d
d
.a、乙一定更高 b、丙一定更高 c、乙和丙一样高 d、无法确定
(4)高温下,利用天然气生产合成气的过程涉及上述图示转化关系(生成的H2未标出),且丙能使石灰水变浑浊、“甲→乙”对应的反应为:CH4+H2O-CO+H2(未配平,条件略).
①当1mol甲与丁反应转化为乙时吸收206.1kJ的热量,1mol乙与丁反应转化为丙时放出41.2kJ的热量.则甲与丁直接转化为乙的热化学方程式为
CH4(g)+2H2O=CO2(g)+4H2(g)△H=+164.9KJ/mol
CH4(g)+2H2O=CO2(g)+4H2(g)△H=+164.9KJ/mol
(丁均为气态).②将甲与丁混合于容积不变密闭容器中,甲将转化为乙,且反应过程中甲浓度变化情况如图所示.试推测:反应10min时,改变的外界条件可能是
降低温度
降低温度
.
③t℃时,乙转化为丙反应化学平衡常数K=1.0,某时刻测得该温度下的密闭容器中乙、丁、丙和氢气的物质的量依次为0.5mol、8.5mol、2.0mol和2.0mol.此时反应正、逆反应速率的关系式是
a
a
(填代号).a.v(正)>v(逆) b.v(正)<v(逆) c.v(正)=v(逆) D.无法判断.