网址:http://m.1010jiajiao.com/timu3_id_406375[举报]
考生必须从中选择1道题作答。
1.【化学—化学与技术】金属铝的生产是以Al2O3为原料,在熔融状态下进行电解:2Al2O3![]() 4Al+3O2↑
4Al+3O2↑
请回答下列问题:
(1)冰晶石(Na3AlF6)的作用是___________________。
(2)电解生成的金属铝是在熔融液的______________(填“上层”或“下层”)。
(3)阴极和阳极均由______________材料做成;电解时不断消耗的电极是___________(填“阳极”或“阴极”)。
(4)铝是高耗能产品,废旧铝材的回收利用十分重要。在工业上,最能体现节能减排思想的是将回收铝做成______________(填代号)。
a.冰晶石 b.氧化铝 c.铝锭 d.硫酸铝
2.【化学—物质结构与性质】
C和Si元素在化学中占有极其重要的地位。
(1)写出Si的基态原子核外电子排布式______________。从电负性角度分析,C、Si和O元素的非金属活泼性由强至弱的顺序为______________。
(2)SiC的晶体结构与晶体硅的相似,其中C原子的杂化方式为______________,微粒间存在的作用力是______________。
(3)氧化物MO的电子总数与SiC的相等,则M为______________(填元素符号)。MO是优良的耐高温材料,其晶体结构与NaCl晶体相似。MO的熔点比CaO的高,其原因是_________________________。
(4)C、Si为同一主族的元素,CO2和SiO2化学式相似,但结构和性质有很大不同。CO2中C与O原子间形成σ键和π键,SiO2中Si与O原子间不形成上述π键。从原子半径大小的角度分析,为何C、O原子间能形成,而Si、O原子间不能形成上述π键。___________。
3.【化学—有机化学基础】
下图中X是一种具有水果香味的合成香料,A是直链有机物,E与FeCl3溶液作用显紫色。

请根据上述信息回答:
(1)H中含氧官能团的名称是____________,B→I的反应类型为____________。
(2)只用一种试剂鉴别D、E、H,该试剂是____________。
(3)H与J互为同分异构体,J在酸性条件下水解有乙酸生成,J的结构简式为____________。
(4)D和F反应生成X的化学方程式为____________________________________。
查看习题详情和答案>>A.H2S未溶解在水中时以分子态存在,溶解于水时形成的氢硫酸中有部分发生电离,但是溶解于水时尽管能够导电,却违背了电解质定义的第二个原则:必须是针对“化合物”而不是“混合物”
B.液态硫化氢不是酸,它是硫的氢化物,只有当硫化氢溶于水时才是酸(氢硫酸),所以硫化氢不是电解质
C.在受水分子作用或受热熔化时,化合物本身直接电离出自由移动离子的化合物,才是电解质
D.氢硫酸是混合物,所以不是电解质 查看习题详情和答案>>
A.H2S未溶解在水中时以分子态存在,溶解于水时形成的氢硫酸中有部分发生电离,但是溶解于水时尽管能够导电,却违背了电解质定义的第二个原则:必须是针对“化合物”而不是“混合物”
B.液态硫化氢不是酸,它是硫的氢化物,只有当硫化氢溶于水时才是酸(氢硫酸),所以硫化氢不是电解质
C.在受水分子作用或受热熔化时,化合物本身直接电离出自由移动离子的化合物,才是电解质
D.氢硫酸是混合物,所以不是电解质 查看习题详情和答案>>
 第四周期元素的单质及化合物在工农业生产中应用广泛.
第四周期元素的单质及化合物在工农业生产中应用广泛.(1)第四周期元素中,基态原子的最外层只有1个电子的元素共有
(2)铂丝蘸取氯化钙在酒精灯上灼烧,火焰呈现砖红色,显色原因是
A.氯化钙受热挥发 B.氯化钙受热分解
C.钙离子中电子跃迁 D.氯离子中电子跃迁
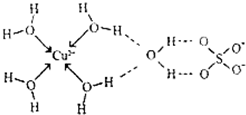
(3)无水硫酸铜呈白色,吸水后形成胆矾,呈蓝色.科学家通过X射线测定出胆矾的结构,其结构可用图表示.
①胆矾晶体中除共价键、配位键及微弱的范德华力外,还存在的两种作用力是
②胆矾晶体CuSO4?5H2O可以写出[Cu(H2O)4]SO4?H2O,其中中心原子(离子)是
③铜离子形成胆矾中配位离子的离子方程式为
(4)Mn、Fe均为第四周期过渡元素,两元素的部分电离能数据如表.据表判断Mn2+和Fe2+再失去-个电子的难易,并从原子结构的角度简述其原因:
| 元素 | Mn | Fe | |
| 电离能kJ?mol-1 | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
