摘要: (1)2FeSO4·7H2O=======Fe2O3+SO2 ↑+SO3↑+14H2O (2)SO2为大气污染物.缺少尾气处理装置 (3)3CH3CH2OH+Fe2O3 2Fe+3CH3CHO+3H2O (4)关闭活塞K.将E的导气管插入水中.微热C管.E中有气泡产生.停止加热后.E管出现一段水柱.说明装置下漏气. (5)防止倒吸 (6)CH3CHO+2Ag(NH3)2OH CH3COONH4+2Ag↓+3NH3+H2O
网址:http://m.1010jiajiao.com/timu3_id_405275[举报]
FeSO4?7H2O广泛用于医药和工业领域.
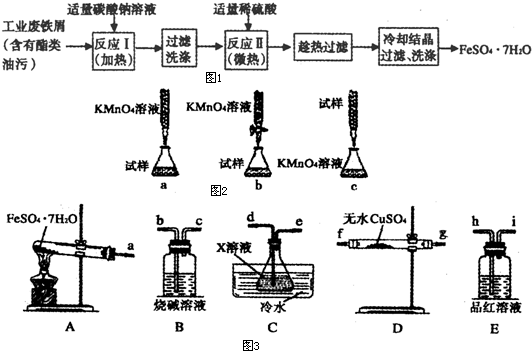
(1)如图1是以工业废铁屑为原料生产FeSO4?7H2O的流程图.
请填写下列空白.
①加适量碳酸钠溶液的目的是 ,反应I需要加热数分钟,其原因是 .
②判断反应Ⅱ完成的现象是 .反应Ⅱ需要100mL1mol/L的稀硫酸,用98.3%,ρ=1.84g/cm3的浓硫酸配制.所用的仪器有量筒、烧杯、玻璃棒、胶头滴管及 .
③测定FeSO4?7H2O产品中Fe2+含量的方法是用KMnO4溶液滴定法(5Fe2++Mn
+8H+=5Fe3++Mn2++4H2O),步骤为:
Ⅰ称取2.8500g FeSO4?7H2O产品,配制成250mL溶液;
Ⅱ量取25.00mL待测溶液于锥形瓶中;
Ⅲ.用硫酸酸化的0.01000moL/L KMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL.
某同学设计如图2所示的滴定方式中,最合理的是 (夹持部分略去)(填字母序号);判断此滴定实验达到终点的方法是 ;计算上述样品中FeSO4?7H2O的质量分数为 (用小数表示,保留三位小数);若用上述方法测定的样品中FeSO4?7H2O的质量分数偏低(测定过程中产生的误差可忽略),其可能原因有 ; .
(2)已知FeSO4?7H2O晶体在加热条件下发生如下反应:2FeSO4?7H2O
Fe2O3+SO2↑+SO3↑+14H2O↑.利用图3装置可检验该反应的气体产物.
请填写下列空白.
①仪器的连接顺序为a接 、 接 、 接 、 接 .
②装置C中的X为 ;该装置中冷水的作用是 .
查看习题详情和答案>>

(1)如图1是以工业废铁屑为原料生产FeSO4?7H2O的流程图.
请填写下列空白.
①加适量碳酸钠溶液的目的是
②判断反应Ⅱ完成的现象是
③测定FeSO4?7H2O产品中Fe2+含量的方法是用KMnO4溶液滴定法(5Fe2++Mn
| O | - 4 |
Ⅰ称取2.8500g FeSO4?7H2O产品,配制成250mL溶液;
Ⅱ量取25.00mL待测溶液于锥形瓶中;
Ⅲ.用硫酸酸化的0.01000moL/L KMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL.
某同学设计如图2所示的滴定方式中,最合理的是
(2)已知FeSO4?7H2O晶体在加热条件下发生如下反应:2FeSO4?7H2O
| ||
请填写下列空白.
①仪器的连接顺序为a接
②装置C中的X为
如图中,B、D、E、F、G是氧化物,F、K是氢化物,C、H是日常生活中最常见的金属单质,J是气态非金属单质.O是白色沉淀且B、H、L、M、N、O中含有同种元素,I是基础化学工业的重要产品(图中部分反应物和生成物没有列出).
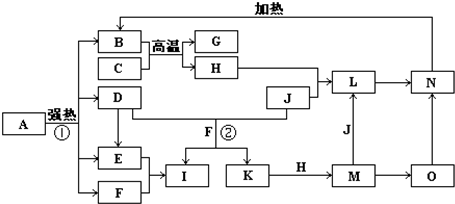
请按要求回答:
(1)写出G、L的化学式G:
(2)反应②的离子方程式
(3)反应①是分解反应,反应中生成的B、D、E、F的物质的量之比为1:1:1:14,则该反应的化学方程式为
(4)将A直接溶于水(未加稀硫酸酸化)得到的溶液,敞口久置,变质过程中涉及的离子方程式为
查看习题详情和答案>>

请按要求回答:
(1)写出G、L的化学式G:
Al2O3
Al2O3
,L:FeCl3
FeCl3
.(2)反应②的离子方程式
SO2+Cl2+2H2O=4H++SO42-+2Cl-
SO2+Cl2+2H2O=4H++SO42-+2Cl-
.(3)反应①是分解反应,反应中生成的B、D、E、F的物质的量之比为1:1:1:14,则该反应的化学方程式为
2FeSO4?7H2O
Fe2O3+SO2↑+SO3↑+14H2O
| ||
2FeSO4?7H2O
Fe2O3+SO2↑+SO3↑+14H2O
.
| ||
(4)将A直接溶于水(未加稀硫酸酸化)得到的溶液,敞口久置,变质过程中涉及的离子方程式为
12Fe2++3O2+6H2O=8Fe3++4Fe(OH)3↓
12Fe2++3O2+6H2O=8Fe3++4Fe(OH)3↓
.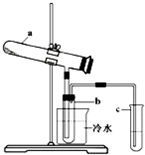 生产硫酸最古老的方法是以绿矾为原料,在蒸馏釜中煅烧.反应的化学方程式为:
生产硫酸最古老的方法是以绿矾为原料,在蒸馏釜中煅烧.反应的化学方程式为:2FeSO4?7H2O
| ||
查看习题详情和答案>>
某研究性学习小组从网上查到绿矾(FeSO4?7H2O)受热分解的方程式为2FeSO4?7H2O
Fe2O3+SO2↑+SO3↑+14H2O↑,设计了如图所示实验装置来验证绿矾受热分解是否发生上述反应.
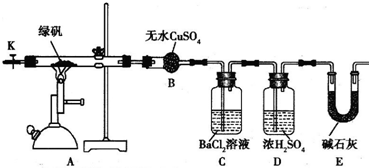
主要实验步骤如下:
①组装仪器并检查装置的气密性;
②称量绿矾样品及U形干燥管E的质量,将称量后的绿矾置于硬质玻璃管内;
③关闭活塞K,加强热使绿矾完全分解;
④打开活塞K,缓缓鼓入一定量的氮气;
⑤再次称量干燥管E的质量;
⑥重复步骤④⑤的操作,直到干燥管E的质量基本不变为止;
⑦称量洗气瓶C中所得沉淀的质量.试回答下列问题:
(1)洗气瓶D中浓H2SO4的作用为 .
(2)步骤⑦从溶液中获取沉淀质量的具体操作为 .
(3)实验小组的报告如下,请补充完整:
(4)该实验所得到的数据与所查到的化学方程式中的定量关系不相符合,请分析可能的原因:
(两条即可).
(5)为达到“验证绿矾受热分解是否发生上述反应”的目的,该实验的设计有多处不妥,请提出改进建议: (两条即可).
查看习题详情和答案>>
| ||

主要实验步骤如下:
①组装仪器并检查装置的气密性;
②称量绿矾样品及U形干燥管E的质量,将称量后的绿矾置于硬质玻璃管内;
③关闭活塞K,加强热使绿矾完全分解;
④打开活塞K,缓缓鼓入一定量的氮气;
⑤再次称量干燥管E的质量;
⑥重复步骤④⑤的操作,直到干燥管E的质量基本不变为止;
⑦称量洗气瓶C中所得沉淀的质量.试回答下列问题:
(1)洗气瓶D中浓H2SO4的作用为
(2)步骤⑦从溶液中获取沉淀质量的具体操作为
(3)实验小组的报告如下,请补充完整:
| 实验记录 | 分析或计算结果 | |
| 现象 | 硬质玻璃管内物质由绿色变为红棕色 | 生成物有 |
| 干燥管B中晶体由白色变为蓝色 | 生成物有H2O | |
| 数据 | 称取绿矾样品16.68g | 反应的绿矾的物质的量为0.06mol |
| 干燥管E最后增加的质量2.24g | 生成SO2 | |
| C中生成白色沉淀的质量为4.66g | 生成SO3 0.02mol |
(5)为达到“验证绿矾受热分解是否发生上述反应”的目的,该实验的设计有多处不妥,请提出改进建议:
已知FeSO4?7H2O晶体在加热条件下发生如下反应:2FeSO4?7H2O
Fe2O3+SO2↑+SO3↑+14H2O↑;如图的装置可用来检验上述反应中所有的气体产物,请回答下列问题:

(1)用于检验SO2气体的装置是 (填装置的字母),确认水蒸气存在的现象是 ;
(2)利用装置B可以确认的产物是 ,装置B中的甲溶液可选(填序号) ,
①足量澄清石灰水 ②足量氯化钡溶液 ③足量硝酸钡溶液
该装置中冷水的作用是 ;
(3)为探究Fe2O3的性质和用途,取试管中少许固体溶于适量盐酸中制备饱和铁盐溶液,将此饱和溶液逐滴加入沸水中加热片刻,观察液体的颜色变为 ,检验该分散系最简方法的操作为 .
查看习题详情和答案>>
| ||

(1)用于检验SO2气体的装置是
(2)利用装置B可以确认的产物是
①足量澄清石灰水 ②足量氯化钡溶液 ③足量硝酸钡溶液
该装置中冷水的作用是
(3)为探究Fe2O3的性质和用途,取试管中少许固体溶于适量盐酸中制备饱和铁盐溶液,将此饱和溶液逐滴加入沸水中加热片刻,观察液体的颜色变为