摘要:19.图中A.B.C.D四条曲线表示ⅣA.VA.ⅥA.ⅦA族元素的气态氢化物 的沸点变化曲线.其中A.D分别表示 . 族元素气态氢化物的沸点变化,同一族中第3.4.5周期元素的气态氢化物沸点依次升高.其原因 ,图中第2周期有三种元素的气态氢化物沸点显著高于相应的同族第3周期元素气态氢化物的沸点.其原因是 . (2)已知氨分子内键与键的夹角约为107°18′.从反应NH3+H+→NH可知:NH中有一根键比较特殊.其结构如下图a所示.但是.虽然有一根键形成过程与众不同.而其结果是完全相同的.都是N.H原子间共用一对电子.键与键的夹角均为109°28′.故NH的结构如图b所示. ① 还有一些你熟悉的分子或离子中.也存在上述特殊共价键.如: 等. (在下列微粒中选择填空:[Ag(NH3)2]+.PCl5.Fe(SCN)3.NH3·H2O.H3O+) ②写出H3O+的电子式: .1919年.Langmuir提出等电子原理:原子数相同.电子总数相同的分子.互称为等电子体.等电子体的结构相似.物理性质相近.据此.你认为H3O+中键与键的夹角与下列哪个角度最接近? . A.120° B.109°28′ C.107°18′ D.60°
网址:http://m.1010jiajiao.com/timu3_id_403406[举报]
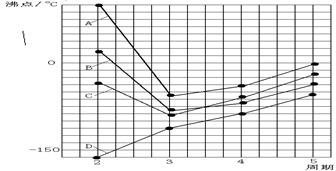
图中A、B、C、D四条曲线表示ⅣA、VA、ⅥA、ⅦA族元素的气态氢化物的沸点变化曲线,其中A、D分别表示________、________族元素气态氢化物的沸点变化;同一族中第3、4、5周期元素的气态氢化物沸点依次升高,其原因________;图中第2周期有三种元素的气态氢化物沸点显著高于相应的同族第3周期元素气态氢化物的沸点,其原因是________.