摘要:26.氮是地球上极为丰富的元素. (1)Li3N晶体中氮以N3-存在.基态N3-的电子排布式为 . (2)N≡N的键能为942 kJ·mol-1.N-N单键的键能为247 kJ·mol-3.计算说明N2中的 键比 键稳定(填“ “ ). (3)(CH3)3NH+和AlCl-4可形成离子液体.离子液体由阴.阳离子组成.熔点低于100℃.其挥发性一般比有机溶剂 (填“大 或“小 ).可用作 (填代号). a.助燃剂 b.“绿色 溶剂 c.复合材料 d.绝热材料 (4)X*中所有电子正好充满K.L.M三个电子层.它与N3-形成 的晶体结构如图所示.X的元素符号是 .与同一个 N3-相连的X*有 个.
网址:http://m.1010jiajiao.com/timu3_id_401707[举报]
氮是地球上极为丰富的元素.填写下列空白.
(1)常温下,锂可与氮气直接反应生成Li3N,Li3N晶体中氮以N3-存在,基态N3-的电子排布式为: ,Li3N晶体属于 晶体(填晶体类型).
(2)CO与N2相似,分子中都存在一个共价叁键,CO含 个π键.
(3)根据下表数据,写出氮气与氢气反应生成氨气的热化学方程式. .
(4)氮化硅是一种高温陶瓷材料,它硬度大、熔点高、化学性质稳定.
①氮化硅晶体属于 晶体(填晶体类型);
②已知氮化硅晶体结构中,原子间都以共价键相连,且N原子与N原子,Si原子与Si原子不直接相连,同时每个原子都满足8电子结构,请写出氮化硅的化学式: .
(5)极纯的氮气可由叠氮化钠(NaN3)加热分解而得到.2NaN3(s)=2Na(l)+3N2(g),反应过程中,断裂的化学键是离子键和共价键,形成的化学键有 .
查看习题详情和答案>>
(1)常温下,锂可与氮气直接反应生成Li3N,Li3N晶体中氮以N3-存在,基态N3-的电子排布式为:
(2)CO与N2相似,分子中都存在一个共价叁键,CO含
(3)根据下表数据,写出氮气与氢气反应生成氨气的热化学方程式.
| 化学键 | N-N | N=N | N≡N | N-H | H-H |
| 键能/kJ?mol-1 | 159 | 418 | 946 | 391 | 436 |
①氮化硅晶体属于
②已知氮化硅晶体结构中,原子间都以共价键相连,且N原子与N原子,Si原子与Si原子不直接相连,同时每个原子都满足8电子结构,请写出氮化硅的化学式:
(5)极纯的氮气可由叠氮化钠(NaN3)加热分解而得到.2NaN3(s)=2Na(l)+3N2(g),反应过程中,断裂的化学键是离子键和共价键,形成的化学键有
氮是地球上极为丰富的元素.
(1)Li3N晶体中氮以N3-存在,基态N3-电子排布式为:
(2)N≡N键能为942kJ/mol,N-N单键键能为247kJ/mol.计算说明N2中的
(3)已知Pt(NH3)2Cl2分子是平面结构.请画出Pt(NH3)2Cl2可能的平面结构简式: 、
、
 、
、 .
.
(4)下列分子中若为手性分子,请用*标出手性碳原子.

查看习题详情和答案>>
(1)Li3N晶体中氮以N3-存在,基态N3-电子排布式为:
1S22S22P6
1S22S22P6
(2)N≡N键能为942kJ/mol,N-N单键键能为247kJ/mol.计算说明N2中的
π
π
键比σ
σ
键稳定(填σ和π)(3)已知Pt(NH3)2Cl2分子是平面结构.请画出Pt(NH3)2Cl2可能的平面结构简式:
 、
、
 、
、
(4)下列分子中若为手性分子,请用*标出手性碳原子.

氮是地球上极为丰富的元素
(1)Li3N晶体中氮以N3-的形式存在,基态N3-的电子排布式为
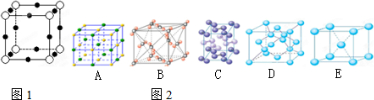
(2)X离子中所有电子正好充满K.L.M三个电子层,它与N3-形成的晶体结构如图1所示.X的元素符号是
(3)水 是生命之源,它与我们的生活密切相关.在化学实验和科学研究中,水也是一种常用的试剂.下列是钠、碘、金刚石、干冰、氯化钠晶体的晶胞图(为按顺序排序).与冰的晶体类型相同的是
(4)在冰晶体中,每个水分子与相邻的4个水分子形成氢键,已知冰的升华热是51kJ/mol,除分子间还存在范德华力(11kJ/mol)则冰晶体中氢键的“键能”是
查看习题详情和答案>>
(1)Li3N晶体中氮以N3-的形式存在,基态N3-的电子排布式为
1S22S22P6
1S22S22P6
;(2)X离子中所有电子正好充满K.L.M三个电子层,它与N3-形成的晶体结构如图1所示.X的元素符号是
Cu
Cu
,X离子与N3-形成的化合物化学式为Cu3N
Cu3N
.(3)水 是生命之源,它与我们的生活密切相关.在化学实验和科学研究中,水也是一种常用的试剂.下列是钠、碘、金刚石、干冰、氯化钠晶体的晶胞图(为按顺序排序).与冰的晶体类型相同的是
BC
BC
(请用相应的编号填写)(4)在冰晶体中,每个水分子与相邻的4个水分子形成氢键,已知冰的升华热是51kJ/mol,除分子间还存在范德华力(11kJ/mol)则冰晶体中氢键的“键能”是
20
20
kJ/mol
氮是地球上极为丰富的元素.
(1)Li3N晶体中氮以N3-存在,基态N3-的电子排布式为
(2)N≡N的键能为942kJ?mol-1,N-N单键的键能为247kJ?mol-1,通过计算说明N2中的
(3)X+中所有电子正好充满K、L、M三个电子层,X的元素符号是
查看习题详情和答案>>
(1)Li3N晶体中氮以N3-存在,基态N3-的电子排布式为
1S22S22P6
1S22S22P6
.(2)N≡N的键能为942kJ?mol-1,N-N单键的键能为247kJ?mol-1,通过计算说明N2中的
π
π
键比σ
σ
键稳定(填“?”“π”).(3)X+中所有电子正好充满K、L、M三个电子层,X的元素符号是
Cu
Cu
,它与N3-形成的晶体化学式是Cu3N
Cu3N
.(2008?山东)氮是地球上极为丰富的元素.
(1)Li3N晶体中氮以N3-存在,基态N3-的电子排布式为
(2)N≡N的键能为942kJ?mol-1,N-N单键的键能为247kJ?mol-1,计算说明N2中的
(3)(CH3)3NH+和AlCl4-可形成离子液体.离子液体由阴阳离子组成,熔点低于100℃,其挥发性一般比有机溶剂
a.助燃剂 b.“绿色”溶剂 c.复合材料 d.绝热材料
(4)X+中所有电子正好充满K、L、M三个电子层,它与N3-形成的晶体结构如图所示.X的元素符号是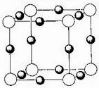
查看习题详情和答案>>
(1)Li3N晶体中氮以N3-存在,基态N3-的电子排布式为
1S22S22P6
1S22S22P6
.(2)N≡N的键能为942kJ?mol-1,N-N单键的键能为247kJ?mol-1,计算说明N2中的
π
π
键比σ
σ
键稳定.(填“σ”或“π”)(3)(CH3)3NH+和AlCl4-可形成离子液体.离子液体由阴阳离子组成,熔点低于100℃,其挥发性一般比有机溶剂
小
小
(填“大”或“小”),可用作b
b
(填代号).a.助燃剂 b.“绿色”溶剂 c.复合材料 d.绝热材料
(4)X+中所有电子正好充满K、L、M三个电子层,它与N3-形成的晶体结构如图所示.X的元素符号是
Cu
Cu
,与同一个N3-相连的X+有6
6
个.