摘要:硝酸铵(化学式为NH4NO3)化肥是农业生产中常见的速效氮肥.当硝酸铵与熟石灰混合可发生2NH4NO3 +Ca(OH)2Ca(NO3)2 + 2NH3↑+2H2O反应.若准确称取某硝酸铵样品8.5 g.与足量的熟石灰混合充分反应后.最多生成1.7g氨气(NH3).确定该样品中硝酸铵的纯度.
网址:http://m.1010jiajiao.com/timu3_id_3998019[举报]
(15分)硝酸铵在现代农业生产和国防中都占有重要地位,下图是云南天然气化工厂合成硝酸铵的简要生产工艺流程: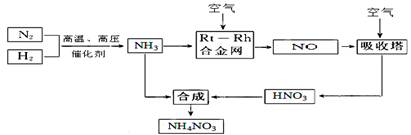
回答下列问题:
(1)N2的电子式 ,合成氨的反应中,若生成1g氨放出热量a KJ,写出该反应的热化学方程式 。
(2)氨催化氧化的化学方程式是 ,
试从化学反应速率和化学平衡原理分析温度、压强对合成氨反应的影响 。
(3)若输送NH3的管道某处发生泄漏,检测的简单方法 。
(4)农业生产上长期、过量使用化肥硝酸铵,会加重土壤酸化,原因是(用离子方程式回答) 。
(5)25℃时,将x mol NH4NO3溶于一定量水中,向该溶液中滴加y L氨水后溶液呈中性,则滴加氨水过程中水的电离平衡将 (填“正向” “不”或“逆向”)移动,所滴加氨水的物质的量浓度为 (25℃时,Kb(NH3·H2O)="2.0" × 10-5 mol·L-1)。