摘要:碳酸盐的检验:用稀盐酸和澄清石灰水.反应产生使石灰水变浑浊的CO2气体. CaCO3+ 2HCI ====CaCI2 + H2O + CO2 Na2CO3 +2 HCI==== 2NaCI + H2O + CO2
网址:http://m.1010jiajiao.com/timu3_id_3985680[举报]
碳酸钙可用于预防和治疗钙缺乏症.某实验小组同学要测定一种钙片中碳酸钙的含量.
查阅资料:获得的资料有:
(1)补钙剂中常加入糖类、维生素D等改善口感或增强药效.这些物质不与稀盐酸反应产生气体,高温灼烧时会燃烧或分解.
(2)碳酸钙高温灼烧分解生成氧化钙和二氧化碳.
(3)常见的碳酸钙含量测定方法:将碳酸钙粉碎,加入已知浓度的过量盐酸充分反应,然后测剩余盐酸的量,根据消耗盐酸的量最终求得碳酸钙的含量.
 (4)澄清石灰水中的Ca(OH)2含量很少,100g澄清石灰水中最多含0.15g Ca(OH)2.
(4)澄清石灰水中的Ca(OH)2含量很少,100g澄清石灰水中最多含0.15g Ca(OH)2.
方案设计和实施:根据资料和已学知识,该小组同学设计如下两种方案进行测定.
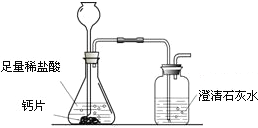
方案1:根据下图所示装置实验.
(1)锥形瓶中发生反应的化学方程式为 .
(2)长颈漏斗下部插入液面下的目的是 .
(3)加入药品前,检验该装置气密性的方法是 .
(4)记录数据如下:
方案2:将钙片粉碎,加入足量的稀盐酸充分反应,根据放出气体的量计算碳酸钙的含量.记录数据如下(空烧杯质量为100g,加入钙片质量为25g):
分析和评价:
(1)方案1和方案2中合理的是 ,原因是 .
(2)该小组同学没有使用碳酸钙高温灼烧分解的方法(实验室可以进行该实验),原因是 .
(3)要使用查阅资料(3)中介绍的方法,还需要学习的是 .
结论:经过计算,该钙片中碳酸钙的质量分数是 .
查看习题详情和答案>>
查阅资料:获得的资料有:
(1)补钙剂中常加入糖类、维生素D等改善口感或增强药效.这些物质不与稀盐酸反应产生气体,高温灼烧时会燃烧或分解.
(2)碳酸钙高温灼烧分解生成氧化钙和二氧化碳.
(3)常见的碳酸钙含量测定方法:将碳酸钙粉碎,加入已知浓度的过量盐酸充分反应,然后测剩余盐酸的量,根据消耗盐酸的量最终求得碳酸钙的含量.
 (4)澄清石灰水中的Ca(OH)2含量很少,100g澄清石灰水中最多含0.15g Ca(OH)2.
(4)澄清石灰水中的Ca(OH)2含量很少,100g澄清石灰水中最多含0.15g Ca(OH)2.方案设计和实施:根据资料和已学知识,该小组同学设计如下两种方案进行测定.
方案1:根据下图所示装置实验.
(1)锥形瓶中发生反应的化学方程式为
(2)长颈漏斗下部插入液面下的目的是
(3)加入药品前,检验该装置气密性的方法是
(4)记录数据如下:
| 钙片质量 | 空洗气瓶质量 | 澄清石灰水的质量 | 反应后洗气瓶及瓶内物质总质量 |
| 25g | 100g | 200g | 300.4g |
| 加入稀盐酸的质量 | 100g | 200g | 300g | 400g |
| 充分反应后烧杯及杯内物质总质量 | 222.8g | 320.6g | 418.4g | 518.4g |
(1)方案1和方案2中合理的是
(2)该小组同学没有使用碳酸钙高温灼烧分解的方法(实验室可以进行该实验),原因是
(3)要使用查阅资料(3)中介绍的方法,还需要学习的是
结论:经过计算,该钙片中碳酸钙的质量分数是
 实验室用盐酸和碳酸钙固体反应,将得到的气体X通入澄清石灰水中,始终没有发现石灰水变浑浊.为此,同学们进行了探究.
实验室用盐酸和碳酸钙固体反应,将得到的气体X通入澄清石灰水中,始终没有发现石灰水变浑浊.为此,同学们进行了探究.[提出猜想]甲同学认为:澄清石灰水已变质; 乙同学认为:气体X中不只含有CO2;
[实验方案]
(1)甲的探究:①取稀硫酸与碳酸钠反应制取CO2;反应的方程式为
Na2CO3+H2SO4=Na2SO4+H2O+CO2↑
Na2CO3+H2SO4=Na2SO4+H2O+CO2↑
,将生成的气体通入澄清石灰水.现象为
澄清的石灰水变浑浊
澄清的石灰水变浑浊
.实验结论:澄清石灰水没有变质.
(2)乙的探究:用盐酸和碳酸钙固体反应,将得到的气体X通入硝酸银溶液.
实验现象
有白色沉淀生成
有白色沉淀生成
;实验结论:气体X中还有
HCl
HCl
气体.根据实验结论,用化学方程式表示石灰水未变浑浊的原因CaCO3+2HCl=CaCl2+CO2↑+H2O;Ca(OH)2+2HCl=CaCl2+2H2O
CaCO3+2HCl=CaCl2+CO2↑+H2O;Ca(OH)2+2HCl=CaCl2+2H2O
.[分析与讨论]
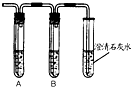
(3)在讨论中,丙同学提出:只用图25实验装置就可以同时完成上述两个假设的探究.则A、B试管中的试剂依次是下列选项中的
②
②
.①浓硫酸、硝酸银溶液
②饱和碳酸氢钠溶液、硝酸银溶液
③硝酸银溶液、石蕊溶液
④氢氧化钠溶液、硝酸银溶液
(4)B试管中试剂的作用是
检验HCl是否除尽
检验HCl是否除尽
.A为碳酸钠,C为相对分子质量为100白色不溶物,请填空:
(1)B常做食品干燥剂,理由(写化学方程式)
(2)D中一定含有的溶质是
a、酚酞溶液 b、稀盐酸 c、澄清石灰水 d、pH试纸
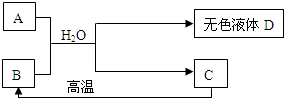
(3)写出A、B和水三种物质的总反应的化学方程式
查看习题详情和答案>>
(1)B常做食品干燥剂,理由(写化学方程式)
CaO+H2O=Ca(OH)2
CaO+H2O=Ca(OH)2
(2)D中一定含有的溶质是
氢氧化钠(或NaOH)
氢氧化钠(或NaOH)
,检验D中是否含有A,可选用的试剂为bc
bc
(填下列序号)a、酚酞溶液 b、稀盐酸 c、澄清石灰水 d、pH试纸

(3)写出A、B和水三种物质的总反应的化学方程式
Na2CO3+CaO+H2O=CaCO3↓+2NaOH
Na2CO3+CaO+H2O=CaCO3↓+2NaOH
(已知 Na2CO3+Ca(OH)2=CaCO3↓+2NaOH)实验室常用稀盐酸和石灰石反应制取二氧化碳.
(1)该反应的符号表达式为
(2)甲图表示加入药品前的一个操作,其目的是

(3)检验生成的气体是二氧化碳的方法是
(4)实验室通常不选用稀硫酸和石灰石反应制取二氧化碳,因生成的微溶物硫酸钙会阻碍反应的进一步进行.某小组经研究,用乙图所示方法成功制得了大量C02(反应物为稀硫酸和石灰石).
①该方法中加热仪器名称是
②推测:在硫酸溶液中加入氯化铵和对溶液加热,目的都是
③思考乙图方法,你认为相比用稀盐酸和石灰石反应,其改进的出发点是
查看习题详情和答案>>
(1)该反应的符号表达式为
CaCO3+HCl→CaCl2+H2O+CO2
CaCO3+HCl→CaCl2+H2O+CO2
.(2)甲图表示加入药品前的一个操作,其目的是
检查装置的气密性
检查装置的气密性
.
(3)检验生成的气体是二氧化碳的方法是
把气体通入澄清的石灰水中,石灰水变浑浊,就证明是二氧化碳
把气体通入澄清的石灰水中,石灰水变浑浊,就证明是二氧化碳
.(4)实验室通常不选用稀硫酸和石灰石反应制取二氧化碳,因生成的微溶物硫酸钙会阻碍反应的进一步进行.某小组经研究,用乙图所示方法成功制得了大量C02(反应物为稀硫酸和石灰石).
①该方法中加热仪器名称是
酒精灯
酒精灯
;②推测:在硫酸溶液中加入氯化铵和对溶液加热,目的都是
增大硫酸钙在溶液中的溶解能力
增大硫酸钙在溶液中的溶解能力
;③思考乙图方法,你认为相比用稀盐酸和石灰石反应,其改进的出发点是
原物质中的盐酸具有挥发性,会进入二氧化碳气体中
原物质中的盐酸具有挥发性,会进入二氧化碳气体中
;对比两种方法,你认为要进行实验改进,关键是干扰实验,所以要进行改进
干扰实验,所以要进行改进
.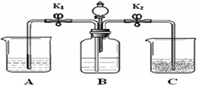 实验室用下图装置进行碳酸钠的性质实验,烧杯A中是澄清石灰水并滴加了酚酞,C中是石灰乳.实验开始前,称取10.6g纯碱置于B中,关闭开关K1打开K2,并加入一定量的稀硫酸.
实验室用下图装置进行碳酸钠的性质实验,烧杯A中是澄清石灰水并滴加了酚酞,C中是石灰乳.实验开始前,称取10.6g纯碱置于B中,关闭开关K1打开K2,并加入一定量的稀硫酸.①烧杯C中并没有明显现象,为了证明B中的确产生了CO2,现将C中悬浊液进行固液分离,过滤后滤液能使酚酞试液变红,则滤液中的主要溶质是
氢氧化钙
氢氧化钙
,该现象不能
不能
(填写“能”或“不能”)说明产生了CO2.②上述过滤后的滤渣可能存在Ca(OH)2和CaCO3.某同学为证明该两种物质同时存在,在一支试管中取少量样品,经过两个步骤完成了检验.若所有检验实验均在该支试管中进行,请完成实验报告:
| 实验步骤 | 所用的试剂或检验方法 | 结 论 |
| 步骤一 | 取样滴加酚酞试液,溶液变红 取样滴加酚酞试液,溶液变红 |
证明 含Ca(OH)2存在 |
| 步骤二 | 继续滴加盐酸,有气泡产生 继续滴加盐酸,有气泡产生 |
证明 CaCO3 CaCO3 存在 |
| 预测的反应现象 | B中反应后,溶液中溶质的化学式 | 烧杯A中发生的主要反应的化学方程式 |
| A中溶液产生大量的白色沉淀产生,红色不褪去. | Na2CO3、Na2SO4 Na2CO3、Na2SO4 |
Na2CO3+Ca(OH)2=CaCO3↓+2NaOH Na2CO3+Ca(OH)2=CaCO3↓+2NaOH |