摘要:19.amLA.B.C三种气态烃的混合物跟足量的氧气混合点燃后.恢复到原常温常压状态.气体体积缩小了2amL.那么A.B.C三种烃可能是: ( ) A.CH4.C2H6.C3H8 B.C2H4.C2H2.CH4 C.CH4.C2H4.C3H4 D.C2H6.C3H6.C4H6
网址:http://m.1010jiajiao.com/timu3_id_396920[举报]
有A、B、C、D、E五种元素,其中A、B、C属于同一周期,A原子最外层p能级的电子数等于次外层的电子总数,B原子最外层中有两个未成对的电子,D、E原子核内各自的质子数与中子数相等,B元素可分别与A、C、D、E生成RB2型化合物,并已知在DB2和EB2中,D与B的质量比为7:8,E与B的质量比为1:1.根据以上条件,回答下列问题:
(1)推断五种元素符号分别是:A
(2)写出D原子的电子排布式
(3)指出E元素在元素周期表中的位置
(4)比较A、B、C三种元素的第一电离能的大小顺序
查看习题详情和答案>>
(1)推断五种元素符号分别是:A
C
C
,BO
O
,CN
N
,DSi
Si
,ES
S
.(2)写出D原子的电子排布式
1s22s22p63s23p2
1s22s22p63s23p2
.(3)指出E元素在元素周期表中的位置
第三周期第ⅥA族
第三周期第ⅥA族
.(4)比较A、B、C三种元素的第一电离能的大小顺序
N>O>C
N>O>C
(由大到小的顺序排列).(2011?烟台模拟)【化学--物质结构与性质】
微粒A、B、C为分子,D和F为阳离子,E为阴离子,它们都含有10个电子;B溶于A后所得的物质可电离出D和E;C是重要的化石能源.将A、B和含F离子的物质混合后可得D和一种白色沉淀.G3+离子与Ar原子的电子层结构相同.请回答:
(1)基态G原子的外围电子排布式是
(2)根据等电子体原理,D离子的空间构型是
(3)构成C的中心原子可以形成多种单质,其中有一种为空间网状结构,右图立方体中心的“ ”表示该晶体中的一个原子,请在该立方体的顶点上用“
”表示该晶体中的一个原子,请在该立方体的顶点上用“ ”表示出与之紧邻的原子.
”表示出与之紧邻的原子.
(4)光谱证实F与烧碱溶液反应有Na[F(OH)4]生成,则Na[F(OH)4]中不存在
a.金属键 b.离子键 c.非极性键 d.极性键 f.配位键 g.σ键 h.π键.
查看习题详情和答案>>
微粒A、B、C为分子,D和F为阳离子,E为阴离子,它们都含有10个电子;B溶于A后所得的物质可电离出D和E;C是重要的化石能源.将A、B和含F离子的物质混合后可得D和一种白色沉淀.G3+离子与Ar原子的电子层结构相同.请回答:
(1)基态G原子的外围电子排布式是
3d14s2
3d14s2
.在A、B、C三种分子中,属于非极性分子的有CH4
CH4
(写化学式).(2)根据等电子体原理,D离子的空间构型是
正四面体
正四面体
,其中心原子轨道的杂化类型是sp3
sp3
.(3)构成C的中心原子可以形成多种单质,其中有一种为空间网状结构,右图立方体中心的“
 ”表示该晶体中的一个原子,请在该立方体的顶点上用“
”表示该晶体中的一个原子,请在该立方体的顶点上用“ ”表示出与之紧邻的原子.
”表示出与之紧邻的原子.
(4)光谱证实F与烧碱溶液反应有Na[F(OH)4]生成,则Na[F(OH)4]中不存在
ach
ach
(填字母).a.金属键 b.离子键 c.非极性键 d.极性键 f.配位键 g.σ键 h.π键.
现有A、B、C、D、E五种短周期主族元素,且从A到E原子序数依次增大,已知A和C元素的原子最外层电子数相同,C、D、E元素的原子电子层数相同,A元素的原子核中只有质子、无中子,B元素的原子核外最外层电子数是电子层数的3倍,D元素的原子核外电子数比C元素的原子核外电子数多2个,E元素的原子半径在同周期中是最小的(稀有气体元素除外).请回答下列问题:
(1)D元素的名称是 ,E离子的原子结构示意图为 ;
(2)用电子式表示化合物CE的形成过程 ;
(3)A、B两元素形成的化合物A2B2的结构式是 ;
(4)将D元素所形成的单质与Mg用导线连接插入有A、B、C三种元素所形成的化合物的水溶液中构成原电池,则该原电池的正极为 (填元素符号),该原电池总反应的离子方程式为: .
查看习题详情和答案>>
(1)D元素的名称是
(2)用电子式表示化合物CE的形成过程
(3)A、B两元素形成的化合物A2B2的结构式是
(4)将D元素所形成的单质与Mg用导线连接插入有A、B、C三种元素所形成的化合物的水溶液中构成原电池,则该原电池的正极为
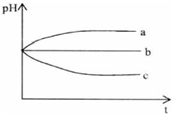 (2012?上饶一模)将pH相同的三种酸性溶液露置于空气中一段时间后,溶液的pH随时间的变化情况如图所示:则a、b、c三种溶液分别可能为( )
(2012?上饶一模)将pH相同的三种酸性溶液露置于空气中一段时间后,溶液的pH随时间的变化情况如图所示:则a、b、c三种溶液分别可能为( )