摘要:氧化铜是一种黑色固体.可溶于稀硫酸.某同学想知道是稀硫酸的哪种粒子(H2O.H+.SO42-)能使氧化铜溶解.请你和他一起通过如图Ⅰ.Ⅱ和Ⅲ三个实验完成这次探究活动. (1)某同学提出的假设是 , (2)通过实验Ⅰ可以证明 , (3)要证明另外两种粒子能否溶解氧化铜.还需要进行实验Ⅱ和Ⅲ.在Ⅱ中加入稀硫酸后氧化铜溶解.则进一步所做的确认为:在Ⅲ中先加入 .再加入 . (4)探究结果为 . (5)你认为除实验Ⅱ和Ⅲ所用的试剂外.还能溶解氧化铜的一种常见物质是 . 族 周期 ⅦB 4 25Mn锰 5 43Te锝 6 75Re铼
网址:http://m.1010jiajiao.com/timu3_id_395373[举报]
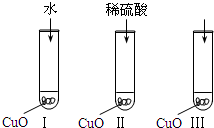 (2007?汕头二模)氧化铜是一种黑色固体,可溶于稀硫酸.某同学想知道是稀硫酸的哪种粒子(H2O,H+,SO42-)能使氧化铜溶解.请你和他一起通过如图Ⅰ、Ⅱ和Ⅲ三个实验完成这次探究活动.
(2007?汕头二模)氧化铜是一种黑色固体,可溶于稀硫酸.某同学想知道是稀硫酸的哪种粒子(H2O,H+,SO42-)能使氧化铜溶解.请你和他一起通过如图Ⅰ、Ⅱ和Ⅲ三个实验完成这次探究活动.(1)提出假设:假设 l:H2O能使氧化铜溶解
假设 2:
H+能够使CuO溶解
H+能够使CuO溶解
假设 3:SO42-能使氧化铜溶解
(2)通过实验Ⅰ可以证明假设
1
1
(填1、2、3)不成立;(3)要证明另外两种粒子能否溶解氧化铜,还需要进行实验Ⅱ和Ⅲ,在Ⅱ中加入稀硫酸后氧化铜溶解,则进一步所做的实验操作是:在Ⅲ中先加入
Na2SO4(或K2SO4等)
Na2SO4(或K2SO4等)
,再加入稀硫酸
稀硫酸
.(4)探究结果为
氧化铜固体溶于稀H2SO4是稀硫酸H+在起作用,而H2O、SO42-两种粒子都不能使CuO溶解
氧化铜固体溶于稀H2SO4是稀硫酸H+在起作用,而H2O、SO42-两种粒子都不能使CuO溶解
.你认为除实验Ⅱ和Ⅲ所用的试剂外,还能溶解氧化铜的一种常见物质是硝酸或盐酸等
硝酸或盐酸等
.硫酸铜晶体在不同温度下可失去部分或全部结晶水甚至分解成氧化物。某学生在不同温度下给8.000 g硫酸铜晶体加热(温度逐渐升高),实验结果记录如下:
| 实验次序 | 温度(℃) | 冷却后剩余固体的质量(g) |
| 1 | 102 | 6.848 |
| 2 | 113 | 5.696 |
| 3 | 258 | 5.120 |
| 4 | 570 | 2.560 |
(1)第1次实验后,试样晶体失去结晶水的质量是_____ g。
(2)通过计算确定第二次实验后固体物质的化学式为______________。
(3)第四次实验后,剩余固体为一种黑色粉末(假设为纯净物),将该黑色粉末溶解于稀硫酸中,至少需要0.50mol/L的稀硫酸多少毫升?(写出计算过程) 查看习题详情和答案>>
硫酸铜晶体在不同温度下可失去部分或全部结晶水甚至分解成氧化物。某学生在不同温度下给8.000 g硫酸铜晶体加热(温度逐渐升高),实验结果记录如下:
(1)第1次实验后,试样晶体失去结晶水的质量是_____ g。
(2)通过计算确定第二次实验后固体物质的化学式为______________。
(3)第四次实验后,剩余固体为一种黑色粉末(假设为纯净物),将该黑色粉末溶解于稀硫酸中,至少需要0.50mol/L的稀硫酸多少毫升?(写出计算过程)
| 实验次序 | 温度(℃) | 冷却后剩余固体的质量(g) |
| 1 | 102 | 6.848 |
| 2 | 113 | 5.696 |
| 3 | 258 | 5.120 |
| 4 | 570 | 2.560 |
(1)第1次实验后,试样晶体失去结晶水的质量是_____ g。
(2)通过计算确定第二次实验后固体物质的化学式为______________。
(3)第四次实验后,剩余固体为一种黑色粉末(假设为纯净物),将该黑色粉末溶解于稀硫酸中,至少需要0.50mol/L的稀硫酸多少毫升?(写出计算过程)
硫酸铜晶体在不同温度下可失去部分或全部结晶水甚至分解成氧化物。某学生在不同温度下给8.000 g硫酸铜晶体加热(温度逐渐升高),实验结果记录如下:
|
实验次序 |
温度(℃) |
冷却后剩余固体的质量(g) |
|
1 |
102 |
6.848 |
|
2 |
113 |
5.696 |
|
3 |
258 |
5.120 |
|
4 |
570 |
2.560 |
(1)第1次实验后,试样晶体失去结晶水的质量是_____ g。
(2)通过计算确定第二次实验后固体物质的化学式为______________。
(3)第四次实验后,剩余固体为一种黑色粉末(假设为纯净物),将该黑色粉末溶解于稀硫酸中,至少需要0.50mol/L的稀硫酸多少毫升?(写出计算过程)
查看习题详情和答案>>