网址:http://m.1010jiajiao.com/timu3_id_394916[举报]
| 容器 | 起始时各物质的量 | 到达平衡时放出的热量(QkJ) | 平衡时SO2转化率 (X) | |||
| SO2(mol) | O2(mol) | SO3(mol) | N2 | |||
| 甲 | 2 | 1 | 0 | 0 | Q1 | X1 |
| 乙 | 1 | 0.5 | 0 | 0 | Q2=39.4 | X2 |
| 丙 | 1 | 0.5 | 0 | 1 | Q3 | X3 |
| 丁 | 1.8 | 0.9 | 0.2 | 0 | Q4 | X4 |
a、2Q3=2Q2<Q1<197kJ b、2X3=2X2<X1<100%
c、Q1>Q4 且 X1>X4 d、SO3的质量m:m甲=m丁>2m乙
e、容器内压强p:p甲=p丁>2p乙 f、c(SO2)与c(O2)之比k:k甲=k丙>k乙
h、若乙的体积为2L,则到达平衡时放出的热量小于39.4kJ
(2)某时刻甲容器内反应达到平衡,保持恒温恒容;
①假设又向容器内加入一定量的SO2气体,则X(SO2)
②假设又向容器中加入一定量的SO3(g),X(SO2)
(3)平衡时,乙容器中SO2的体积分数为
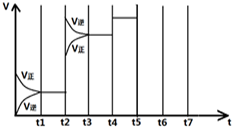
(4)如图表示某一时间段中该反应反应速率与反应过程的关系(t2、t4、t5)时刻改变的条件都只有一个).

①t2时改变的条件是
②若t5时降低压强,试画出t-v图象
③若各阶段对应的平衡常数如图所示
| t1-t2 | t3-t4 | t4-t5 | t6-t7 |
| K1 | K2 | K3 | K4 |
 在一定条件下发生化学反应:2SO2(g)+O2(g)?2SO3(g)△H=-197kJ/mol.现有容积均为1L的甲、乙两个容器,在上述条件下分别充入气体,到达平衡时,反应放出的热(Q),及平衡时的转化率(X)如下表所示:
在一定条件下发生化学反应:2SO2(g)+O2(g)?2SO3(g)△H=-197kJ/mol.现有容积均为1L的甲、乙两个容器,在上述条件下分别充入气体,到达平衡时,反应放出的热(Q),及平衡时的转化率(X)如下表所示:| 容器 | 起始时各物质的量 | 到达平衡时放出的热量(QkJ) | 平衡时SO2转化率 (X) | |||
| SO2 | O2 | SO3 | N2 | |||
| 甲 | 2 | 1 | 0 | 0 | Q1 | X1 |
| 乙 | 1 | 0.5 | 0 | 1 | Q2= 39.4 |
X2 |
a、Q2<Q1<197kJ b、X2<X1<100% c、Q1=78.8 d、X1=2X2
(2)某时刻甲容器内反应达到平衡,保持恒温恒容;
①假设又向容器内加入一定量的SO2气体,则X(SO2)
②假设又向容器中加入一定量的SO3(g),X(SO2)
(3)平衡时,乙容器中SO2的体积分数为
(4)如图表示某一时间段中该反应反应速率与反应过程的关系(t2、t4、t5)时刻改变的条件都只有一个).
①t2时改变的条件是
②若t 5时降低压强,试画出v-t图象③若各阶段对应的平衡常数如图所示
| t 1-t 2 | t 3-t 4 | t 4-t 5 | t 6-t 7 |
| K1 | K2 | K3 | K4 |
(1)Al13代表的含义是____________。
A.铝是13号元素 B.铝原子有13个电子
C.铝原子有13个质子 D.由13个铝原子组成的新物质
(2)科学家预言“超级原子”的发现将会重建周期表,因为Al13、Al14的性质很像现行元素周期表中的某主族元素。已知当这类“超级原子”具有40个价电子时最稳定(铝原子具有3个价电子),类似于稀有气体的最外层8个电子的稳定性。
①铝在元素周期表中的位置:第______________周期第______________族,其原子结构示意图为______________。
②Al13有39个价电子,所以与______________(填主族)的元素性质类似;Al14有______________个价电子,且与______________的元素性质相似。
(3)这些“超级原子”的制备方法是:首先在实验室中将金属铝制成蒸气,在这个过程中会形成一些由多个铝原子组成的极其微小的球体,用质谱仪从铝蒸气中可以过滤出Al13“超级原子”,也就是说由13个铝原子组成的小球最稳定,这些“超级原子”能够与呈链形的碘分子发生化学反应,反应原理是Al13“超级原子”取代了碘分子中的一个碘原子的位置,其他碘原子也“悬挂”在Al13“超级原子”上。
①关于“超级原子”Al13与碘反应的产物叙述错误的是______________。
A.是一种新的碘铝化合物
B.是碘与铝的混合物
C.该物质具有碘的性质
D.该物质具有铝的性质
②“超级原子”Al13在气相中还能与HI发生化合反应,请你写出这个反应的化学方程式_____________________________________________________________________。
查看习题详情和答案>>药品:①2%NaOH溶液 ②稀HCl ③稀H2SO4 ④饱和KHCO3溶液 ⑤浓H2SO4 ⑥CaCO3块状固体 ⑦K2CO3粉末?
仪器装置(如图所示):?

若用X代表制备过程中可随开随用的气体发生装置图,Y代表除杂洗气装置,Z代表制备产品的装置。试按要求回答下列问题:?
(1)制取CO2气体的发生装置图可选用 ;但要使制备过程做到随开随用,只能选用 。(填字母编号)?
(2)除杂装置可选用 (填字母编号),装置内的试剂应选用 (填序号),除去的杂质为 (填化学式)。?
(3)将装置按X、Y、Z顺序连接并检查气密性后,当加入药品实验时,X装置中发生化学反应的离子方程式为? ? 。?
(4)常温下,向Z装置的NaOH溶液中通入过量CO2气体,其目的是 ;若要保证Z装置中不析出晶体(不考虑过饱和溶液问题),NaOH溶液最大浓度不能超过 %(质量分数)。(小数点后保留1位有效数字)
附:有关物质在常温(20 ℃)时的溶解度?
化学式 | Na2CO3 | NaHCO3 | NaOH | NaCl | Na2SO4 |
溶解度(g/100 g) | 21.3 | 9.6 | 107 | 35.8 | 19.4 |
药品:①2% NaOH溶液②稀HCl③稀H![]() SO
SO![]() ④饱和KHCO
④饱和KHCO![]() 溶液⑤浓H
溶液⑤浓H![]() SO
SO![]() ⑥CaCO
⑥CaCO![]() 固体⑦K
固体⑦K![]() CO
CO![]() 粉末
粉末
仪器装置(如图所示):
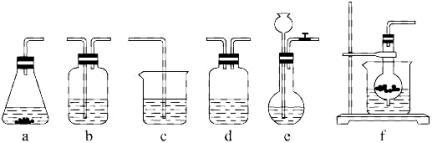
请根据题目要求完成下列问题:
请按下表要求,填写选择的装置和药品。
分项内容 | CO | 除杂洗气装置(Y) | 制备产品装置(Z) |
选择的装置 (填序号) |
|
| C |
选择的药品 (填序号) |
|
| ① |
(2)如何检验所选择的CO![]() 发生装置(X)的气密性,请写出主要操作过程:__________。
发生装置(X)的气密性,请写出主要操作过程:__________。
(3)将装置按X、Y、Z顺序连接并检查气密性后,当加入药品实验时,X装置中发生化学反应的离子方程式为_____________,Y装置中除去的杂质为_________________。
(4)常温下,向Z装置的NaOH溶液中通入过量CO2气体,其目的是______________。
(5)若要保证Z装置中不析出晶体(不考虑过饱和溶液问题),NaOH溶液最大浓度不能超过________________%(质量分数)。
附:有关物质在常温(25 ℃)时的溶解度
化学式 | Na | NaHCO | NaOH | NaCl | Na |
溶解度 (g/100 g H | 21.3 | 9.60 | 107 | 35.8 | 19.4
|