摘要:37].亚硫酸钠和碘酸钾在酸性溶液中发生以下反应: Na2SO3+ KIO3+ H2SO4→ Na2SO4+ K2SO4+ I2+ H2O (1)配平上面的氧化还原反应方程式.将系数填入方框中. (2)其中氧化剂是 .若反应中有5 mol电子转移.则生成的碘是 mol. (3)该反应的过程和机理较复杂.一般认为发生以下①-④反应: ①IO3-+SO32-=IO2-+SO42- ②IO2-+2SO32-= I-+2SO42- ③5I-+6H++ IO3-=3I2+3H2O ④I2+SO32-+H2O= 2I-+SO42-+2H+ 根据上述步骤推测该反应总的反应速率由 应应决定(填写上述四步反应的序号). (4)若预先加入淀粉溶液.由上述四步反应可以看出必须在 离子消耗完全时.才会有使淀粉变蓝的现象产生.
网址:http://m.1010jiajiao.com/timu3_id_394914[举报]
 硫代硫酸钠(Na2S2O3)可由亚硫酸钠和硫粉通过化合反应制得.已知:Na2S2O3在酸性溶液中不能稳定存在;硫代硫酸钠与碘反应的离子方程式为:2S2O32-+I2→S4O62-+2I-.
硫代硫酸钠(Na2S2O3)可由亚硫酸钠和硫粉通过化合反应制得.已知:Na2S2O3在酸性溶液中不能稳定存在;硫代硫酸钠与碘反应的离子方程式为:2S2O32-+I2→S4O62-+2I-.(Ⅰ)制备Na2S2O3?5H2O
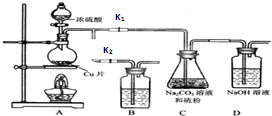
(1)打开K1,关闭K2,向放有铜片的圆底烧瓶中加入足量浓硫酸,加热.圆底烧瓶中发生反应的化学方程式是
Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O
| ||
Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O
.
| ||
(2)C中混合液被气流搅动,反应一段时间后,硫粉的量逐渐减少.C中碳酸钠的作用是
起反应物作用及提供碱性环境
起反应物作用及提供碱性环境
.“停止C中的反应”的操作是打开K2,关闭K1
打开K2,关闭K1
.(3)过滤C中的混合液.将滤液加热浓缩、冷却结晶、过滤、洗涤、烘干,得到产品.“过滤”用到的玻璃仪器是(填仪器名称)
漏斗、烧杯、玻璃棒
漏斗、烧杯、玻璃棒
.(4)装置B中盛放的试剂是(填化学式)
NaOH
NaOH
溶液,其作用是吸收多余SO2,防止污染环境
吸收多余SO2,防止污染环境
.(Ⅱ)用I2的标准溶液测定产品的纯度
取5.5g产品,配制成100mL溶液.取10.00mL溶液,以淀粉溶液为指示剂,用浓度为0.050mol/L I2的标准溶液进行滴定,相关数据记录如下表所示.
| 编号 | 1 | 2 | 3 |
| 溶液的体积/mL | 10.00 | 10.00 | 10.00 |
| 消耗I2标准溶液的体积/mL | 19.95 | 17.10 | 20.05 |
溶液变蓝,且半分钟不改变
溶液变蓝,且半分钟不改变
.(2)Na2S2O3?5H2O在产品中的质量分数是
90.2%
90.2%
(用百分数表示,且保留1位小数).(1)亚硫酸钠和碘酸钾在酸性溶液中发生以下反应:
①配平上面的氧化还原反应方程式,将化学计量数填入方框中.
②其中氧化剂是
③若反应中有5mol电子转移,则生成碘的物质的量是
(2)完成表格中的内容:
(3)勒夏特列原理:如果改变影响平衡的一个条件(如浓度、温度、压强等).平衡就向着能够
查看习题详情和答案>>
5
5
Na2SO3+2
2
KIO3+1
1
H2SO4--5
5
Na2SO4+1
1
K2SO4+1
1
I2+1
1
H2O①配平上面的氧化还原反应方程式,将化学计量数填入方框中.
②其中氧化剂是
KIO3
KIO3
.③若反应中有5mol电子转移,则生成碘的物质的量是
0.5
0.5
mol(2)完成表格中的内容:
| 改变的条件 | 平衡移动的方向 | 平衡移动的过程 |
| 增大反应物的浓度 | 正向移动 正向移动 |
反应物的浓度 减小 减小 |
| 减小压强 | 向气体体积增大方向移动 向气体体积增大方向移动 |
体系的压强逐渐 增大 增大 |
| 升高温度 | 向吸热方向移动 向吸热方向移动 |
体系的温度逐渐 降低 降低 |
| 使用合适的催化剂 | 平衡不移动 平衡不移动 |
速率 加快 加快 达平衡所需时间 缩短 缩短 |
减弱这种改变
减弱这种改变
的方向移动.(2012?闵行区二模)亚硫酸钠和碘酸钾在酸性溶液里反应的化学方程式是:
(1)配平该反应,若反应中有5mol电子转移,则生成的碘是
(2)该反应过程较复杂,一般认为分以下几步:
①IO3-+SO32-→IO2-+SO42-(反应慢)
②IO2-+2SO32-→I-+2SO42-(反应快)
③5I-+6H++IO3-→3I2+3H2O(反应快)
④I2+SO32-+H2O→2I-+SO42-+2H+(反应快)
根据上述条件推测,此反应速率由
(3)若预先加入淀粉溶液,由反应过程看,必在
(4)在酸性溶液中IO3-离子被I-离子还原生成碘,在碱性溶液中IO3-离子不被I-离子还原,而无论在酸性或碱性溶液中IO4-都被I-离子还原,IO4-与I-的碱性溶液的反应产物中加入淀粉溶液变蓝.若IO4-被还原时化合价是逐步降低的,在碱性溶液中IO4-离子与I-反应的离子方程式为
查看习题详情和答案>>
5
5
Na2SO3+2
2
KIO3+1
1
H2SO4→5
5
Na2SO4+1
1
K2SO4+1
1
I2+1
1
H2O(1)配平该反应,若反应中有5mol电子转移,则生成的碘是
127
127
g.(2)该反应过程较复杂,一般认为分以下几步:
①IO3-+SO32-→IO2-+SO42-(反应慢)
②IO2-+2SO32-→I-+2SO42-(反应快)
③5I-+6H++IO3-→3I2+3H2O(反应快)
④I2+SO32-+H2O→2I-+SO42-+2H+(反应快)
根据上述条件推测,此反应速率由
①
①
步(填序号)反应决定.(3)若预先加入淀粉溶液,由反应过程看,必在
SO32-
SO32-
离子消耗完时,才会有溶液变蓝的现象产生.原因是SO32-的还原性大于I-,可被I2氧化
SO32-的还原性大于I-,可被I2氧化
.(4)在酸性溶液中IO3-离子被I-离子还原生成碘,在碱性溶液中IO3-离子不被I-离子还原,而无论在酸性或碱性溶液中IO4-都被I-离子还原,IO4-与I-的碱性溶液的反应产物中加入淀粉溶液变蓝.若IO4-被还原时化合价是逐步降低的,在碱性溶液中IO4-离子与I-反应的离子方程式为
IO4-+2I-+H2O=IO3-+I2+2OH-
IO4-+2I-+H2O=IO3-+I2+2OH-
.亚硫酸钠和碘酸钾在酸性溶液中发生以下发应:
 .
.
(1)配平上面的方程式,在横线上填入系数,在 填上反应产物
填上反应产物
(2)其中氧化剂是
(3)该反应的过程和机理较复杂,一般认为发生以下四步反应:
①IO3-+SO32-→IO2-+SO42-(反应速率慢)
②IO2-+2SO32-→I-+2SO42-(反应速率快)
③5I-+6H++IO3-→3I2+3H2O(反应速率快)
④I2+SO32-+H2O→I-+SO42-+2H+(反应速率快)
根据上述步骤推测该反应总的反应速率由
(4)预先加入淀粉溶液,由上述四步反应可以看出必须在
查看习题详情和答案>>
5
5
Na2SO3+2
2
KIO3+1
1
H2SO45
5
Na2SO4+1
1
K2SO4+1
1
I2+1
1
 .
.(1)配平上面的方程式,在横线上填入系数,在
 填上反应产物
填上反应产物H2O
H2O
.(2)其中氧化剂是
KIO3
KIO3
,若反应中有2.5mol电子转移,则生成的碘是0.25
0.25
mol;氧化产物为1.25
1.25
mol.(3)该反应的过程和机理较复杂,一般认为发生以下四步反应:
①IO3-+SO32-→IO2-+SO42-(反应速率慢)
②IO2-+2SO32-→I-+2SO42-(反应速率快)
③5I-+6H++IO3-→3I2+3H2O(反应速率快)
④I2+SO32-+H2O→I-+SO42-+2H+(反应速率快)
根据上述步骤推测该反应总的反应速率由
①
①
(填反应编号)步反应决定.(4)预先加入淀粉溶液,由上述四步反应可以看出必须在
SO32-
SO32-
离子消耗完后,才会使淀粉变蓝的现象产生.(10分)含硫化合物的种类很多,现有SO2、Na2SO3、H2SO4、CuSO4这4种常见的含硫化合物。回答下列问题:
(1)为进一步减少SO2的污染并变废为宝,我国正在探索在一定条件下用CO还原SO2得到单质硫的方法来除去SO2 。写出该反应的化学方程式: 。
(2)亚硫酸钠和碘酸钾在酸性溶液中发生以下反应: —
— 
①配平上面的氧化还原反应方程式.将化学计量数填入方框中。
②其中氧化剂是 ,若反应中有5 mol电子转移,则生成的碘单质是 mol。
(3) 向FeCl3和BaCl2的酸性混合溶液中通入SO2气体,有白色沉淀生成。此沉淀是
| A.BaSO4 | B.FeS | C.BaSO3 | D.S |
 查看习题详情和答案>>
查看习题详情和答案>>