网址:http://m.1010jiajiao.com/timu3_id_394891[举报]

(1)研磨的作用是
(2)该工艺中可循环使用的物质是
(3)白云石轻烧的主要产物是MgO?CaCO3,而传统工艺是将白云石加热分解为MgO和CaO后提取,白云石轻烧的优点是
(4)加热反应的离子方程式为
(5)①加热反应时,在323k和353k溶液中c(NH4+)与反应时间的关系如下图所示,请在如图画出373k的曲线.

②由图可知,随着温度升高:
Q、W、X、Y、Z是5种短周期元素,原子序数逐渐增大,Q与W组成的化合物是天然气的主要成分,W与Y、X与Y组成的化合物是机动车排出的大气污染物,Y和Z能形成原子个数比为1∶1和1∶2的两种离子化合物.
(1)W在元素周期表中的位置是________周期________族.
(2)工业合成XQ3是放热反应.下列措施中,既能加快反应速率,又能提高原料利用率是________.(填写序号)
A.升高温度
B.加入催化剂
C.将XQ3及时分离出去
D.增大反应体系的压强
(3)2.24 L(标准状况)XQ3被200 mL 1 mol/L QXY3溶液吸收后,所得溶液中离子浓度从大到小的顺序是________.(用离子符号表示)
(4)WQ4Y与Y2的反应可将化学能转化为电能,其工作原理如图所示,a极的电极反应是________.

(5)已知:W(s)+Y2(g)=WY2(g);△H=-393.5 kJ/mol
WY(g)+![]() Y2(g)=WY2(g);△H=-238.0 kJ/mol.则24 gW与一定量的Y2反应,放出热量362.5 kJ,所得产物成分及物质的量之比为________.
Y2(g)=WY2(g);△H=-238.0 kJ/mol.则24 gW与一定量的Y2反应,放出热量362.5 kJ,所得产物成分及物质的量之比为________.
(6)X和Z组成的一种离子化合物,能与水反应生成两种碱,该反应的化学方程式为________.
| |||||||||||||||||||||||||||||||||||||
金属钨用途广泛,主要用于制造硬质或耐高温的合金,以及灯泡的灯丝。高温下,在密闭容器中用H2还原WO3可得到金属钨,其总反应为:
WO3 (s) + 3H2 (g)  W
(s) + 3H2O (g) 请回答下列问题:
W
(s) + 3H2O (g) 请回答下列问题:
(1)在一定温度下进行上述反应,若反应容器的容积为0.5 L,2min后达到平衡,测得固体的质量减少了4.80 g,则H2的平均反应速率_________;该反应的平衡常数表达式K=___________
(2)某温度下反应达平衡时,H2与水蒸气的体积比为2:3,则H2的平衡转化率为__________;随温度的升高,H2与水蒸气的体积比减小,则该反应为 ____ (填“吸热”或“放热”) 反应。
(3)一定温度下,在密闭恒容的容器中,能表示上述反应达到化学平衡状态的是________。
A.混合气体的总压强保持不变 B.v正(H20)= v正(H2)
C.混合气体的密度保持不变 D.混合气体的平均式量保持不变
(4)钨丝灯管中的W在使用过程中缓慢挥发,使灯丝变细,加入I2可延长灯管的使用寿命,其工作原理为:W (s) +2I2 (g)  WI4
(g)。下列说法正确的有__________。
WI4
(g)。下列说法正确的有__________。
A.温度升高时,WI4的分解速率加快,W和I2的化合速率减慢
B.WI4在灯丝上分解,产生的W又沉积在灯丝上
C.WI4在灯管壁上分解,使灯管的寿命延长
D.灯管内的I2可循环使用
查看习题详情和答案>>
金属钨用途广泛,主要用于制造硬质或耐高温的合金,以及灯泡的灯丝。高温下,在密闭容器中用H2还原WO3可得到金属钨,其总反应为:
WO3 (s) + 3H2 (g)  W (s) + 3H2O (g) 请回答下列问题:
W (s) + 3H2O (g) 请回答下列问题:
(1)在一定温度下进行上述反应,若反应容器的容积为0.5 L,2min后达到平衡,测得固体的质量减少了4.80 g,则H2的平均反应速率_________;该反应的平衡常数表达式K=___________
(2)某温度下反应达平衡时,H2与水蒸气的体积比为2:3,则H2的平衡转化率为__________;随温度的升高,H2与水蒸气的体积比减小,则该反应为 ____(填“吸热”或“放热”) 反应。
(3)一定温度下,在密闭恒容的容器中,能表示上述反应达到化学平衡状态的是________。
A.混合气体的总压强保持不变 B.v正(H20)= v正(H2)
C.混合气体的密度保持不变 D.混合气体的平均式量保持不变
(4)钨丝灯管中的W在使用过程中缓慢挥发,使灯丝变细,加入I2可延长灯管的使用寿命,其工作原理为:W (s) +2I2 (g) 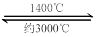 WI4 (g)。下列说法正确的有__________。
WI4 (g)。下列说法正确的有__________。
A.温度升高时,WI4的分解速率加快,W和I2的化合速率减慢
B.WI4在灯丝上分解,产生的W又沉积在灯丝上
C.WI4在灯管壁上分解,使灯管的寿命延长
D.灯管内的I2可循环使用