网址:http://m.1010jiajiao.com/timu3_id_394102[举报]
(14分)已知CO2(g)+H2(g) CO(g)+H2O(g)的平衡常数随温度变化如下表:
CO(g)+H2O(g)的平衡常数随温度变化如下表:
|
t/℃ |
700 |
800 |
850 |
1 000 |
1 200 |
|
K |
2.6 |
1.7 |
1.0 |
0.9 |
0.6 |
请回答下列问题:
(1)上述正向反应是________反应(选填“放热”或“吸热”)。
(2)若达平衡后降温,则平衡向________移动,CO2转化率________,正反应速率________(选填“增大”、“减小”或“不变”)。
(3)在850℃发生上述反应,以表中的物质的量投入恒容反应器中,其中向正反应方向移动的有________(选填A、B、C、D、E)
|
|
A |
B |
C |
D |
E |
|
n(CO2) |
3 |
1 |
0 |
1 |
1 |
|
n(H2) |
2 |
1 |
0 |
1 |
2 |
|
n(CO) |
1 |
2 |
3 |
0.5 |
3 |
|
n(H2O) |
5 |
2 |
3 |
2 |
1 |
(4)在850℃时,可逆反应:CO2(g)+H2(g) CO(g)+H2O(g),在该容器内各物质的浓度变化如下:
CO(g)+H2O(g),在该容器内各物质的浓度变化如下:
|
时间/min |
CO2 (mol/L) |
H2 (mol/L) |
CO (mol/L) |
H2O (mol/L) |
|
0 |
0.200 |
0.300 |
0 |
0 |
|
2 |
0.138 |
0.238 |
0.062 |
0.062 |
|
3 |
c1 |
c2 |
c3 |
c3 |
|
4 |
c1 |
c2 |
c3 |
c3 |
则3 min~4 min平衡后c3=______________,CO2的转化率为____________。
查看习题详情和答案>>
(14分)已知CO2(g)+H2(g)CO(g)+H2O(g)的平衡常数随温度变化如下表:
| t/℃ | 700 | 800 | 850 | 1 000 | 1 200 |
| K | 2.6 | 1.7 | 1.0 | 0.9 | 0.6 |
请回答下列问题:
(1)上述正向反应是________反应(选填“放热”或“吸热”)。
(2)若达平衡后降温,则平衡向________移动,CO2转化率________,正反应速率________(选填“增大”、“减小”或“不变”)。
(3)在850℃发生上述反应,以表中的物质的量投入恒容反应器中,其中向正反应方向移动的有________(选填A、B、C、D、E)
|
| A | B | C | D | E |
| n(CO2) | 3 | 1 | 0 | 1 | 1 |
| n(H2) | 2 | 1 | 0 | 1 | 2 |
| n(CO) | 1 | 2 | 3 | 0.5 | 3 |
| n(H2O) | 5 | 2 | 3 | 2 | 1 |
(4)在850℃时,可逆反应:CO2(g)+H2(g)CO(g)+H2O(g),在该容器内各物质的浓度变化如下:
| 时间/min | CO2 (mol/L) | H2 (mol/L) | CO (mol/L) | H2O (mol/L) |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
则3 min~4 min平衡后c3=______________,CO2的转化率为____________。
查看习题详情和答案>>
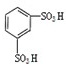
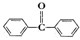 )及其衍生物,第Ⅱ类为苯甲酸苯酯(
)及其衍生物,第Ⅱ类为苯甲酸苯酯(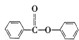 )的衍生物,某紫外线吸收剂UV-0(属于第Ⅰ类产品)的合成路线如下:
)的衍生物,某紫外线吸收剂UV-0(属于第Ⅰ类产品)的合成路线如下: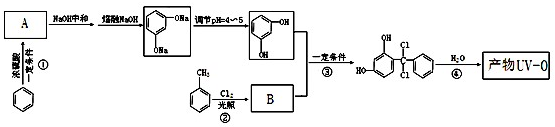
已知:
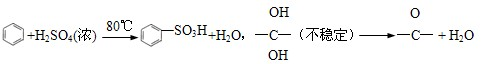
(1)A 的结构简式为

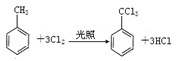
(2)反应②化学方程式为

(3)产物UV-0的同分异构体中,符合第Ⅱ类产品结构的有机化合物共有
(4)BAD也是一种紫外线吸收剂,属于第Ⅱ类产品,它的结构简式如下:
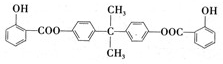
BAD中含有的官能团为
(5)
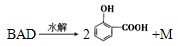
M的1H核磁共振谱图表明共含有
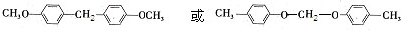
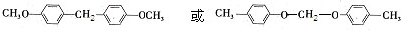
| 温度℃ 溶解度 溶质 g/100g水 |
10 | 20 | 30 | 40 | 50 | 60 | 70 |
| NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 |
| NH4HCO3 | 15.8 | 21.0 | 27.0 | ||||
| NaHCO3 | 8.2 | 9.6 | 11.1 | 12.7 | 14.4 | 16.4 | |
| NH4Cl | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 | 60.2 |
Ⅰ、化盐与精制:①粗盐(含Ca2+、Mg2+、SO42-)溶解;②加入足量NaOH和Na2CO3溶液,煮沸;③过滤;④加入盐酸调pH至7.
Ⅱ、转化:①将精制后的食盐溶液温度控制在30~35℃之间;在不断搅拌下,加入研细的碳酸氢铵;保温,搅拌半小时;②静置,
Ⅲ、制纯碱:将得的NaHCO3放入蒸发皿中,在酒精灯上灼烧,冷却到室温,即得到纯碱.
(1)“化盐与精制”可除去的粗盐中的杂质离子是
(2)“转化”的离子方程式是
(3)“转化”过程中,温度控制在30~35℃之间的加热方式是
(4)a,b处的操作分别是
(5)实验室制得的纯碱含少量NaCl还可能含少量NaHCO3,为测定纯碱的纯度,用电子天平准确称取样品G克,将其放入锥形瓶中用适量蒸馏水溶解,滴加2滴酚酞,用c mol/L的标准盐酸滴定至溶液由浅红色变成无色且半分钟不变,滴定过程中无气体产生,所用盐酸的体积为V1 mL.此时发生的反应为:CO32-+H+→HCO3-
①样品中碳酸钠质量百分含量的表达式是
| c×V1 ×10-3×M(Na2CO3)g |
| Gg |
| c×V1 ×10-3×M(Na2CO3)g |
| Gg |
②向锥形瓶溶液中继续滴加2滴甲基橙,用同浓度的盐酸继续滴定至终点,所用盐酸的体积为V2mL.滴定终点时溶液颜色的变化是
| t/min | X/mol | Y/mol | Z/mol |
| 0 | 1.00 | 1.00 | 0.00 |
| 1 | 0.90 | 0.80 | 0.20 |
| 3 | 0.75 | 0.50 | 0.50 |
| 5 | 0.65 | 0.30 | 0.70 |
| 9 | 0.55 | 0.10 | 0.90 |
| 10 | 0.55 | 0.10 | 0.90 |
| 14 | 0.55 | 0.10 | 0.90 |
(1)根据左表中数据,在图1中画出X、Y、Z的物质的量(n)随时间(t)变化的曲线:
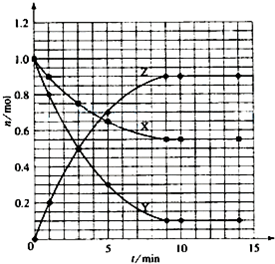

(2)体系中发生反应的化学方程式是
(3)列式计算该反应在0-3min时间内产物Z的平均反应速率:
(4)该反应达到平衡时反应物X的转化率α等于
(5)如果该反应是放热反应.改变实验条件(温度、压强、催化剂)得到Z随时间变化的曲线①、②、③(如图2所示)则曲线①、②、③所对应的实验条件改变分别是:①