摘要:27.短周期元素X.Y.Z.W原子序数依次增大.常温时化合物XW是气体. 遇氨气产生大量白烟.化合物Z2Y2是淡黄色固体. ⑴ 写出离子化合物ZW的化学式 . ⑵ 写出Z2Y2与H2O反应的化学方程式 . ⑶ 如图装置所示.进行下列操作: 第一步. 将开关K1接通后.水槽中 附近先变红 .碳棒上的电极反应式为 . 第二步. 将开关K1断开.向水槽中滴入XW的溶液至红色恰 好褪去.再接通开关K2.发现电流表指针偏转. 写出碳棒上的电极反应式 . 第三步: 一段时间后.将开关K2断开.向水槽中滴入酸性K3[Fe(CN)6]溶液.可以看到有蓝色沉淀Fe3[Fe(CN)6]2生成.标出化学式 Fe3[Fe(CN)6]2 中铁元素的化合价. ⑷ Z2Y2可与氯化亚铁溶液反应产生红褐色沉淀和能使带火星木条复燃的气体.若 沉淀和气体的物质的量之比为2:1.反应的化学方程式是 .
网址:http://m.1010jiajiao.com/timu3_id_380496[举报]
短周期元素X、Y、Z、W原子序数依次增大.X是形成化合物种类最多的元素,Y是自然界含量最多的元素,Z是同周期中金属性最强的元素,W的负一价离子与Y的某种氢化物分子含有相同的电子数.
(1)元素X、Y、Z按原子半径由大到小的顺序排列为
(2)W的单质与水反应的离子方程式为
(3)化合物A由X、Y、Z三元素共同构成,其浓溶液中通入W的单质时,可产生气体XY2和化合物ZWY3.反应的化学方程式为
查看习题详情和答案>>
(1)元素X、Y、Z按原子半径由大到小的顺序排列为
Na>C>O
Na>C>O
.(用元素符号表示).(2)W的单质与水反应的离子方程式为
Cl2+H2O=H++Cl-+HClO
Cl2+H2O=H++Cl-+HClO
.(3)化合物A由X、Y、Z三元素共同构成,其浓溶液中通入W的单质时,可产生气体XY2和化合物ZWY3.反应的化学方程式为
3Cl2+3Na2CO3=5NaCl+NaClO3+3CO2
3Cl2+3Na2CO3=5NaCl+NaClO3+3CO2
.短周期元素X、Y、Z、W原子序数依次增大.X氢化物的水溶液显碱性;Y在元素周期表中所处的周期序数与族序数相等;Z单质是将太阳能转化为电能的常用材料;W是重要的“成盐元素”,主要以钠盐的形式存在于海水中.请回答:
(1)Y在元素周期表中的位置是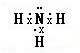
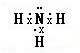 .
.
(2)X氢化物的水溶液与W氢化物的水溶液混合后恰好反应时,溶液呈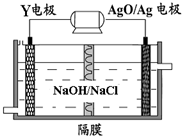
(3)Y-AgO电池是应用广泛的鱼雷电池,其原理如图所示.该电池的负极反应式是
(4)Z和W比较,非金属性较弱的是
a.元素在地壳中的含量
b.最高价氧化物对应水化物的酸性
c.断开氢化物中1mol H-Z或H-W键所需的能量
d.Z与W以共价键形成化合物时,Z或W显示的电性.
查看习题详情和答案>>
(1)Y在元素周期表中的位置是
第三周期第ⅢA族
第三周期第ⅢA族
;X氢化物的电子式是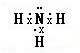
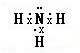
(2)X氢化物的水溶液与W氢化物的水溶液混合后恰好反应时,溶液呈
酸
酸
(填“酸”、“碱”或“中”)性,用离子方程式表示其原因是NH4++H2O?NH3?H2O+H+
NH4++H2O?NH3?H2O+H+
.
(3)Y-AgO电池是应用广泛的鱼雷电池,其原理如图所示.该电池的负极反应式是
Al+4OH--3e-=AlO2-+2H2O
Al+4OH--3e-=AlO2-+2H2O
.(4)Z和W比较,非金属性较弱的是
Si
Si
(填元素符号),下列可以验证这一结论的是bcd
bcd
(填序号).a.元素在地壳中的含量
b.最高价氧化物对应水化物的酸性
c.断开氢化物中1mol H-Z或H-W键所需的能量
d.Z与W以共价键形成化合物时,Z或W显示的电性.