摘要:31.大豆植株的颜色受一对等位基因控制.基因型AA的植株呈深绿色.基因型Aa的植株叶体呈浅绿色.基因型aa的植株呈黄色.深绿色和浅绿色植株的繁殖和生存能力相同.而黄色植株会在幼苗阶段死亡. (1)基因型为Aa的植株.有的细胞中含有两个A基因.可能的原因是 . (2)基因型为AA的植株.茎叶为绿色.而在遮光条件下茎叶为黄白色.这是因为光照会影响了 .从而影响叶绿素合成. (3)如果让深绿色植株给浅绿色植株授粉.其后代成熟植株中.基因型是 .其中深绿色植株的比值为 . (4)现有一批浅绿色植株(P).经相互授粉得到F1.成熟的F1植株经相互授粉得到F2--.以相同的方法得到Fn. ①用遗传图解表示由P得到F1的过程. ②F2成熟的植株中.浅绿色植株所占的比值是 . ③在下列坐标图中画出成熟植株中.a的基因频率随繁殖代数变化的曲线. 班级: 姓名: 考号:
网址:http://m.1010jiajiao.com/timu3_id_379330[举报]
 为测定已变质的过氧化钠的纯度,设计如下图所示的实验;Q为一具有良好的弹性气球,称取一定量的样品放于其中,按图安装的实验装置打开分液漏斗的活塞,将稀H2SO4滴入气球中.请填空:
为测定已变质的过氧化钠的纯度,设计如下图所示的实验;Q为一具有良好的弹性气球,称取一定量的样品放于其中,按图安装的实验装置打开分液漏斗的活塞,将稀H2SO4滴入气球中.请填空:(1)Q内发生反应生成
2
2
种气体,其中的反应有1
1
个氧化还原反应.(2)为测定反应生成气体的总体积,滴稀H2SO4前必须关闭(填K1、K2或K3,下同)
K1、K2
K1、K2
,打开K3
K3
.(3)当上述反应停止,将K1、K2、K3处于关闭状态,然后先打开K2,再缓缓打开K1,这时可观察到的现象是
气球Q慢慢缩小
气球Q慢慢缩小
.(4)导管a的作用是
平衡分液漏斗上下的压强使顺利流下
平衡分液漏斗上下的压强使顺利流下
.(5)b中装的固体试剂是
碱石灰
碱石灰
,为何要缓缓打开K1控制气体流速,使CO2充分吸收
控制气体流速,使CO2充分吸收
.(6)实验结束时量筒I中有x mL水,量筒II中收集到y mL气体,则过氧化钠的纯度是
| 78y |
| 53x+25y |
| 78y |
| 53x+25y |
请将下面有关原子核外电子排布原理叙述填写完整:
(1)能量最低原理:原子核外电子先占有能量
(2)泡利不相容原理:每个原子轨道上最多只能容纳
(3)洪特规则:原子核外电子在能量相同的各个轨道上排布时①电子尽可能分占不同的原子轨道,②自旋状态
查看习题详情和答案>>
(1)能量最低原理:原子核外电子先占有能量
较低
较低
的轨道.然后依次进入能量较高
较高
的轨道.(2)泡利不相容原理:每个原子轨道上最多只能容纳
2
2
个自旋状态相反
相反
的电子.(3)洪特规则:原子核外电子在能量相同的各个轨道上排布时①电子尽可能分占不同的原子轨道,②自旋状态
相
相
同,③全空、全满
全满
或半满
半满
时能量最低.甲同学釆用如图Ⅰ所示装置验证铜与稀硝酸的反应,并用排水法收集NO气体
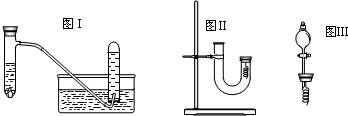
(1)写出试管内溶液中发生反应的化学方程式
(2)在实验过程中观察到试管内的溶液呈
(3)乙同学认为甲虽然收集到的气体是一氧化氮,但并不能说明反应中一定生成一氧化氮.他的理由是
有关化学方程式为:
(4)丙同学釆用如图Ⅱ所示装置进行实验,证明了铜与稀硝酸反应生成一氧化氮.该同学的步骤如下表所示,请回答实验中的有关问题.
(5)从环保的角度看,丙同学的实验存在的缺陷是
(6)丁同学用图Ⅲ所示装置代替图Ⅱ中U型管右端的附有铜丝的胶塞进行实验,待反应停止后将一氧化氮气体排入分液漏斗中,观察到的实验现象与丙同学实验的第
(7)实验结束后丁同学向分液漏斗中注入适量水并充分振荡,试写出发生的化学反应方程式
(8)若将32.64g铜与140mL一定浓度的硝酸反应,铜完全溶解,产生的NO和NO2混合气体在标准状况下的体积为11.2L(不考虑NO2的反应),试回答:
①若铜与硝刚好反应完全,则原硝酸溶液的物质的量浓度为
②将产生的气体全部释放后,向溶液中加入VmL amol?L-1的NaOH溶液,恰好使溶液中的Cu2+全部转化为沉淀,则原硝酸溶液的物质的量浓度为
mol/L
mol/L
③已知NO和NO2的混合气与足量氧气混合后能被水完全吸收成硝酸,则要使上述11.2L气体完全被水吸收成硝酸,理论上需消耗标准状况下的氧气
查看习题详情和答案>>

(1)写出试管内溶液中发生反应的化学方程式
3Cu+8HNO3=3Cu(NO3 ) 2+2NO↑+4H2O
3Cu+8HNO3=3Cu(NO3 ) 2+2NO↑+4H2O
(2)在实验过程中观察到试管内的溶液呈
绿
绿
色;收集气体的试管内的气体呈无
无
色(3)乙同学认为甲虽然收集到的气体是一氧化氮,但并不能说明反应中一定生成一氧化氮.他的理由是
在铜和稀硝酸反应容器的上部看到了红棕色气体
在铜和稀硝酸反应容器的上部看到了红棕色气体
在铜和稀硝酸反应容器的上部看到了红棕色气体
在铜和稀硝酸反应容器的上部看到了红棕色气体
有关化学方程式为:
2NO+O2=2NO2
2NO+O2=2NO2
(4)丙同学釆用如图Ⅱ所示装置进行实验,证明了铜与稀硝酸反应生成一氧化氮.该同学的步骤如下表所示,请回答实验中的有关问题.
| 实验步骤 | 问题 |
| 1从U型管左端加入稀硝酸直至充满U型管右端 | ∥/ |
| 2用附有铜丝的胶塞塞住U型管右端,观察现象 | 现象是 有无色气体产生,右边溶液逐渐变成绿色 有无色气体产生,右边溶液逐渐变成绿色 |
| 3待反应停止后打开胶塞,观察实验现象 | 现象是 无色气体与空气接触后立即变成红棕色 无色气体与空气接触后立即变成红棕色 |
将氮氧化合物放入空气中会污染环境
将氮氧化合物放入空气中会污染环境
.(6)丁同学用图Ⅲ所示装置代替图Ⅱ中U型管右端的附有铜丝的胶塞进行实验,待反应停止后将一氧化氮气体排入分液漏斗中,观察到的实验现象与丙同学实验的第
3
3
步骤的相同.丁同学要将一氧化氮气体排入分液漏斗中应进行的正确操作是①打开分液漏斗上部的塞子
打开分液漏斗上部的塞子
②慢慢打开分液漏斗的活塞
慢慢打开分液漏斗的活塞
③待液面与胶塞接触时立即关闭活塞
待液面与胶塞接触时立即关闭活塞
(7)实验结束后丁同学向分液漏斗中注入适量水并充分振荡,试写出发生的化学反应方程式
3NO2+H2O=2 HNO3+NO
3NO2+H2O=2 HNO3+NO
(8)若将32.64g铜与140mL一定浓度的硝酸反应,铜完全溶解,产生的NO和NO2混合气体在标准状况下的体积为11.2L(不考虑NO2的反应),试回答:
①若铜与硝刚好反应完全,则原硝酸溶液的物质的量浓度为
10.86mol﹒L-1
10.86mol﹒L-1
②将产生的气体全部释放后,向溶液中加入VmL amol?L-1的NaOH溶液,恰好使溶液中的Cu2+全部转化为沉淀,则原硝酸溶液的物质的量浓度为
| 10-3a﹒V +0.5 |
| 0.14 |
| 10-3a﹒V +0.5 |
| 0.14 |
③已知NO和NO2的混合气与足量氧气混合后能被水完全吸收成硝酸,则要使上述11.2L气体完全被水吸收成硝酸,理论上需消耗标准状况下的氧气
5.71
5.71
升.(保留两位小数);解题过程:设生成的一氧化氮为xmol,二氧化氮为ymol.
3Cu+8HNO3=3Cu(NO3 ) 2+2NO↑+4H2O
3 2
1.5xmol xmol
Cu+4HNO3(浓)=Cu(NO3 ) 2+2NO2↑+2H2O
1 2
ymol.ymol.
所以方程组为
所以
即一氧化氮为0.26mol,二氧化氮为0.24mol.
4NO+2H2O+3O2=4HNO3
4 3
0.26mol 0.195mol
4 NO2+2H2O+O2=4HNO3
41
0.24mol 0.06mol
所以需要氧气0.195mol+0.06mol=0.255mol,体积为0.255mol×22.4L/mol=5.71L
3Cu+8HNO3=3Cu(NO3 ) 2+2NO↑+4H2O
3 2
1.5xmol xmol
Cu+4HNO3(浓)=Cu(NO3 ) 2+2NO2↑+2H2O
1 2
| 1 |
| 2 |
所以方程组为
|
所以
|
即一氧化氮为0.26mol,二氧化氮为0.24mol.
4NO+2H2O+3O2=4HNO3
4 3
0.26mol 0.195mol
4 NO2+2H2O+O2=4HNO3
41
0.24mol 0.06mol
所以需要氧气0.195mol+0.06mol=0.255mol,体积为0.255mol×22.4L/mol=5.71L
设生成的一氧化氮为xmol,二氧化氮为ymol.
3Cu+8HNO3=3Cu(NO3 ) 2+2NO↑+4H2O
3 2
1.5xmol xmol
Cu+4HNO3(浓)=Cu(NO3 ) 2+2NO2↑+2H2O
1 2
ymol.ymol.
所以方程组为
所以
即一氧化氮为0.26mol,二氧化氮为0.24mol.
4NO+2H2O+3O2=4HNO3
4 3
0.26mol 0.195mol
4 NO2+2H2O+O2=4HNO3
41
0.24mol 0.06mol
所以需要氧气0.195mol+0.06mol=0.255mol,体积为0.255mol×22.4L/mol=5.71L
.3Cu+8HNO3=3Cu(NO3 ) 2+2NO↑+4H2O
3 2
1.5xmol xmol
Cu+4HNO3(浓)=Cu(NO3 ) 2+2NO2↑+2H2O
1 2
| 1 |
| 2 |
所以方程组为
|
所以
|
即一氧化氮为0.26mol,二氧化氮为0.24mol.
4NO+2H2O+3O2=4HNO3
4 3
0.26mol 0.195mol
4 NO2+2H2O+O2=4HNO3
41
0.24mol 0.06mol
所以需要氧气0.195mol+0.06mol=0.255mol,体积为0.255mol×22.4L/mol=5.71L
(2012?通州区一模)某有机物X(C12H13O6Br)分子中含有多种官能团,其结构简式为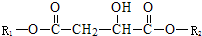 (其中R1、R2为未知部分的结构;R2中含有Br原子),为推测X的分子结构,进行如图的转化:
(其中R1、R2为未知部分的结构;R2中含有Br原子),为推测X的分子结构,进行如图的转化:
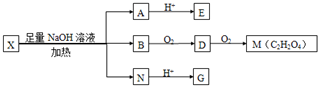
已知向E的水溶液中滴入FeCl3溶液发生显色反应;G、M都能与NaHCO3溶液反应.
(1)M的结构简式为
(2)E不能发生的反应有
a.加成反应 b.消去反应 c.氧化反应 d.取代反应
(3)B的核磁共振氢谱表明该分子中有
(4)G在一定条件下发生反应生成分子组成为C4H4O4的有机物(该有机物可使溴的四氯化碳溶液褪色),G生成C4H4O4的化学方程式为:
(5)已知X中R1里含有能与FeCl3溶液发生显色反应的官能团,且E分子中苯环上的一氯代物只有一种,则X的结构简式是:
 ;
;
(6)Y与G互为同分异构体,Y的分子中只含有醛基、羧基、羟基三种官能团,且同一个碳原子上不能同时连有两个羟基,则Y的分子结构有
查看习题详情和答案>>
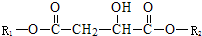 (其中R1、R2为未知部分的结构;R2中含有Br原子),为推测X的分子结构,进行如图的转化:
(其中R1、R2为未知部分的结构;R2中含有Br原子),为推测X的分子结构,进行如图的转化:
已知向E的水溶液中滴入FeCl3溶液发生显色反应;G、M都能与NaHCO3溶液反应.
(1)M的结构简式为
HOOC-COOH
HOOC-COOH
;其俗称是草酸
草酸
;(2)E不能发生的反应有
b
b
(填序号);a.加成反应 b.消去反应 c.氧化反应 d.取代反应
(3)B的核磁共振氢谱表明该分子中有
2
2
种不同类型的氢原子;由B转化成D的化学方程式是HOCH2-CH2OH+O2
OHC-CHO+2H2O
| ||
| △ |
HOCH2-CH2OH+O2
OHC-CHO+2H2O
;
| ||
| △ |
(4)G在一定条件下发生反应生成分子组成为C4H4O4的有机物(该有机物可使溴的四氯化碳溶液褪色),G生成C4H4O4的化学方程式为:
HOOC-CH2-CH(OH)-COOH
HOOC-CH=CH-COOH+H2O
| 一定条件 |
HOOC-CH2-CH(OH)-COOH
HOOC-CH=CH-COOH+H2O
;| 一定条件 |
(5)已知X中R1里含有能与FeCl3溶液发生显色反应的官能团,且E分子中苯环上的一氯代物只有一种,则X的结构简式是:


(6)Y与G互为同分异构体,Y的分子中只含有醛基、羧基、羟基三种官能团,且同一个碳原子上不能同时连有两个羟基,则Y的分子结构有
2
2
种. ”来表示.已知某环烷烃是平面结构,其结构如红十字协会的会徽,因此有人将它称为“红十字烷”,如“
”来表示.已知某环烷烃是平面结构,其结构如红十字协会的会徽,因此有人将它称为“红十字烷”,如“ ”,写出它的分子式
”,写出它的分子式