摘要:2].右图表示在适宜的温度.水分和CO2条件下.两种植物光合作用强度的变化情况.下列说法错误的是 A 当光照强度增加到一定程度时.光合作用强度不再增加.即达到饱和 B C3植物比C4植物光合作用强度更容易达到饱和 C C4植物比C3植物光能利用率高 D 水稻是阴生植物.玉米是阳生植物
网址:http://m.1010jiajiao.com/timu3_id_35677[举报]
甲醇是一种很好的燃料,被称为21世纪的新型燃料.
工业上可通过H2和CO化合制备甲醇,该反应的热化学方程式为:
CO(g)+2H2(g) CH3OH(g)△H1=-116kJ?molˉ1
CH3OH(g)△H1=-116kJ?molˉ1
(1)已知:CO(g)+
O2(g)=CO2(g)△H2=-283kJ?molˉ1
H2(g)+
O2(g)=H2O (g)△H3=-242kJ?molˉ1
1mol甲醇燃烧生成CO2和水蒸气放出
(2)在压强为0.1MPa条件下,将a mol CO与 3a mol H2的混合气体在催化剂作用下在VL容器中制备甲醇.
①若容器容积不变,下列措施可增加甲醇产率的是
A.升高温度 B.将CH3OH(g)从体系中分离
C.充入He,使体系总压强增大 D.再充入1mol CO和3mol H2
②为了寻找合成甲醇的温度和压强的适宜条件,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中.
A.则上表中剩余的实验条件数据:a=
B.根据反应特点,右上图是在压强分别为0.1MPa和5MPa下CO的转化率随温度变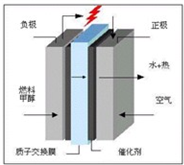 化的曲线图,请指明图中的压强P1=
化的曲线图,请指明图中的压强P1=
③100℃时,CH3OH(g) CO(g)+2H2(g)反应的平衡常数为
CO(g)+2H2(g)反应的平衡常数为
(用含a、V的代数式表示).
(3)科学家预言,燃料电池将是21世纪获得电力的重要途径,而甲醇燃料电池具备甲醇燃料容易携带、容易存储等优点,目前被认为将会替代传统的电池成为携带型设备的主要电源.右图是甲醇的质子交换膜型燃料电池模型.写出其电极反应式
正极:
负极:
查看习题详情和答案>>
工业上可通过H2和CO化合制备甲醇,该反应的热化学方程式为:
CO(g)+2H2(g)
 CH3OH(g)△H1=-116kJ?molˉ1
CH3OH(g)△H1=-116kJ?molˉ1(1)已知:CO(g)+
| 1 |
| 2 |
H2(g)+
| 1 |
| 2 |
1mol甲醇燃烧生成CO2和水蒸气放出
651
651
kJ的热量.(2)在压强为0.1MPa条件下,将a mol CO与 3a mol H2的混合气体在催化剂作用下在VL容器中制备甲醇.
①若容器容积不变,下列措施可增加甲醇产率的是
BD
BD
.A.升高温度 B.将CH3OH(g)从体系中分离
C.充入He,使体系总压强增大 D.再充入1mol CO和3mol H2
②为了寻找合成甲醇的温度和压强的适宜条件,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中.

| 实验编号 | T(℃) | n(CO)/n(H2) | P(MPa) |
| 1 | 150 | 1/3 | 0.1 |
| 2 | a | 1/3 | 5 |
| 3 | 350 | b | 5 |
150
150
、b=1/3
1/3
.B.根据反应特点,右上图是在压强分别为0.1MPa和5MPa下CO的转化率随温度变
 化的曲线图,请指明图中的压强P1=
化的曲线图,请指明图中的压强P1=0.1
0.1
MPa.③100℃时,CH3OH(g)
 CO(g)+2H2(g)反应的平衡常数为
CO(g)+2H2(g)反应的平衡常数为| 4a2 |
| V2 |
| 4a2 |
| V2 |
(用含a、V的代数式表示).
(3)科学家预言,燃料电池将是21世纪获得电力的重要途径,而甲醇燃料电池具备甲醇燃料容易携带、容易存储等优点,目前被认为将会替代传统的电池成为携带型设备的主要电源.右图是甲醇的质子交换膜型燃料电池模型.写出其电极反应式
正极:
3O2+12e-+12H+→6H2O
3O2+12e-+12H+→6H2O
负极:
2CH4O-12e-+2H2O→12H++2CO2
2CH4O-12e-+2H2O→12H++2CO2
.
甲醇是一种很好的燃料,被称为21世纪的新型燃料.
工业上可通过H2和CO化合制备甲醇,该反应的热化学方程式为:
CO(g)+2H2(g) CH3OH(g)△H1=-116kJ?molˉ1
CH3OH(g)△H1=-116kJ?molˉ1
(1)已知:CO(g)+ O2(g)=CO2(g)△H2=-283kJ?molˉ1
O2(g)=CO2(g)△H2=-283kJ?molˉ1
H2(g)+ O2(g)=H2O (g)△H3=-242kJ?molˉ1
O2(g)=H2O (g)△H3=-242kJ?molˉ1
1mol甲醇燃烧生成CO2和水蒸气放出 kJ的热量.
(2)在压强为0.1MPa条件下,将a mol CO与 3a mol H2的混合气体在催化剂作用下在VL容器中制备甲醇.
①若容器容积不变,下列措施可增加甲醇产率的是 .
A.升高温度 B.将CH3OH(g)从体系中分离
C.充入He,使体系总压强增大 D.再充入1mol CO和3mol H2
②为了寻找合成甲醇的温度和压强的适宜条件,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中.
A.则上表中剩余的实验条件数据:a= 、b= .
B.根据反应特点,右上图是在压强分别为0.1MPa和5MPa下CO的转化率随温度变化的曲线图,请指明图中的压强P1= MPa.
③100℃时,CH3OH(g) CO(g)+2H2(g)反应的平衡常数为
CO(g)+2H2(g)反应的平衡常数为
(用含a、V的代数式表示).
(3)科学家预言,燃料电池将是21世纪获得电力的重要途径,而甲醇燃料电池具备甲醇燃料容易携带、容易存储等优点,目前被认为将会替代传统的电池成为携带型设备的主要电源.右图是甲醇的质子交换膜型燃料电池模型.写出其电极反应式
正极:
负极: .

 查看习题详情和答案>>
查看习题详情和答案>>
工业上可通过H2和CO化合制备甲醇,该反应的热化学方程式为:
CO(g)+2H2(g)
 CH3OH(g)△H1=-116kJ?molˉ1
CH3OH(g)△H1=-116kJ?molˉ1(1)已知:CO(g)+
 O2(g)=CO2(g)△H2=-283kJ?molˉ1
O2(g)=CO2(g)△H2=-283kJ?molˉ1H2(g)+
 O2(g)=H2O (g)△H3=-242kJ?molˉ1
O2(g)=H2O (g)△H3=-242kJ?molˉ11mol甲醇燃烧生成CO2和水蒸气放出 kJ的热量.
(2)在压强为0.1MPa条件下,将a mol CO与 3a mol H2的混合气体在催化剂作用下在VL容器中制备甲醇.
①若容器容积不变,下列措施可增加甲醇产率的是 .
A.升高温度 B.将CH3OH(g)从体系中分离
C.充入He,使体系总压强增大 D.再充入1mol CO和3mol H2
②为了寻找合成甲醇的温度和压强的适宜条件,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中.
| 实验编号 | T(℃) | n(CO)/n(H2) | P(MPa) |
| 1 | 150 | 1/3 | 0.1 |
| 2 | a | 1/3 | 5 |
| 3 | 350 | b | 5 |
B.根据反应特点,右上图是在压强分别为0.1MPa和5MPa下CO的转化率随温度变化的曲线图,请指明图中的压强P1= MPa.
③100℃时,CH3OH(g)
 CO(g)+2H2(g)反应的平衡常数为
CO(g)+2H2(g)反应的平衡常数为 (用含a、V的代数式表示).
(3)科学家预言,燃料电池将是21世纪获得电力的重要途径,而甲醇燃料电池具备甲醇燃料容易携带、容易存储等优点,目前被认为将会替代传统的电池成为携带型设备的主要电源.右图是甲醇的质子交换膜型燃料电池模型.写出其电极反应式
正极:
负极: .

 查看习题详情和答案>>
查看习题详情和答案>>