摘要:浓NaOH溶液 浓H2SO4 24.某中学研究性学习小组的同学对牛奶中的蛋白质进行分析实验:取30mL牛奶(密度为1.03g·cm-3).用盖尔达法分解蛋白质.把氮完全转化为氨.用0.5mol·L-1 H2SO4溶液50.0mL吸收后.剩余的酸用38.0 mL 1 mol·L-1的NaOH溶液中和. 水蒸气 分解 盖尔达法:蛋白质 硫酸铵 氨 求:(1)30.0mL牛奶中含有多少克氮? (2)如果蛋白质中氮元素的质量分数为16.8%.则牛奶中含蛋白质的质量分数为多 少?25.某温度下的溶液中.c(H+)=10x mol/L.c(OH-)=10y mol/L.x与y的关系如右图所示, (1)求该温度下.中性溶液的pH. (2)求该温度下0.01mol/L NaOH溶液的pH. (3)该温度下.pH= a的醋酸溶液与pH= b的NaOH溶液等体积混合.恰好完全反应.求此醋酸溶液中醋酸的电离度. 高考科目教学质量第一次检测
网址:http://m.1010jiajiao.com/timu3_id_355987[举报]
(2010?合肥三模)以下是一些元素的信ο,其中有一种元素不在短周期.根据信ο完成问题:
(1)写出A元素基态原子的核外电子排布式
(2)B、C、X的简单离子半径由大到小的顺序为
(3)化合物YZ4B化学键的类型是
(4)A元素的单质在潮湿空气中锈蚀生成绿色物质,用一个化学方程式表示锈蚀过程
(5)常温下,工业上用惰性电极在电解槽中电解100L 1.5mol?L-1CB的水溶液时,两极共收集到气体22.4L(标准状况下),计算电解后阴极区溶液的pH=
查看习题详情和答案>>
| 元素A | 元素B | 元素C | 元素X | 元素Y | 元素Z |
| 单质是一种常见金属,与元素X形成黑色和砖红色两种化合物 | 单质是一种黄绿色气体 | 短周期中金属性最强,与X反应能生成两种化合物 | 最外层电子数是内层电子数的3倍,能形成双原子阴离子 | 单质为双原子分子,结构中σ键与π键数目比为1:2 | 阳离子就是一个质子 |
1s22s22p63s23p63d104s1或[Ar]3d104s1
1s22s22p63s23p63d104s1或[Ar]3d104s1
.(2)B、C、X的简单离子半径由大到小的顺序为
Cl->O2->Na+
Cl->O2->Na+
(用元素离子符号表示).(3)化合物YZ4B化学键的类型是
离子键和共价键
离子键和共价键
,检验该固体化合物中阳离子的实验的方法和现象是取少量固体于试管中,加入浓NaOH溶液并加热,用湿润的红色石蕊试纸放在试管口,红色石蕊试纸变蓝
取少量固体于试管中,加入浓NaOH溶液并加热,用湿润的红色石蕊试纸放在试管口,红色石蕊试纸变蓝
.(4)A元素的单质在潮湿空气中锈蚀生成绿色物质,用一个化学方程式表示锈蚀过程
2Cu+O2+CO2+H2O═Cu2(OH)2CO3
2Cu+O2+CO2+H2O═Cu2(OH)2CO3
.(5)常温下,工业上用惰性电极在电解槽中电解100L 1.5mol?L-1CB的水溶液时,两极共收集到气体22.4L(标准状况下),计算电解后阴极区溶液的pH=
12
12
(假设电解前后溶液体积不变).进行化学实验时,必须规范操作,强化安全意识,防止发生事故.下列做法错误的是( )
①实验室装有白磷的试剂瓶上贴有标签:
②稀释浓H2SO4时,将浓HSO沿器壁慢慢倒入水中,并用玻璃棒不断搅拌
③实验室制取氯气时,未设计尾气吸收装置
④做金属钠的性质实验时,剩余的钠放回原试剂瓶
⑤金属钠着火时,用泡沫灭火器扑灭
⑥浓NaOH溶液溅到皮肤上,立即用稀H2SO4清洗.
①实验室装有白磷的试剂瓶上贴有标签:

②稀释浓H2SO4时,将浓HSO沿器壁慢慢倒入水中,并用玻璃棒不断搅拌
③实验室制取氯气时,未设计尾气吸收装置
④做金属钠的性质实验时,剩余的钠放回原试剂瓶
⑤金属钠着火时,用泡沫灭火器扑灭
⑥浓NaOH溶液溅到皮肤上,立即用稀H2SO4清洗.
查看习题详情和答案>>
原子序数由小到大排列的四种短周期元素X、Y、Z、W,四种元素的原子序数之和为32,在周期表中X是原子半径最小的元素,Y、Z左右相邻,Z、W位于同主族.
(1)X元素是
(2)X与Y 形成化合物的电子式为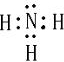
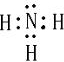 ,X与W组成的化合物中存在
,X与W组成的化合物中存在
(3)写出实验室制备YX3的化学方程式:
(4)由X、Y、Z、W四种元素组成的一种离子化合物A,已知1mol A能与足量NaOH浓溶液反应生成标准状况下44.8L气体.则A的名称是
(5)由X、Y、Z、W和Fe五种元素组成的式量为392的化合物B,1mol B中含有6mol结晶水.对化合物B进行如下实验:
a. 取B的溶液加入过量浓NaOH溶液并加热,产生白色沉淀和无色刺激性气味气体.过一段时间白色沉淀变为灰绿色,最终变为红褐色;b. 另取B的溶液,加入过量BaCl2溶液产生白色沉淀,加盐酸沉淀不溶解则B的化学式为
查看习题详情和答案>>
(1)X元素是
氢
氢
(填名称),W在周期表中的位置第三周期第ⅥA族
第三周期第ⅥA族
.(2)X与Y 形成化合物的电子式为
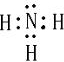
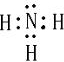
共价
共价
键(填“离子”“共价”).(3)写出实验室制备YX3的化学方程式:
2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O
| ||
2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O
| ||
(4)由X、Y、Z、W四种元素组成的一种离子化合物A,已知1mol A能与足量NaOH浓溶液反应生成标准状况下44.8L气体.则A的名称是
硫酸铵
硫酸铵
.(5)由X、Y、Z、W和Fe五种元素组成的式量为392的化合物B,1mol B中含有6mol结晶水.对化合物B进行如下实验:
a. 取B的溶液加入过量浓NaOH溶液并加热,产生白色沉淀和无色刺激性气味气体.过一段时间白色沉淀变为灰绿色,最终变为红褐色;b. 另取B的溶液,加入过量BaCl2溶液产生白色沉淀,加盐酸沉淀不溶解则B的化学式为
(NH4)2Fe(SO4)2?6H2O
(NH4)2Fe(SO4)2?6H2O
.