摘要:33.用KClO3热分解法制得的O2中常有微量的Cl2和O3.为测定Cl2和O3的含量.将KClO3分解后所得气体V1L通过足量的KI溶液.所得气体干燥后为V2L.再用Na2S2O3滴定KI溶液中生成的I2.反应如下: O3+2KI+H2O=O2+I2+2KOH --------①式 Cl2+2KI=I2+2KCl --------②式 I2+2 Na2S2O3=2NaI+ Na2S4O6 --------③式 若V1=1.00L,V2=0.98L,滴定时消耗0.10moL·L-1的Na2S2O3溶液0.0267L.求KClO3热分解得到的气体里Cl2和O3的体积分数. [高三化学综合练习答案]
网址:http://m.1010jiajiao.com/timu3_id_355030[举报]
冶炼金属常用以下几种方法:①以C、CO或H2做还原剂 ②以活泼金属Na、Mg等还原 ③利用铝热反应原理还原 ④电解法 ⑤热分解法.下列金属各采用哪种方法还原最佳.(用序号填写下列空白.)
(1)Fe、Zn、Cu等中等活泼金属 .
(2)Na、Mg、Al等活泼或较活泼金属 .
(3)Hg、Ag等不活泼金属 .
查看习题详情和答案>>
(1)Fe、Zn、Cu等中等活泼金属
(2)Na、Mg、Al等活泼或较活泼金属
(3)Hg、Ag等不活泼金属
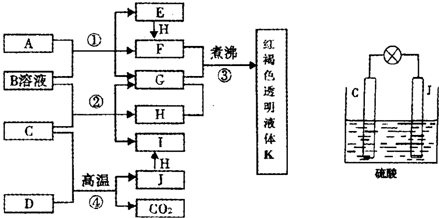
已知D、H是常见的非金属单质,其中H是黄绿色气体.J是一种金属单质,J元素的+2价化合物比+4价化合物稳定.D、J元素在周期表中同主族,D是形成化合物种类最多的元素.A、C是金属氧化物,C和J均是某种常见电池的电极材料,B与C反应时,每生成1mol H同时消耗4mol B和1mol C.它们之间的关系如图:
(1)写出物质A的化学式
(2)写出反应②的化学方程式
(3)由金属氧化物A和C得到其相应的金属单质,在冶金工业上一般可用
①热分解法 ②热还原法 ③电解法
其中从A得到其相应金属也可以用铝热法,若反应中lmolA参加反应,转移电子的物质的量为
(4)用C、J作电极,与硫酸构成如图所示电池,工作时电池发生的总反应式为
(5)向框图中的红褐色透明液体K中逐滴滴入HCl溶液.可以观察到先产生红褐色沉淀,后红褐色沉淀溶解,请解释原因
查看习题详情和答案>>
(1)写出物质A的化学式
Fe3O4
Fe3O4
.(2)写出反应②的化学方程式
PbO2+4HCl=PbCl2+Cl2↑+2H2O
PbO2+4HCl=PbCl2+Cl2↑+2H2O
.(3)由金属氧化物A和C得到其相应的金属单质,在冶金工业上一般可用
②
②
方法(填序号).①热分解法 ②热还原法 ③电解法
其中从A得到其相应金属也可以用铝热法,若反应中lmolA参加反应,转移电子的物质的量为
8
8
mol.(4)用C、J作电极,与硫酸构成如图所示电池,工作时电池发生的总反应式为
Pb+PbO2+2H2SO4=2PbSO4+2H2O
Pb+PbO2+2H2SO4=2PbSO4+2H2O
,当反应转移1mol电子时,溶液中消耗H+的物质的量为2
2
mol.(5)向框图中的红褐色透明液体K中逐滴滴入HCl溶液.可以观察到先产生红褐色沉淀,后红褐色沉淀溶解,请解释原因
开始加盐酸时,氢氧化铁胶体遇电解质发生聚沉,再继续滴加则氢氧化铁沉淀与盐酸发生酸碱中和反应,沉淀溶解
开始加盐酸时,氢氧化铁胶体遇电解质发生聚沉,再继续滴加则氢氧化铁沉淀与盐酸发生酸碱中和反应,沉淀溶解

已知D、M、H是常见的非金属单质,其中M是无色气体,H是有色气体,J是一种金属单质(其同族的某种元素是形成化合物种类最多的元素),A、C是金属氧化物,C和J均是某种常见电池的电极材料,J元素的+2价化合物比+4价化合物稳定,B与C反应时,每生成1molH同时消耗4molB和1molC,K只知含有CO 或CO2中的一种或两种.它们关系如图:

(1)写出下列物质的化学式:A
(2)写出下列反应的化学方程式:
②
⑤
(3)由金属氧化物A和C得到其相应的金属,在冶金工业上一般可用
①热分解法 ②热还原法 ③电解法
其中从A得到其相应金属也可用铝热法,若反应中1molA参加反应,转移电子的物质的量为
(4)用C、J作电极,与硫酸构成如图所示电池,正极的电极反应为

查看习题详情和答案>>

(1)写出下列物质的化学式:A
Fe3O4
Fe3O4
DC
C
(2)写出下列反应的化学方程式:
②
PbO2+4HCl(浓)═PbCl2+Cl2↑+2H2O
PbO2+4HCl(浓)═PbCl2+Cl2↑+2H2O
⑤
2HClO═2HCl+O2↑
2HClO═2HCl+O2↑
(3)由金属氧化物A和C得到其相应的金属,在冶金工业上一般可用
②
②
方法(填序号)①热分解法 ②热还原法 ③电解法
其中从A得到其相应金属也可用铝热法,若反应中1molA参加反应,转移电子的物质的量为
8mol
8mol
(4)用C、J作电极,与硫酸构成如图所示电池,正极的电极反应为
PbO2+2e-+4H++SO42-═PbSO4+2H2O
PbO2+2e-+4H++SO42-═PbSO4+2H2O
当反应转移1mol电子时,负极质量增加48
48
g.
常见金属的冶炼方法
(1)热分解法:适用于冶炼金属活动性较差的金属(金属活动顺序表中 及其以后的金属),如:
(2)电解法:适合冶炼活动性很强的金属(一般在金属活动性顺序表中排在 及其以前的金属).如: ;
; ;
(3)热还原法:用还原剂(C、CO、H2、Al等)还原金属氧化物,适用于金属活动性顺序表中的 与 之间的大多数金属的冶炼.如: ; ; ; ; ;
铝热反应实验现象及化学方程式:
实验说明:
a、Al与Fe2O3能发生铝热反应,与其它较不活泼金属氧化物也能发生铝热反应.
b、铝热反应的最大特点是放出大量的热,在生产上利用这一特点,可用于焊接钢轨,冶金工业上也常用这一原理,使铝与金属氧化物反应,冶炼钒、铬、锰等.如:
Al+ MnO2═ .
查看习题详情和答案>>
(1)热分解法:适用于冶炼金属活动性较差的金属(金属活动顺序表中
(2)电解法:适合冶炼活动性很强的金属(一般在金属活动性顺序表中排在
(3)热还原法:用还原剂(C、CO、H2、Al等)还原金属氧化物,适用于金属活动性顺序表中的
铝热反应实验现象及化学方程式:
| 现 象 | |
| 铝与氧化铁反应的化学方程式 |
a、Al与Fe2O3能发生铝热反应,与其它较不活泼金属氧化物也能发生铝热反应.
b、铝热反应的最大特点是放出大量的热,在生产上利用这一特点,可用于焊接钢轨,冶金工业上也常用这一原理,使铝与金属氧化物反应,冶炼钒、铬、锰等.如: