摘要:重铭酸钾化学式为K2Cr2O7.俗称红矾.有毒.它是可溶性的美丽的红色晶体.将K2Cr2O7跟浓H2SO4混合.发生反应:K2Cr2O7 + H2SO4 == K2SO4 + 2CrO3 + H2O.得到的CrO3是橙红色晶体.与水反应得到红色的溶液.它能将铜件表面处理得很光亮且不易锈蚀. (1)生成CrO3的反应是由两种基本类型的反应共同完成的.一种是 反应.另一种是 反应. (2)CrO3属于哪一类氧化物 (3)将CrO3的水溶液与过量NaOH反应时.可得到一种类似硫酸钠组成的的黄色盐类.它的化学式为 .
网址:http://m.1010jiajiao.com/timu3_id_355025[举报]
有机物X含有碳、氢、氧三种元素。
(1)探究X与钠反应产生气体的成分。
①X与钠反应产生的气体具有可燃性。将气体点燃,把一干燥的小烧杯罩在火焰上,片刻在烧杯壁上出现液滴,迅速倒转烧杯,向烧杯中加入少量澄清石灰水,未见浑浊。则X与钠反应产生的气体为________。
②根据苯、乙烷等碳氢化合物不能与钠反应产生上述气体这一事实,可得出X分子里有不同于烃分子里的氢原子存在。即有机物X除含有碳氢键之外,还有的化学键是________键。
(2)工业上, X可由乙烯与水反应制得,则X的分子式是________。
X分子含有的官能团的名称是________。写出X发生催化氧化反应的化学方程式______________。
X能被酸性高锰酸钾或重铬酸钾氧化为生活中的另一种重要的有机化合物Y,X与Y发生反应的化学方程式是________________。为了提高该反应的反应速率,可采取的措施是_______________。可用某溶液除去产品中混有的杂质,写出除杂过程发生反应的化学反应方程式______________________。
查看习题详情和答案>>
(2011?西城区一模)铬铁矿的主要成分可表示为FeO?Cr2O3,还含有SiO2、Al2O3等杂质,以铬铁矿为原料制备重铬酸钾(K2Cr2O7)的过程如下图所示.
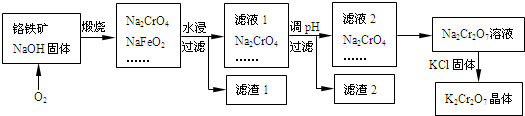
已知:①NaFeO2遇水强烈水解.②Cr2O72-+H2O 2CrO42-+2H+
2CrO42-+2H+
请回答:
(1)K2Cr2O7中Cr元素的化合价是
(2)生成滤渣1中红褐色物质的反应的化学方程式是
(3)利用滤渣2,可制得两种氧化物,其中一种氧化物经电解冶炼可获得金属,该电解反应的化学方程式是
(4)由滤液2转化为Na2Cr2O7溶液应采取的措施是
(5)向Na2Cr2O7溶液中加入KCl固体,获得K2Cr2O7晶体的操作依次是:加热浓缩、
(6)煅烧铬铁矿生成Na2CrO4和NaFeO2反应的化学方程式是
查看习题详情和答案>>

已知:①NaFeO2遇水强烈水解.②Cr2O72-+H2O
 2CrO42-+2H+
2CrO42-+2H+请回答:
(1)K2Cr2O7中Cr元素的化合价是
+6
+6
.(2)生成滤渣1中红褐色物质的反应的化学方程式是
NaFeO2+2H2O=NaOH+Fe(OH)3↓
NaFeO2+2H2O=NaOH+Fe(OH)3↓
.滤液1的成分除Na2CrO4外,还含有(填化学式)NaAlO2、Na2SiO3和NaOH
NaAlO2、Na2SiO3和NaOH
.(3)利用滤渣2,可制得两种氧化物,其中一种氧化物经电解冶炼可获得金属,该电解反应的化学方程式是
2Al2O3(熔融)
4Al+3O2↑
| ||
2Al2O3(熔融)
4Al+3O2↑
.
| ||
(4)由滤液2转化为Na2Cr2O7溶液应采取的措施是
加硫酸酸化
加硫酸酸化
.(5)向Na2Cr2O7溶液中加入KCl固体,获得K2Cr2O7晶体的操作依次是:加热浓缩、
冷却结晶
冷却结晶
、过滤、洗涤、干燥.(6)煅烧铬铁矿生成Na2CrO4和NaFeO2反应的化学方程式是
4FeO?Cr2O3+7O2+20NaOH
8Na2CrO4+4NaFeO2+10H2O
| ||
4FeO?Cr2O3+7O2+20NaOH
8Na2CrO4+4NaFeO2+10H2O
.
| ||
已知重铬酸钾K2Cr2O7和浓盐酸在常温下反应可生成氯气,试回答下列问题:
(1)请完成并配平如下的化学方程式(将未知物的化学式和化学计量数填入)
(2)浓盐酸在上述反应中显示(填写序号)
A.只有还原性 B.只有氧化性 C.只有酸性 D.既有氧化性又有还原性 E.既有酸性又有还原性
(3)若反应中转移0.6mol 电子,则被氧化的还原剂的物质的量为
(4)已知ClO2(气体)具有很强的氧化性,故常用作消毒剂,其消毒的效率(以单位质量的消毒剂得到电子的物质的量大小来表示) 约是Cl2的
查看习题详情和答案>>
(1)请完成并配平如下的化学方程式(将未知物的化学式和化学计量数填入)
1
1
K2Cr2O7+14
14
HCl═2
2
KCl+2
2
CrCl3+3
3
Cl2↑+7
7
□(2)浓盐酸在上述反应中显示(填写序号)
E
E
A.只有还原性 B.只有氧化性 C.只有酸性 D.既有氧化性又有还原性 E.既有酸性又有还原性
(3)若反应中转移0.6mol 电子,则被氧化的还原剂的物质的量为
0.6
0.6
mol,产生的Cl2的体积(STP)为6.72
6.72
L.(4)已知ClO2(气体)具有很强的氧化性,故常用作消毒剂,其消毒的效率(以单位质量的消毒剂得到电子的物质的量大小来表示) 约是Cl2的
2.63
2.63
倍(保留2位小数)工业上用铬铁矿(主要成分FeO?Cr2O3,杂质为SiO2、Al2O3等)生产重铬酸钾(化学式K2Cr2O,)的流程如下:

(1)固体A中,除Na2CrO4、NaFeO2、NaOH外还有
(2)固体A水浸时,NaFeO2会发生强烈水解产生固体B,其化学反应方程式为
(3)固体C中含有2种物质,要先加入下列物质中的
A.氢氧化钠溶液 B.稀氨水 C.稀盐酸
(4)步骤④加入盐酸得到的溶液F中,除Na2Cr2O7外,还含有的溶质是
(5)在上述流程中,有氧化还原反应发生的是第
(6)已知20℃时K2Cr2O7饱和溶液浓度为0.4mol?L-1,步骤⑤中加入固体氯化钾,若使K+离子浓度达到4mol?L-1(保持温度20℃),则溶液F中Cr2O2-7离子的浓度最大为
查看习题详情和答案>>

(1)固体A中,除Na2CrO4、NaFeO2、NaOH外还有
Na2SiO3、NaAlO2
Na2SiO3、NaAlO2
等;(2)固体A水浸时,NaFeO2会发生强烈水解产生固体B,其化学反应方程式为
NaFeO2+2H2O=NaOH+Fe(OH)3
NaFeO2+2H2O=NaOH+Fe(OH)3
;(3)固体C中含有2种物质,要先加入下列物质中的
C
C
,然后才能进行过滤分离.A.氢氧化钠溶液 B.稀氨水 C.稀盐酸
(4)步骤④加入盐酸得到的溶液F中,除Na2Cr2O7外,还含有的溶质是
NaCl
NaCl
;(5)在上述流程中,有氧化还原反应发生的是第
①
①
步.(6)已知20℃时K2Cr2O7饱和溶液浓度为0.4mol?L-1,步骤⑤中加入固体氯化钾,若使K+离子浓度达到4mol?L-1(保持温度20℃),则溶液F中Cr2O2-7离子的浓度最大为
0.016mol/L
0.016mol/L
.(2012?浦东新区二模)铬铁矿的主要成分可表示为FeO?Cr2O3,还含有MgO、Al2O3、Fe2O3等杂质,以下是以铬铁矿为原料制备重铬酸钾(K2Cr2O7)的流程图:
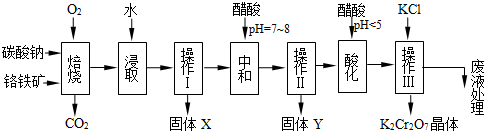
已知:
①4FeO?Cr2O3+8Na2CO3+7O2
8Na2CrO4+2Fe2O3+8CO2↑;
②Na2CO3+Al2O3
2NaAlO2+CO2↑;
③Cr2O72-+H2O?2CrO42-+2H+
根据题意回答下列问题:
(1)固体X中主要含有
(2)酸化步骤用醋酸调节溶液pH<5,其目的是
物质溶解度/(g/100g水)0°C40°C80°CKCl2840.151.3NaCl35.736.438K2Cr2O74.726.373Na2Cr2O7163215376
(3)操作Ⅲ有多步组成,获得K2Cr2O7晶体的操作依次是:加入KCl固体、蒸发浓缩、
(4)表格是相关物质的溶解度数据,操作Ⅲ发生反应的化学方程式是:Na2Cr2O7+2KCl→K2Cr2O7↓+2NaCl.
该反应在溶液中能发生的理由是
(5)副产品Y主要含氢氧化铝,还含少量镁、铁的难溶化合物及可溶性杂质,精确分析Y中氢氧化铝含量的方法是称取n g样品,加入过量
(用含m、n的代数式表示).
(6)六价铬有毒,而Cr3+相对安全.工业含铬(CrO3)废渣无害化处理的方法之一是干法解毒,用煤不完全燃烧生成的CO还原CrO3.在实验室中模拟这一过程的装置如下:
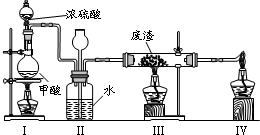
CO由甲酸脱水制得;实验结束时熄灭酒精灯的顺序是
查看习题详情和答案>>

已知:
①4FeO?Cr2O3+8Na2CO3+7O2
| 750℃ |
②Na2CO3+Al2O3
| 750℃ |
③Cr2O72-+H2O?2CrO42-+2H+
根据题意回答下列问题:
(1)固体X中主要含有
Fe2O3、MgO
Fe2O3、MgO
(填写化学式);要检测酸化操作中溶液的pH是否等于4.5,应该使用pH计或精密pH试纸
pH计或精密pH试纸
(填写仪器或试剂名称).(2)酸化步骤用醋酸调节溶液pH<5,其目的是
使CrO42-转化为Cr2O72-
使CrO42-转化为Cr2O72-
.物质溶解度/(g/100g水)0°C40°C80°CKCl2840.151.3NaCl35.736.438K2Cr2O74.726.373Na2Cr2O7163215376
(3)操作Ⅲ有多步组成,获得K2Cr2O7晶体的操作依次是:加入KCl固体、蒸发浓缩、
冷却结晶
冷却结晶
、过滤、洗涤
洗涤
、干燥.(4)表格是相关物质的溶解度数据,操作Ⅲ发生反应的化学方程式是:Na2Cr2O7+2KCl→K2Cr2O7↓+2NaCl.
该反应在溶液中能发生的理由是
K2Cr2O7的溶解度比Na2Cr2O7小(或四种物质中K2Cr2O7的溶解度最小).
K2Cr2O7的溶解度比Na2Cr2O7小(或四种物质中K2Cr2O7的溶解度最小).
.
| 物质 | 溶解度/(g/100g水) | ||
| 0°C | 40°C | 80°C | |
| KCl | 28 | 40.1 | 51.3 |
| NaCl | 35.7 | 36.4 | 38 |
| K2Cr2O7 | 4.7 | 26.3 | 73 |
| Na2Cr2O7 | 163 | 215 | 376 |
NaOH溶液
NaOH溶液
(填写试剂)、溶解、过滤、再通入过量二氧化碳
通入过量二氧化碳
(填写试剂)、…灼烧、冷却、称量,得干燥固体m g.计算样品中氢氧化铝的质量分数为| 26m |
| 17n |
| 26m |
| 17n |
(6)六价铬有毒,而Cr3+相对安全.工业含铬(CrO3)废渣无害化处理的方法之一是干法解毒,用煤不完全燃烧生成的CO还原CrO3.在实验室中模拟这一过程的装置如下:

CO由甲酸脱水制得;实验结束时熄灭酒精灯的顺序是
III、I、IV
III、I、IV
.