摘要: 0.01 kg氢气完全燃烧生成液态水要放出1429 kJ的热量.则以下热化学方程式的表示正确的是:
网址:http://m.1010jiajiao.com/timu3_id_354933[举报]
氮气与氢气反应生成氨气的平衡常数见表:
(1)工业上合成氨的温度一般控制在500℃,原因是 .
(2)在2L密闭容器中加入1mol氮气和3mol氢气,进行工业合成氨的模拟实验,若2分钟后,容器内压强为原来的0.8倍,则0到2分钟,氨气的反应速率为 mol/(L?min).
(3)下列说法能表明该反应达到平衡的是 .
A.气体的平均分子量不再变化
B.密闭容器内的压强不再变化
C.v(N2)=2v(NH3)
D.气体的密度不再变化
(4)下列措施,既能加快该反应的反应速率,又能增大转化率的是 .
A.使用催化剂 B.缩小容器体积 C.提高反应温度 D.移走NH3
(5)常温下,在氨水中加入一定量的氯化铵晶体,下列说法错误的是 .
A.溶液的pH增大 B.氨水的电离度减小 C.(OH-)减小 D.(NH4+)减小
(6)将氨水与盐酸等浓度等体积混合,下列做法能使(NH4+)与(Cl-)比值变大的是 .
A.加入固体氯化铵 B.通入少量氯化氢 C.降低溶液温度 D.加入少量固体氢氧化钠.
查看习题详情和答案>>
| N2+3H2?2NH3 | ||||
| 温度 | 25℃ | 200℃ | 400℃ | 600℃ |
| 平衡常数K | 5×108 | 650 | 0.507 | 0.01 |
(2)在2L密闭容器中加入1mol氮气和3mol氢气,进行工业合成氨的模拟实验,若2分钟后,容器内压强为原来的0.8倍,则0到2分钟,氨气的反应速率为
(3)下列说法能表明该反应达到平衡的是
A.气体的平均分子量不再变化
B.密闭容器内的压强不再变化
C.v(N2)=2v(NH3)
D.气体的密度不再变化
(4)下列措施,既能加快该反应的反应速率,又能增大转化率的是
A.使用催化剂 B.缩小容器体积 C.提高反应温度 D.移走NH3
(5)常温下,在氨水中加入一定量的氯化铵晶体,下列说法错误的是
A.溶液的pH增大 B.氨水的电离度减小 C.(OH-)减小 D.(NH4+)减小
(6)将氨水与盐酸等浓度等体积混合,下列做法能使(NH4+)与(Cl-)比值变大的是
A.加入固体氯化铵 B.通入少量氯化氢 C.降低溶液温度 D.加入少量固体氢氧化钠.
下列三个反应在某密闭容器中进行:
反应①Fe(s)+CO2(g)?FeO(s)+CO(g)△H1=a kJ?mol-1
反应②2CO(g)+O2(g)?2CO2(g)△H2=b kJ?mol-1
反应③2Fe(s)+O2(g)?2FeO(s)△H3
(1)则△H3=
(2)已知500℃时反应①的平衡常数K=1.0,在此温度下2L密闭容器中进行反应①,Fe和CO2的起始量均为2.0mol,达到平衡时CO2的转化率为
(3)将上述平衡体系升温至700℃,再次达到平衡时体系中CO的浓度是CO2浓度的两倍,则a
A.缩小反应器体积 B.再通入CO2 C.升高温度 D.使用合适的催化剂
(4)最近一些科学家研究采用高质子导电性的SCY陶瓷(能传递H+)实现氮的固定--氨的电解法合成,大大提高了氮气和氢气的转化率.总反应式为:N2+3H2
2NH3.则在电解法合成氨的过程中,应将H2不断地通入
(5)在25℃下,将a mol?L-1的氨水与0.01mol?L-1的盐酸等体积混合,反应后溶液中c(NH4+)=c(Cl-),则溶液显
查看习题详情和答案>>
反应①Fe(s)+CO2(g)?FeO(s)+CO(g)△H1=a kJ?mol-1
反应②2CO(g)+O2(g)?2CO2(g)△H2=b kJ?mol-1
反应③2Fe(s)+O2(g)?2FeO(s)△H3
(1)则△H3=
(2a+b)kJ?mol-1
(2a+b)kJ?mol-1
(用含a、b的代数式表示)(2)已知500℃时反应①的平衡常数K=1.0,在此温度下2L密闭容器中进行反应①,Fe和CO2的起始量均为2.0mol,达到平衡时CO2的转化率为
50%
50%
(3)将上述平衡体系升温至700℃,再次达到平衡时体系中CO的浓度是CO2浓度的两倍,则a
>
>
0(填“>”、“<”或“=”).为了加快化学反应速率且使体系中CO的物质的量增加,其它条件不变时,可以采取的措施有BC
BC
(填序号).A.缩小反应器体积 B.再通入CO2 C.升高温度 D.使用合适的催化剂
(4)最近一些科学家研究采用高质子导电性的SCY陶瓷(能传递H+)实现氮的固定--氨的电解法合成,大大提高了氮气和氢气的转化率.总反应式为:N2+3H2
| 通电 | 一定条件 |
阳
阳
极(填“正”、“负”、“阴”或“阳”);在另一电极通入N2,该电极反应式为N2+6H++6e-=2NH3
N2+6H++6e-=2NH3
.(5)在25℃下,将a mol?L-1的氨水与0.01mol?L-1的盐酸等体积混合,反应后溶液中c(NH4+)=c(Cl-),则溶液显
中
中
性(填“酸”“碱”或“中”),可推断 a大于
大于
0.01(填大于、等于或小于).为了检验某新型镍催化剂在不同温度下对苯催化加氢的影响.采用微型反应装置,在压强为0.78MPa,氢气和苯的物质的量之比为6.5:1的条件下不断升温,定时取样分析成分:
下列说法正确的是( )
| 温度/℃ | 85 | 90 | 95 | 100 | 200 | 280 | 300 | 320 | 340 |
| 苯(mmol) | 96.05 | 91.55 | 91.30 | 80.85 | 10 | 23.35 | 36.90 | 55.99 | 72.37 |
| 环己烷(mmol) | 3.95 | 8.45 | 8.7 | 19.15 | 90 | 76.65 | 63.10 | 44.01 | 27.63 |
| A、随着反应温度的升高,苯的反应速率先增大后减少 |
| B、通过改变温度或压强能使氢气和苯的转化率相同 |
| C、调控压强、氢气和苯的物质的量之比能提高苯的转化率 |
| D、当温度超过280℃,苯的转化率迅速下降,可能是因为温度过高催化剂活性下降 |
某兴趣小组的同学在探究金属活动性顺序时,决定把铝片放入硫酸铜的水溶液中进行实验,以验证铝和铜的活动性顺序.小组的同学进行了分工,甲同学取一定量的无水硫酸铜粉末加到一定量的蒸馏水中溶解,发现溶液变浑浊,加水稀释仍然浑浊.
(1)你认为是什么原因造成的
(2)请你给出配制此溶液的建议
(3)经过小组讨论后,终于配制成澄清溶液.甲同学截取一段铝片放入盛有该硫酸铜溶液的试管中,观察,一开始无明显现象,一段时间后铝片表面先变
(4)乙同学认为将铝片放入前应
[提出问题]该气体是什么呢?
[猜想]①甲同学认为可能是氢气 ②乙同学认为可能是二氧化硫.
[查资料]铜盐溶液中,溶液的pH决定溶液中Cu2+浓度大小,通过查资料得到如下数据(Cu2+浓度小于1.0×10-5molL-1时忽略不计):
[方案设计]同学们设计方案逐一加以验证:
①
②
[讨论交流]你觉得还可以通过什么操作验证Al和Cu的活动性
查看习题详情和答案>>
(1)你认为是什么原因造成的
硫酸铜水解生成氢氧化铜沉淀
硫酸铜水解生成氢氧化铜沉淀
,写出反应的化学方程式CuSO4+2H2O=Cu(OH)2↓+H2SO4
CuSO4+2H2O=Cu(OH)2↓+H2SO4
.(2)请你给出配制此溶液的建议
取硫酸铜粉末加入少量硫酸再加适量蒸馏水稀释
取硫酸铜粉末加入少量硫酸再加适量蒸馏水稀释
.(3)经过小组讨论后,终于配制成澄清溶液.甲同学截取一段铝片放入盛有该硫酸铜溶液的试管中,观察,一开始无明显现象,一段时间后铝片表面先变
暗
暗
,随后溶液颜色变浅并在铝片表面沉积一层疏松的红色物质.(4)乙同学认为将铝片放入前应
先用砂纸打磨光亮
先用砂纸打磨光亮
,并重做此实验,除发现跟甲同学一样的现象外,还看到有气泡产生,于是激发了他们的探究欲望.[提出问题]该气体是什么呢?
[猜想]①甲同学认为可能是氢气 ②乙同学认为可能是二氧化硫.
[查资料]铜盐溶液中,溶液的pH决定溶液中Cu2+浓度大小,通过查资料得到如下数据(Cu2+浓度小于1.0×10-5molL-1时忽略不计):
| Cu2+/molL-1 | 0.1 | 0.01 | 0.001 | 0.0001 | 0.00001 |
| 溶液pH | 4.7 | 5.2 | 5.7 | 6.2 | 6.7 |
①
将产生的气体收集到小试管中,做爆鸣气实验
将产生的气体收集到小试管中,做爆鸣气实验
;②
将产生的气体通入品红溶液汇总,观察是否褪色
将产生的气体通入品红溶液汇总,观察是否褪色
.[讨论交流]你觉得还可以通过什么操作验证Al和Cu的活动性
分别取铜片和铝片,加入稀盐酸中观察
分别取铜片和铝片,加入稀盐酸中观察
.(1)2009年,长春应用化学研究所在甲醇燃料电池技术上获得新突破,原理如图所示.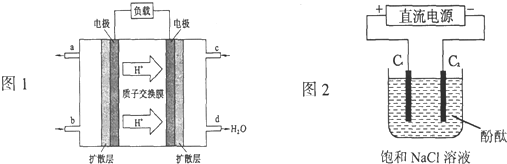
①请写出从C口通入O2发生的电极反应式
②以石墨电极电解饱和食盐水,电解开始后在
(2)合成氨所需的氢气可用煤和水作原料经多步反应制得,其中的一步反应为:CO(g)+H2O(g)?CO2(g)+H2(g)△H<0,200℃时,该反应的平衡常数为1/2.25,该温度下,将一定量的CO和H2O 投入某10L密闭容器,5min时达平衡,各物质浓度(mol?L-1)变化如下:
①请分别计算CO和CO2的平衡浓度
②CO的平衡转化率为
a.增加压强 b.降低温度 c.体积不变,再充入CO d.更换催化剂 e.体积不变,再充入0.1molH2O
③若5min~10min只改变了某一条件,该条件是
查看习题详情和答案>>

①请写出从C口通入O2发生的电极反应式
O2+4e-+4H+=2H2O
O2+4e-+4H+=2H2O
.②以石墨电极电解饱和食盐水,电解开始后在
阴极
阴极
的周围(填“阴极”或“阳极”)先出现红色.假设电池的理论效率为80%(电池的理论效率是指电池产生的最大电能与电池反应所释放的全部能量之比),若消耗6.4g甲醇气体,外电路通过的电子个数为5.8×1023
5.8×1023
(保留两位有效数字).(2)合成氨所需的氢气可用煤和水作原料经多步反应制得,其中的一步反应为:CO(g)+H2O(g)?CO2(g)+H2(g)△H<0,200℃时,该反应的平衡常数为1/2.25,该温度下,将一定量的CO和H2O 投入某10L密闭容器,5min时达平衡,各物质浓度(mol?L-1)变化如下:
| 0min | 5min | 10min | |
| CO | 0.01 | 0.0056 | |
| H2O | 0.01 | 0.0156 | |
| CO2 | 0 | 0.0044 | |
| H2 | 0 | 0.0044 |
0.006 mol?L-1
0.006 mol?L-1
,0.004 mol?L-1
0.004 mol?L-1
.②CO的平衡转化率为
40%
40%
,欲提高CO的转化率,下列措施中可行的是be
be
(填序号).a.增加压强 b.降低温度 c.体积不变,再充入CO d.更换催化剂 e.体积不变,再充入0.1molH2O
③若5min~10min只改变了某一条件,该条件是
H2O的浓度
H2O的浓度
,如何改变的增大了0.01 mol?L-1
增大了0.01 mol?L-1
.