摘要:D+E:产生白色沉淀和刺激性气味气体.沉淀不溶于稀硝酸. 试根据上述实验现象推断A.B.C.D.E的化学式.写出各步反应的离子方程式. [解析]本题有一定难度.若阴.阳离子逐个组合.验证.最终也能得出结论.但绝不可取.必须全面分析.兵分六路率先突破.实验1.4都生成不溶于稀硝酸的白色沉淀.这两种沉淀不外乎是AgCl和BaSO4.D与E反应还生成刺激性气味的气体.显然是氨气.若沉淀是AgCl.则可溶性银盐只能是AgNO3.那么另一种就是NH4Cl.但AgNO3与NH4Cl反应不可能有氨气逸出.因此.实验1.4生成的沉淀分别只能是AgCl和BaSO4. 进一步推出.A.B中须有一种是AgNO3.另一种是氯化物,D.E中必有一种是(NH4)2SO4.根据阴离子组合.另一种只能是Ba(OH)2.且D不可能是(NH4)2SO4.因为找不到另一种金属离子(Ag+离子已排除)与SO42-离子结合生成不溶于稀硝酸的白色沉淀.因此.D只能是Ba(OH)2.E是(NH4)2SO4.余下的推断就不难进行了. 故本题的正确答案是:A是AgNO3.B是AlCl3.C是Na2CO3.D是Ba(OH)2.E是(NH4)2SO4.上述各步反应的离子方程式为:
网址:http://m.1010jiajiao.com/timu3_id_350279[举报]
下图中,A、D为气体非金属单质,N、P是金属单质;M为红褐色沉淀;B、E为有刺激性气味的气体;通常状况下,Z为液体;C是由三咱短周期非金属元素组成的离子化合物;I、L为白色沉淀.反应②、⑥均可用于实验室制取某种常见气体;工业上以D为原料生产B(图中部分反应物和生成物没有列出).
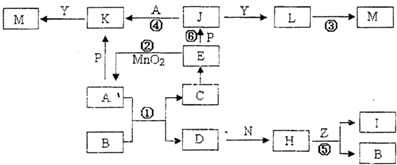
请按要求回答:
(1)写出D的结构式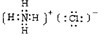
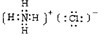 ;H的电子式
;H的电子式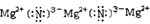
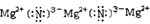 .
.
(2)上述①--⑥反应中属于氧化还原反应的有
用于除去K溶液中含有的少量J(填写序号).
(3)反应②的离子方程式为了
实验室制B的化学方程式为
(4)生活中K可用作净水剂,用离子方程式表示其原理
(5)写出A、M和氢氧化钾在一定条件下反应生成K2PO4(P为题中P物质的元素符号,答题时用所对应的元素符号表示)
查看习题详情和答案>>

请按要求回答:
(1)写出D的结构式
N≡N
N≡N
,C的电子式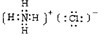
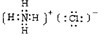
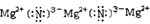
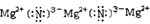
(2)上述①--⑥反应中属于氧化还原反应的有
①②③④⑥
①②③④⑥
(填写序号),其中反应④
④
可用于除去K溶液中含有的少量J(填写序号).
(3)反应②的离子方程式为了
4H++MnO2
Cl2↑+Mn2++2H2O
| ||
4H++MnO2
Cl2↑+Mn2++2H2O
.
| ||
实验室制B的化学方程式为
Ca(OH)2+2NH4Cl
CaCl2+2NH3↑+2H2O
| ||
Ca(OH)2+2NH4Cl
CaCl2+2NH3↑+2H2O
.
| ||
(4)生活中K可用作净水剂,用离子方程式表示其原理
Fe3++3H2O
Fe(OH)3(胶体)+3H+
| ||
Fe3++3H2O
Fe(OH)3(胶体)+3H+
.
| ||
(5)写出A、M和氢氧化钾在一定条件下反应生成K2PO4(P为题中P物质的元素符号,答题时用所对应的元素符号表示)
3Cl2+2Fe(OH)3+10KOH
2K2FeO4+6KCl
| ||
3Cl2+2Fe(OH)3+10KOH
2K2FeO4+6KCl
.
| ||
下图中,A、D为气体非金属单质,N、P是金属单质;M为红褐色沉淀;B、E为有刺激性气味的气体;通常状况下,Z为液体;C是由三咱短周期非金属元素组成的离子化合物;I、L为白色沉淀.反应②、⑥均可用于实验室制取某种常见气体;工业上以D为原料生产B(图中部分反应物和生成物没有列出).

请按要求回答:
(1)写出D的结构式______,C的电子式______;H的电子式______.
(2)上述①--⑥反应中属于氧化还原反应的有______(填写序号),其中反应______可
用于除去K溶液中含有的少量J(填写序号).
(3)反应②的离子方程式为了______.
实验室制B的化学方程式为______.
(4)生活中K可用作净水剂,用离子方程式表示其原理______.
(5)写出A、M和氢氧化钾在一定条件下反应生成K2PO4(P为题中P物质的元素符号,答题时用所对应的元素符号表示)______.
查看习题详情和答案>>
下图中,A、D为气体非金属单质,N、P是金属单质;M为红褐色沉淀;B、E为有刺激性气味的气体;通常状况下,Z为液体;C是由三咱短周期非金属元素组成的离子化合物;I、L为白色沉淀.反应②、⑥均可用于实验室制取某种常见气体;工业上以D为原料生产B(图中部分反应物和生成物没有列出).
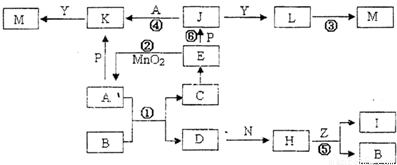
请按要求回答:
(1)写出D的结构式______,C的电子式______;H的电子式______.
(2)上述①--⑥反应中属于氧化还原反应的有______(填写序号),其中反应______可
用于除去K溶液中含有的少量J(填写序号).
(3)反应②的离子方程式为了______ Cl2↑+Mn2++2H2O 查看习题详情和答案>>

请按要求回答:
(1)写出D的结构式______,C的电子式______;H的电子式______.
(2)上述①--⑥反应中属于氧化还原反应的有______(填写序号),其中反应______可
用于除去K溶液中含有的少量J(填写序号).
(3)反应②的离子方程式为了______ Cl2↑+Mn2++2H2O 查看习题详情和答案>>
常见的非金属黄色晶体单质A与常见金属单质B,在加热条件下反应生成化合物C,C与水反应生成白色沉淀D和气体E,D既能溶于强酸,也能溶于强碱.E在足量空气中燃烧产生刺激性气体G,G在大气中能导致酸雨的形成.E被足量氢氧化钠溶液吸收得到无色溶液F.溶液F在空气中长期放置与氧气发生反应,溶液呈强碱性,生成物之一为H.H的组成元素与F相同,其结构和化学性质与过氧化钠相似,溶液显黄色.请回答下列问题:
(1)B与氢氧化钠溶液反应的化学方程式为:
(2)G与氯酸钠在酸性条件下反应可生成消毒杀菌剂二氧化氯.该反应的氧化产物为
(3)溶液F在空气中长期放置生成H的化学反应方程式为:
(4)H的溶液与稀硫酸反应产生的现象为
查看习题详情和答案>>
(1)B与氢氧化钠溶液反应的化学方程式为:
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
.(2)G与氯酸钠在酸性条件下反应可生成消毒杀菌剂二氧化氯.该反应的氧化产物为
硫酸钠(Na2SO4)
硫酸钠(Na2SO4)
,当生成2mol二氧化氯时,转移电子2
2
mol.(3)溶液F在空气中长期放置生成H的化学反应方程式为:
4Na2S+O2+2H2O=4NaOH+2Na2S2(或2Na2S+O2+2H2O=4NaOH+2S,Na2S+S=Na2S2)
4Na2S+O2+2H2O=4NaOH+2Na2S2(或2Na2S+O2+2H2O=4NaOH+2S,Na2S+S=Na2S2)
.(4)H的溶液与稀硫酸反应产生的现象为
溶液由黄色变为无色,产生浅黄色沉淀和(臭鸡蛋气味的)气体
溶液由黄色变为无色,产生浅黄色沉淀和(臭鸡蛋气味的)气体
.下图涉及的物质所含元素中,除一种元素外,其余均为短周期元素.已知:A、F为无色气体单质,B为具有刺激性气味的气体,C为黑色氧化物,E为红色金属单质(部分反应的产物未列出).请回答下列问题:

(1)B的电子式为
 ;
;
(2)写出B和C反应的化学方程式
(3)写出E与G的稀溶液的离子方程式,并标出电子转移数目:
 ;
;
(4)J、K均是同种金属的氯化物,且K为白色沉淀.写出SO2还原J生成K的离子方程式
(5)汽车尾气中常含有D和CO,二者在催化剂作用下可以大部分转化为两种对空气无污染的物质,已知:F(g)+A(g)=2D (g)△H=+180.5KJ/mol
2C (s)+O2 (g)=2CO(g)△H=-221.0KJ/mol
C (s)+O2(g)=CO2(g)△H=-393.5KJ/mol
则上述尾气转化的热化学方程式为:
查看习题详情和答案>>

(1)B的电子式为


(2)写出B和C反应的化学方程式
3CuO+2NH3
3Cu+N2+3H2O
| ||
3CuO+2NH3
3Cu+N2+3H2O
;
| ||
删除此空
删除此空
(3)写出E与G的稀溶液的离子方程式,并标出电子转移数目:


(4)J、K均是同种金属的氯化物,且K为白色沉淀.写出SO2还原J生成K的离子方程式
2Cu2++2Cl-+SO2+2H2O=2CuCl↓+4H++SO42-
2Cu2++2Cl-+SO2+2H2O=2CuCl↓+4H++SO42-
;(5)汽车尾气中常含有D和CO,二者在催化剂作用下可以大部分转化为两种对空气无污染的物质,已知:F(g)+A(g)=2D (g)△H=+180.5KJ/mol
2C (s)+O2 (g)=2CO(g)△H=-221.0KJ/mol
C (s)+O2(g)=CO2(g)△H=-393.5KJ/mol
则上述尾气转化的热化学方程式为:
2NO(g)+2CO(g)=N2(g)+2CO2(g)△H=-746.5KJ/mol
2NO(g)+2CO(g)=N2(g)+2CO2(g)△H=-746.5KJ/mol
.