网址:http://m.1010jiajiao.com/timu3_id_347223[举报]
A.把SO2通入紫色石蕊试液,可验证SO2的漂白性
B.一学生用pH试纸测得某氯水的pH为2
C.不宜用瓷坩埚灼烧氢氧化钠或碳酸钠
D.将10g ZnSO4?7H2O溶解在90g水中配制10%的ZnSO4溶液
E.向某溶液中滴加氯化钡溶液,产生不溶于稀硝酸的白色沉淀,则该溶液中一定含有SO2-4
F.配制一定物质的量浓度的溶液,定容时俯视容量瓶的刻度线,会使所配溶液浓度偏高
(II)(二氯化硫(SCl2)熔点-78℃,沸点59℃.密度1.638g/mL.遇水易分解二氯化硫与三氧化硫作用可生成重要化工试剂亚硫酰氯(SOCl2).以下是由氯气与硫反应合成二氯化硫的实验装置.

回答下列问题:
(1)装置B盛放的药品是
(2)实验开始前先在D中放入一定量的硫粉,加热使硫熔化,然后转动和摇动烧瓶使硫附着在烧瓶内壁表面形成一薄层,这样做的目的是
(3)实验时,D装置需加热至50-59℃,最好采用何种方式加热
(4)F装置中干燥管内所盛物质是
试回答下列问题:

(1)装置A中发生反应的化学方程式为:
| ||
| ||
(2)装置C中盛放的试剂是
(3)实验开始前先排尽系统中空气,此做法目的是
(4)实验时,如何防止E中液体挥发
(5)画出虚线框内与F连接的仪器,并指出其中盛装试剂名称,以完善该实验装置.

回答下列问题:
(1)B中发生反应的离子方程式为_____________________。
(2)C中盛放的试剂是______________,D中试剂的作用是________________________。
(3)实验开始前,先在E中放入一定量的硫粉,加热至
(4)E中发生反应的化学方程式为________________________。
(5)二氯化硫与三氧化硫在一定条件下反应生成亚硫酰氯,并生成一种大气污染物。写出发生反应的化学方程式____________________________________。
(6)上述实验装置中,有一个明显不完善之处需要改进或补充,请简述改进或补充的措施________________________。
查看习题详情和答案>>(12分)二氯化硫(SCl2)熔点—78oC,沸点59 oC,密度1.638g/cm3,遇水易分解,以下是由氯气与硫反应合成二氯化硫的实验装置,其中F中装有无水CaCl2固体。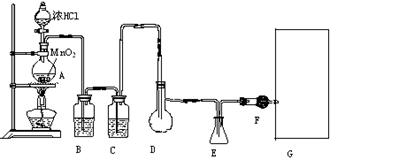
试回答下列问题:
(1)装置A中发生反应的化学方程式为: 
(2)装置C中盛放的试剂是 ,装置F的作用为
(3)实验开始前先排尽系统中空气,此做法目的是
再向D中放入一定量的硫粉,加热使之融化,然后摇动烧瓶使硫附着在烧瓶内壁形成一薄层膜,这样做的目的是
(4)实验时,如何防止E中液体挥发
(5)画出虚线框内与F连接的仪器,并指出其中盛装试剂名称,以完善该实验装置
二氯化硫(SCl2)熔点-78℃,沸点59℃,密度1.638g/mL,遇水易分解,二氯化硫与三氧化硫作用可生成重要化工试剂亚硫酰氯(SOCl2)。以下是氯气与硫合成二氯化硫的实验装置。
试回答下列问题:

(1)装置A中发生反应的化学方程式为 。
(2)装置B、C应盛放的药品分别是 、 。
(3)实验开始前先在D中放一定量的硫粉.加热使硫熔化,然后转动和摇动烧瓶使硫附着在烧瓶内壁形成一薄层表面,这样做的目的是 。
(4)实验时,D装置需加热至50—59℃.最好采用的措施是 、如何防止E中液体挥发? 。
(5)F装置中干燥管内所盛物质是 ,作用是 。
(6)由二氯化硫与SO3作用生成亚硫酰氯的化学方程式为 。
查看习题详情和答案>>