摘要:一般说, 含碳量在 的铁合金叫生铁, 含碳量在 的铁合金叫钢.把铁 矿石炼成生铁的主要原理是 .炼钢的主要原理是 .
网址:http://m.1010jiajiao.com/timu3_id_346754[举报]
粗盐中除含有钙离子、镁离子、硫酸根离子等可溶性杂质外,还含有泥沙等不溶性杂质,我们食用的精盐是用粗食盐提纯而得到的。通过教材中“粗盐的提纯”及你做过的该实验回答下列问题:
(1)实验室进行NaCl溶液蒸发时,一般有以下操作过程:①放置酒精灯;②固定铁圈位置;③放上蒸发皿(蒸发皿中盛有NaCl溶液);④加热搅拌;⑤停止加热。其正确的操作为__________________________________________________。
(2)如何运用最简单的方法检验溶液中有无![]() ?_______________________________。如果有,应该如何除去
?_______________________________。如果有,应该如何除去![]() ?____________________________________________________。
?____________________________________________________。
(3)在粗盐经过溶解、过滤后的溶液中滴加饱和Na2CO3溶液,直至不再产生沉淀为止。这步操作的目的是__________________________________。
(4)将经过操作(3)后的溶液过滤。这一步操作能除掉哪些杂质?__________________。
(5)实验室里将粗盐制成精盐的过程中,在溶解、过滤、蒸发三个步骤的操作中都要用到玻璃棒,分别说出在这三种情况下使用玻璃棒的目的:
溶解时:_______________________________________________________________;
过滤时:_______________________________________________________________;
蒸发时:_______________________________________________________________。
查看习题详情和答案>>(1)通过实验测定H2O2溶液中H2O2的质量分数:
①用 (填仪器名称)量取5.00mL H2O2溶液(密度为1.00g?mL-1)置于锥形瓶中加水稀释,再加稀硫酸酸化:
②用0.1000mol?L-1KMnO4溶液滴定,MnO
被还原成Mn2+,反应的离子方程式为 .如何判断滴定终点: ③用相同的方法滴定三次,消耗的KMnO4溶液的体积分别为20.00mL、19.98mL、20.02mL.则H2O2溶液中溶质的质量分数为
(2)在实验室里制取某些有毒气体时,为了尽量防止毒气逸散造成空气污染,有人设计了如下图所示的装置[Ⅰ].并设想用装置[Ⅱ]或装置[Ⅲ]两种简易装置代替装置[Ⅰ]的b~c部分,以求达到同样的目的.
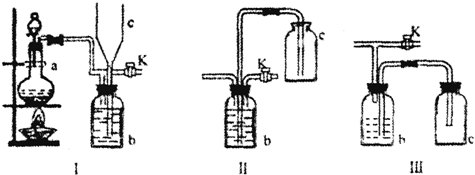
试回答:
①若用装置[Ⅰ]制取氯气,b瓶加入的液体一般为 .在选取试剂正确且适量的前题下,反应开始后,当关闭活塞K时如若发现c中液面上升不明显,你分析可能的原因是 ,检查的简单方法是
②装置[Ⅰ]中b能防止多余气体逸散的原因是:
③欲用装置[Ⅱ]或装置[Ⅲ]代替装置[Ⅰ]中的b~c部分(选用液体相同),是否可行?说明理由.
装置[Ⅱ]是否可行(填“是”或“否”) 理由是
装置[Ⅲ]是否可行(填“是”或“否”) 理由是 .
查看习题详情和答案>>
①用
②用0.1000mol?L-1KMnO4溶液滴定,MnO
- 4 |
(2)在实验室里制取某些有毒气体时,为了尽量防止毒气逸散造成空气污染,有人设计了如下图所示的装置[Ⅰ].并设想用装置[Ⅱ]或装置[Ⅲ]两种简易装置代替装置[Ⅰ]的b~c部分,以求达到同样的目的.

试回答:
①若用装置[Ⅰ]制取氯气,b瓶加入的液体一般为
②装置[Ⅰ]中b能防止多余气体逸散的原因是:
③欲用装置[Ⅱ]或装置[Ⅲ]代替装置[Ⅰ]中的b~c部分(选用液体相同),是否可行?说明理由.
装置[Ⅱ]是否可行(填“是”或“否”)
装置[Ⅲ]是否可行(填“是”或“否”)
下列框图所示的转化关系中,A、C均为常见的金属单质,A、C在冷的H的浓溶液中均会发生钝化;E为固体非金属单质.B为红色固体氧化物,X为常见无色液体.L焰色为黄色,且能使酚酞变红(反应过程中生成的水及其他产物已略去).

请回答以下问题:
(1)含碳量在0.04%~2.3%之间的C的合金,是目前世界上使用量最大的合金,这种合金是
A.铝合金 B.青铜 C.生铁 D.钢
(2)检验上述黄色溶液中阳离子的方法是
(3)I与氯气反应的离子方程式为
(4)A与B应生成C和D的化学方程式为
(5)D与L反应的化学方程式为
查看习题详情和答案>>

请回答以下问题:
(1)含碳量在0.04%~2.3%之间的C的合金,是目前世界上使用量最大的合金,这种合金是
D
D
.A.铝合金 B.青铜 C.生铁 D.钢
(2)检验上述黄色溶液中阳离子的方法是
取样,滴加KSCN溶液,溶液呈血红色,则黄色溶液中阳离子为Fe3+
取样,滴加KSCN溶液,溶液呈血红色,则黄色溶液中阳离子为Fe3+
.(3)I与氯气反应的离子方程式为
2Fe2++Cl2=2Fe3++2Cl-
2Fe2++Cl2=2Fe3++2Cl-
.(4)A与B应生成C和D的化学方程式为
Fe2O3+2Al
A12O3+2Fe
| ||
Fe2O3+2Al
A12O3+2Fe
.
| ||
(5)D与L反应的化学方程式为
Al2O3+2NaOH=2NaAlO2+H2O
Al2O3+2NaOH=2NaAlO2+H2O
.下列框图所示的转化关系中,A、C均为常见的金属单质,A、C在冷的H的浓溶液中均会发生钝化;E为工业制取硫酸中某种矿物的主要成分.B为红棕色固体氧化物,X为常见无色液体.L焰色为黄色,且能使酚酞变红(反应过程中生成的水及其他产物已略去).

请回答以下问题:
(1)含碳量在0.04%~2.3%之间的C的合金,是目前世界上使用量最大的合金,这种合金是
A.铝合金 B.青铜 C.生铁 D.钢
(2)检验上述黄色溶液中阳离子的方法是
(3)I与氯气反应的离子方程式为
(4)A与B应生成C和D的化学方程式为
(5)D与L反应的化学方程式为
(6)E与O2反应的化学方程式为
查看习题详情和答案>>

请回答以下问题:
(1)含碳量在0.04%~2.3%之间的C的合金,是目前世界上使用量最大的合金,这种合金是
D
D
.A.铝合金 B.青铜 C.生铁 D.钢
(2)检验上述黄色溶液中阳离子的方法是
取样,滴加KSCN溶液,溶液呈血红色,则黄色溶液中阳离子为Fe3+
取样,滴加KSCN溶液,溶液呈血红色,则黄色溶液中阳离子为Fe3+
.(3)I与氯气反应的离子方程式为
2Fe2++Cl2=2Fe3++2Cl-
2Fe2++Cl2=2Fe3++2Cl-
.(4)A与B应生成C和D的化学方程式为
Fe2O3+2Al
Al2O3+2Fe
| ||
Fe2O3+2Al
Al2O3+2Fe
.
| ||
(5)D与L反应的化学方程式为
Al2O3+2NaOH=2NaAlO2+H2O
Al2O3+2NaOH=2NaAlO2+H2O
.(6)E与O2反应的化学方程式为
4FeS2+11O2
2Fe2O3+4SO2
| ||
4FeS2+11O2
2Fe2O3+4SO2
.
| ||