摘要:20℃时在水中的溶解度为25g.将32g白色粉末加入mg水中形成饱和溶液并有·晶体析出.则m的取值范围是 A.18g≤m≤128g B.36g<m<180g C.18g<m<128g D.36g≤m≤180g
网址:http://m.1010jiajiao.com/timu3_id_344853[举报]
一氯甲烷的某些物理数据如下表:
在实验室里可用下图装置制备一氯甲烷:
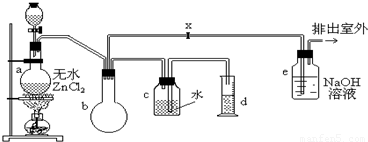
制备装置的分液漏斗中盛有甲醇,烧瓶中盛有浓盐酸.
请填写下列空白:
(1)制备一氯甲烷的化学方程式是______;该反应属于______反应.
(2)装置e中可能发生反应的化学方程式是______.
(3)检验气体产物CH3Cl的方法是:在e的逸出口点燃CH3Cl气体,火焰呈蓝绿色(与其它烃的燃烧现象有明显区别,且生成物中有HCl).CH3Cl燃烧的化学方程式是______.
(4)装置b的作用是______.某学生在关闭活塞x的情况下做此实验时发现,收集到一定体积的气体产物所消耗的甲醇和浓盐酸的量比理论计算的量多(装置的气密性没有问题),其原因是______.实验结束后,d中收集到的液体中含有______.
查看习题详情和答案>>
| 熔点 ℃ | 沸点 ℃ | 液态时 密度 g/cm3 | 18℃时在水中的溶解度 mL/L | 乙醚、丙酮 或苯中的 溶解性 | 乙醇 中的 溶解性 |
| -97.73 | -24.2 | 0.9159 | 280 | 互溶 | 能溶 |

制备装置的分液漏斗中盛有甲醇,烧瓶中盛有浓盐酸.
请填写下列空白:
(1)制备一氯甲烷的化学方程式是______;该反应属于______反应.
(2)装置e中可能发生反应的化学方程式是______.
(3)检验气体产物CH3Cl的方法是:在e的逸出口点燃CH3Cl气体,火焰呈蓝绿色(与其它烃的燃烧现象有明显区别,且生成物中有HCl).CH3Cl燃烧的化学方程式是______.
(4)装置b的作用是______.某学生在关闭活塞x的情况下做此实验时发现,收集到一定体积的气体产物所消耗的甲醇和浓盐酸的量比理论计算的量多(装置的气密性没有问题),其原因是______.实验结束后,d中收集到的液体中含有______.
查看习题详情和答案>>
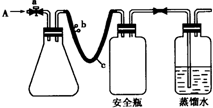 (2012?南通模拟)实验室用下列方法测定某水样中O2的含量.
(2012?南通模拟)实验室用下列方法测定某水样中O2的含量.(1)实验原理
用如图所示装置,使溶解在水中的O2在碱性条件下将Mn2+氧化成MnO(OH)2,反应的离子方程式为
2Mn2++O2+4OH-=2MnO(OH)2
2Mn2++O2+4OH-=2MnO(OH)2
.再用I-将生成的MnO(OH)2还原为Mn2+,反应的离子方程式为:MnO(OH)2+2I-+4H+=Mn2++I2+3H2O.然后用Na2S2O3标准溶液滴定生成的I2,反应方程式为:I2+2Na2S2O3=2NaI+Na2S4O6.(2)实验步骤
①打开止水夹a 和b,从A 处向装置内鼓入过量N2,此操作的目的是
赶走装置内空气,避免空气中的O2的干扰
赶走装置内空气,避免空气中的O2的干扰
;②用注射器抽取某水样20.00mL从A 处注入锥形瓶;
③再分别从A 处注入含m mol NaOH溶液及过量的MnSO4溶液;
④完成上述操作后,关闭a、b,将锥形瓶中溶液充分振荡;
⑤打开止水夹a、b,分别从A 处注入足量NaI溶液,并用稀H2SO4溶液调节pH至接近中性;
⑥
重复④的操作
重复④的操作
;⑦取下锥形瓶,向其中加入2~3滴
淀粉溶液
淀粉溶液
作指示剂;⑧用0.005mol?L-1Na2S2O3 滴定至终点.
(3)数据分析
①若滴定过程中消耗的Na2S2O3 标准溶液体积为3.90mL,则此水样中氧(O2)的含量为
7.8mg?L-1
7.8mg?L-1
(单位:mg?L-1).②若未用Na2S2O3 标准溶液润洗滴定管,则测得水样中O2的含量将
偏大
偏大
(填“偏大”、“偏小”或“不变”).③步骤⑤中加入适量的H2SO4使溶液接近中性,其原因是
加入稀H2SO4使MnO(OH)2充分转化为Mn2+,但加入稀H2SO4的量时不宜过多,否则后续滴定过程中Na2S2O3与过量的酸反应导致消耗的Na2S2O3溶液偏大
加入稀H2SO4使MnO(OH)2充分转化为Mn2+,但加入稀H2SO4的量时不宜过多,否则后续滴定过程中Na2S2O3与过量的酸反应导致消耗的Na2S2O3溶液偏大
.高铁酸钾(K2FeO4)具有极高的氧化性,且其还原产物为铁锈,对环境无不良影响.因该物质具有“绿色”、选择性高、活性强等特点受到人们关注.
I、高铁酸钾制备方法之一为:①在一定温度下,将氯气通入KOH溶液中制得次氯酸钾溶液;②在剧烈搅拌条件下,将Fe(NO3)3分批加入次氯酸钾溶液中,控制反应温度,以免次氯酸钾分解;③加 KOH至饱和,使K2FeO4 充分析出,再经纯化得产品,其纯度在95%以上.
(1)氯碱工业中制备氯气的化学方程式是 ;
(2)温度过高会导致次氯酸钾分解生成两种化合物,产物之一是氯酸钾(KClO3),另一种产物应该是 (写化学式)
(3)制备过程有一步反应如下,请配平此方程式(将计量数填入方框中):
Fe(OH)3+ ClO-+ OH-═ Fe
+ Cl-+ H2O
Ⅱ、为探究高铁酸钾的某种性质,进行如下两个实验:
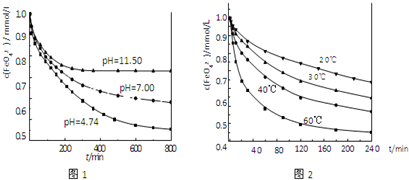
实验1:将适量K2FeO4分别溶解于pH 为 4.74、7.00、11.50 的水溶液中,配得FeO42-浓度为 1.0mmol?L-1(1mmol?L-1=10-3mol?L-1)的试样,静置,考察不同初始 pH 的水溶液对K2FeO4某种性质的影响,结果见图1(注:800min后,三种溶液中高铁酸钾的浓度不再改变).
实验2:将适量 K2FeO4 溶解于pH=4.74 的水溶液中,配制成FeO42-浓度为 1.0mmol?L-1 的试样,将试样分别置于 20℃、30℃、40℃和 60℃的恒温水浴中,考察不同温度对K2FeO4某种性质的影响,结果见图2.
(4)实验1的目的是 ;
(5)实验2可得出的结论是 ;
(6)高铁酸钾在水中的反应为4FeO42-+10H2O?4Fe(OH)3+8OH-+3O2↑.
由图1可知,800min时,pH=11.50的溶液中高铁酸钾最终浓度比pH=4.74的溶液中高,主要原因是 ;
Ⅲ、高铁酸钾还是高能电池的电极材料.例如,Al-K2FeO4电池就是一种高能电池(以氢氧化钾溶液为电解质溶液),该电池放电时负极反应式是 .
查看习题详情和答案>>
I、高铁酸钾制备方法之一为:①在一定温度下,将氯气通入KOH溶液中制得次氯酸钾溶液;②在剧烈搅拌条件下,将Fe(NO3)3分批加入次氯酸钾溶液中,控制反应温度,以免次氯酸钾分解;③加 KOH至饱和,使K2FeO4 充分析出,再经纯化得产品,其纯度在95%以上.
(1)氯碱工业中制备氯气的化学方程式是
(2)温度过高会导致次氯酸钾分解生成两种化合物,产物之一是氯酸钾(KClO3),另一种产物应该是
(3)制备过程有一步反应如下,请配平此方程式(将计量数填入方框中):
| O | 2- 4 |
Ⅱ、为探究高铁酸钾的某种性质,进行如下两个实验:

实验1:将适量K2FeO4分别溶解于pH 为 4.74、7.00、11.50 的水溶液中,配得FeO42-浓度为 1.0mmol?L-1(1mmol?L-1=10-3mol?L-1)的试样,静置,考察不同初始 pH 的水溶液对K2FeO4某种性质的影响,结果见图1(注:800min后,三种溶液中高铁酸钾的浓度不再改变).
实验2:将适量 K2FeO4 溶解于pH=4.74 的水溶液中,配制成FeO42-浓度为 1.0mmol?L-1 的试样,将试样分别置于 20℃、30℃、40℃和 60℃的恒温水浴中,考察不同温度对K2FeO4某种性质的影响,结果见图2.
(4)实验1的目的是
(5)实验2可得出的结论是
(6)高铁酸钾在水中的反应为4FeO42-+10H2O?4Fe(OH)3+8OH-+3O2↑.
由图1可知,800min时,pH=11.50的溶液中高铁酸钾最终浓度比pH=4.74的溶液中高,主要原因是
Ⅲ、高铁酸钾还是高能电池的电极材料.例如,Al-K2FeO4电池就是一种高能电池(以氢氧化钾溶液为电解质溶液),该电池放电时负极反应式是
硫酸亚铁可与等物质的量的硫酸铵生成硫酸亚铁铵:(NH4)2SO4?FeSO4?6H2O,商品名称为莫尔盐,是一种复盐.一般亚铁盐在空气中易被氧气氧化,形成复盐后就比较稳定.与其他复盐一样,硫酸亚铁铵在水中的溶解度比组成它的每一种盐的溶解度都小,且几乎不溶于乙醇,利用这一性质可以制取硫酸亚铁铵晶体.三种盐的溶解度(单位为g/l00gH2O)见下表:
实验用品:Fe屑(含少量碳)、3mol/LH2SO4、( NH4)2SO4、蒸馏水、无水乙醇.
实验步骤流程图:
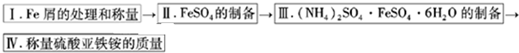
请完成以下实验记录:
(1)步骤I中用10% Na2CO3的热溶液处理铁屑的目的是 ,经处理后的干燥铁屑质量记为m1;
(2)将称量好的Fe屑放入锥形瓶中,加入适量3mol/LH2SO4溶液,放在水浴中加热至气泡量产生较少时为止(有氢气生成,用明火加热注意安全).趁热过滤,并用少量热水洗涤锥形瓶及滤纸,将滤液和洗涤液一起转移至蒸发皿中.将滤纸上的固体常温干燥后称重,记为m2;
(3)称取一定质量的(NH4)2SO4,加入 g(用含m1和m2的代数式表示,要求化简,下同.)水配制成室温下(20℃)的饱和溶液,并将其加入到上面实验的蒸发皿中,缓缓加热,浓缩至表面出现结晶薄膜为止.放置冷却,得到硫酸亚铁铵的晶体,过滤后用 洗涤晶体.
(4)产品纯度的测定
先称取产品1.600g,加水溶解,配成100ml溶液,移取25.00mL待测溶液与锥形瓶中,再用硫酸酸化的0.0100mol/LKMnO4标准溶液进行滴定其中的Fe2+,达到滴定终点时消耗标准液的平均值为20.00mL,则样品中的(NH4)2SO4?FeSO4?6H2O的质量分数?(列式计算) 查看习题详情和答案>>
| 温度/℃ | FeSO4?7H2O | (NH4)2SO4 | (NH4)2SO4?FeSO4?6H2O |
| 10 | 20.0 | 73.0 | 17.2 |
| 20 | 26.5 | 75.4 | 21.6 |
| 30 | 32.9 | 78.0 | 28.1 |
实验步骤流程图:

请完成以下实验记录:
(1)步骤I中用10% Na2CO3的热溶液处理铁屑的目的是
(2)将称量好的Fe屑放入锥形瓶中,加入适量3mol/LH2SO4溶液,放在水浴中加热至气泡量产生较少时为止(有氢气生成,用明火加热注意安全).趁热过滤,并用少量热水洗涤锥形瓶及滤纸,将滤液和洗涤液一起转移至蒸发皿中.将滤纸上的固体常温干燥后称重,记为m2;
(3)称取一定质量的(NH4)2SO4,加入
(4)产品纯度的测定
先称取产品1.600g,加水溶解,配成100ml溶液,移取25.00mL待测溶液与锥形瓶中,再用硫酸酸化的0.0100mol/LKMnO4标准溶液进行滴定其中的Fe2+,达到滴定终点时消耗标准液的平均值为20.00mL,则样品中的(NH4)2SO4?FeSO4?6H2O的质量分数?(列式计算) 查看习题详情和答案>>
下表是几种弱电解质的电离平衡常数、难溶电解质的溶度积Ksp(25℃).
回答下列问题:
(1)由上表分析,若①CH3COOH ②HCO3-③C6H5OH ④H2PO4-均可看作酸,则它们酸性由强到弱的顺序为 (须填编号);
(2)写出C6H5OH与Na3PO4反应的离子方程式: ;
(3)25℃时,将等体积等浓度的醋酸和氨水混合,混合液中:c(CH3COO-) c(NH4+);(填“>”、“=”或“<”)
(4)25℃时,向10ml 0.01mol/L苯酚溶液中滴加Vml 0.01mol/L氨水,混合溶液中粒子浓度关系正确的是 ;
A.若混合液pH>7,则V≥10
B.若混合液pH<7,则c(NH4+)>c(C6H5O-)>c(H+)>c(OH-)
C.V=10时,混合液中水的电离程度小于10ml 0.01mol/L苯酚溶液中水的电离程度
D.V=5时,2c(NH3?H2O)+2c(NH4+)=c(C6H5O-)+c(C6H5OH)
(5)水解反应是典型的可逆反应.水解反应的化学平衡常数称为水解常数(用Kh表示),类比化学平衡常数的定义,请写出Na2CO3第一步水解反应的水解常数的表达式 .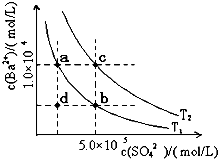
(6)Ⅰ.如图所示,有T1、T2两种温度下两条BaSO4在水中的沉淀溶解平衡曲线,回答下列问题:
①T1 T2(填>、=、<),T2温度时Ksp(BaSO4)= ;
②讨论T1温度时BaSO4的沉淀溶解平衡曲线,下列说法正确的是
A.加入Na2SO4可使溶液由a点变为b点
B.在T1曲线上方区域(不含曲线)任意一点时,均有BaSO4沉淀生成
C.蒸发溶剂可能使溶液由d点变为曲线上a、b之间的某一点(不含a、b)
D.升温可使溶液由b点变为d点
Ⅱ.现有0.2mol的BaSO4沉淀,每次用1L饱和Na2CO3溶液(浓度为1.7mol/L)处理.若使BaSO4中的SO42-全部转化到溶液中,需要反复处理 次.[提示:BaSO4(s)+CO32-(aq)?BaCO3(s)+SO42- (aq)].
查看习题详情和答案>>
| 电解质 | 平衡方程式 | 平衡常数K | Ksp |
| CH3COOH | CH3COOH?CH3COO-+H+ | 1.76×10-5 | |
| H2CO3 | H2CO3?H++HCO3- HCO3-?H++CO32- |
K1=4.31×10-7 K2=5.61×10-11 |
|
| C6H5OH | C6H5OH?C6H5O-+H+ | 1.1×10-10 | |
| H3PO4 | H3PO4?H++H2PO4- H2PO4-?H++HPO42- HPO42-?H++PO43- |
K1=7.52×10-3 K2=6.23×10-8 K3=2.20×10-13 |
|
| NH3?H2O | NH3?H2O?NH4++OH- | 1.76×10-5 | |
| BaSO4 | BaSO4?Ba2++SO42- | 1.07×10-10 | |
| BaCO3 | BaCO3?Ba2++CO32- | 2.58×10-9 |
(1)由上表分析,若①CH3COOH ②HCO3-③C6H5OH ④H2PO4-均可看作酸,则它们酸性由强到弱的顺序为
(2)写出C6H5OH与Na3PO4反应的离子方程式:
(3)25℃时,将等体积等浓度的醋酸和氨水混合,混合液中:c(CH3COO-)
(4)25℃时,向10ml 0.01mol/L苯酚溶液中滴加Vml 0.01mol/L氨水,混合溶液中粒子浓度关系正确的是
A.若混合液pH>7,则V≥10
B.若混合液pH<7,则c(NH4+)>c(C6H5O-)>c(H+)>c(OH-)
C.V=10时,混合液中水的电离程度小于10ml 0.01mol/L苯酚溶液中水的电离程度
D.V=5时,2c(NH3?H2O)+2c(NH4+)=c(C6H5O-)+c(C6H5OH)
(5)水解反应是典型的可逆反应.水解反应的化学平衡常数称为水解常数(用Kh表示),类比化学平衡常数的定义,请写出Na2CO3第一步水解反应的水解常数的表达式

(6)Ⅰ.如图所示,有T1、T2两种温度下两条BaSO4在水中的沉淀溶解平衡曲线,回答下列问题:
①T1
②讨论T1温度时BaSO4的沉淀溶解平衡曲线,下列说法正确的是
A.加入Na2SO4可使溶液由a点变为b点
B.在T1曲线上方区域(不含曲线)任意一点时,均有BaSO4沉淀生成
C.蒸发溶剂可能使溶液由d点变为曲线上a、b之间的某一点(不含a、b)
D.升温可使溶液由b点变为d点
Ⅱ.现有0.2mol的BaSO4沉淀,每次用1L饱和Na2CO3溶液(浓度为1.7mol/L)处理.若使BaSO4中的SO42-全部转化到溶液中,需要反复处理