摘要:某X价的金属元素卤化物的分子量为m.其同价硝酸盐的分子量为n.又知X值为 (m-n)/18.则此卤化物中卤素是 A.氟 B.氯 C.溴 D.碘
网址:http://m.1010jiajiao.com/timu3_id_344834[举报]
(2011?太原二模)[化学--选物质结构与性质]
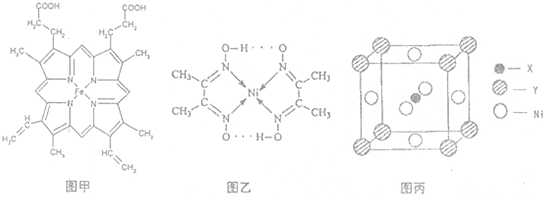
(1)如图甲,血红素含有C、H、O、N、Fe五种元素,C、H、N、O四种元素的电负性由小到大的顺序是
(2)卤素化学丰富多彩,能形成卤化物、卤素互化物、多卤化物等多种类型的化合物.Cl2、IBr、ICl沸点由高到低的顺序为
①HClO4、②HIO4、③HIO6[可写成(HO)5IO]的酸性由强到弱的顺序为
(3)目前,全世界镍的消费量仅次于铜、铝、铅、锌,居有色金属第五位.配合物Ni(CO)4常温为流态,易溶于CCl4、苯等有机溶剂,固态Ni(CO)4属于
A.氢键 B.离子键 C.范德华力 D.配位键
(4)最近发现,只含X、Y和Ni三种元素的某种晶体具有超导性.X元素原子的2p能级的电子排布图为 ,Y元素原子的价电子排布式为3s2,该晶体的一个晶胞如图丙所示,则该晶体的化学式为
,Y元素原子的价电子排布式为3s2,该晶体的一个晶胞如图丙所示,则该晶体的化学式为
查看习题详情和答案>>

(1)如图甲,血红素含有C、H、O、N、Fe五种元素,C、H、N、O四种元素的电负性由小到大的顺序是
H<C<N<O
H<C<N<O
,根据以上电负性请判断H2N-CHO中C和N的化合价分别为+2
+2
和-3
-3
.基态Fe原子的核外电子排布式为1s22s22p63s23p63d64s2或[Ar]3d64s2
1s22s22p63s23p63d64s2或[Ar]3d64s2
.血红素中两种N原子的杂化方式分别为sp2
sp2
、sp3
sp3
.(2)卤素化学丰富多彩,能形成卤化物、卤素互化物、多卤化物等多种类型的化合物.Cl2、IBr、ICl沸点由高到低的顺序为
BrI>ICl>Cl2
BrI>ICl>Cl2
.I+3(可看成II+2)属于多卤素阳离子,根据VSEPR模型推测I+3的空间构型为V形
V形
.多卤化物RbICl2加热时会分解为晶格能相对较大的卤化物A和卤素互化物或卤素单质,则A的化学式为RbCl
RbCl
.①HClO4、②HIO4、③HIO6[可写成(HO)5IO]的酸性由强到弱的顺序为
①②③
①②③
(填序号).(3)目前,全世界镍的消费量仅次于铜、铝、铅、锌,居有色金属第五位.配合物Ni(CO)4常温为流态,易溶于CCl4、苯等有机溶剂,固态Ni(CO)4属于
分子
分子
晶体.如图乙配合物分子内的作用力除共价键外,还存在的两种作用力是AD
AD
(填字母编号).A.氢键 B.离子键 C.范德华力 D.配位键
(4)最近发现,只含X、Y和Ni三种元素的某种晶体具有超导性.X元素原子的2p能级的电子排布图为
 ,Y元素原子的价电子排布式为3s2,该晶体的一个晶胞如图丙所示,则该晶体的化学式为
,Y元素原子的价电子排布式为3s2,该晶体的一个晶胞如图丙所示,则该晶体的化学式为MgCNi3
MgCNi3
.
| |||||||||||||||||||
[化学--选物质结构与性质]

(1)如图甲,血红素含有C、H、O、N、Fe五种元素,C、H、N、O四种元素的电负性由小到大的顺序是______,根据以上电负性请判断H2N-CHO中C和N的化合价分别为______和______.基态Fe原子的核外电子排布式为______.血红素中两种N原子的杂化方式分别为______、______.
(2)卤素化学丰富多彩,能形成卤化物、卤素互化物、多卤化物等多种类型的化合物.Cl2、IBr、ICl沸点由高到低的顺序为______.I+3(可看成II+2)属于多卤素阳离子,根据VSEPR模型推测I+3的空间构型为______.多卤化物RbICl2加热时会分解为晶格能相对较大的卤化物A和卤素互化物或卤素单质,则A的化学式为______.
①HClO4、②HIO4、③HIO6[可写成(HO)5IO]的酸性由强到弱的顺序为______(填序号).
(3)目前,全世界镍的消费量仅次于铜、铝、铅、锌,居有色金属第五位.配合物Ni(CO)4常温为流态,易溶于CCl4、苯等有机溶剂,固态Ni(CO)4属于______晶体.如图乙配合物分子内的作用力除共价键外,还存在的两种作用力是______(填字母编号).
A.氢键 B.离子键 C.范德华力 D.配位键
(4)最近发现,只含X、Y和Ni三种元素的某种晶体具有超导性.X元素原子的2p能级的电子排布图为

,Y元素原子的价电子排布式为3s2,该晶体的一个晶胞如图丙所示,则该晶体的化学式为______.
查看习题详情和答案>>

(1)如图甲,血红素含有C、H、O、N、Fe五种元素,C、H、N、O四种元素的电负性由小到大的顺序是______,根据以上电负性请判断H2N-CHO中C和N的化合价分别为______和______.基态Fe原子的核外电子排布式为______.血红素中两种N原子的杂化方式分别为______、______.
(2)卤素化学丰富多彩,能形成卤化物、卤素互化物、多卤化物等多种类型的化合物.Cl2、IBr、ICl沸点由高到低的顺序为______.I+3(可看成II+2)属于多卤素阳离子,根据VSEPR模型推测I+3的空间构型为______.多卤化物RbICl2加热时会分解为晶格能相对较大的卤化物A和卤素互化物或卤素单质,则A的化学式为______.
①HClO4、②HIO4、③HIO6[可写成(HO)5IO]的酸性由强到弱的顺序为______(填序号).
(3)目前,全世界镍的消费量仅次于铜、铝、铅、锌,居有色金属第五位.配合物Ni(CO)4常温为流态,易溶于CCl4、苯等有机溶剂,固态Ni(CO)4属于______晶体.如图乙配合物分子内的作用力除共价键外,还存在的两种作用力是______(填字母编号).
A.氢键 B.离子键 C.范德华力 D.配位键
(4)最近发现,只含X、Y和Ni三种元素的某种晶体具有超导性.X元素原子的2p能级的电子排布图为

,Y元素原子的价电子排布式为3s2,该晶体的一个晶胞如图丙所示,则该晶体的化学式为______.