摘要:下列各组溶液由于相互加入的顺序不同.而观察到的实验现象不同的是: A.硫氰化钾 和三氯化铁 B.三氯化铝和浓氨水 C.碳酸氢钠和澄清石灰水 D.稀硝酸银和稀氨水
网址:http://m.1010jiajiao.com/timu3_id_344812[举报]
将下列各组溶液进行相互反应,根据溶液加入的先后顺序和反应过程中出现的现象就能进行鉴别的是
- A.KOH和Al2(SO4)3
- B.稀硫酸和NaHCO3
- C.CaCl2和Na2CO3
- D.Ba(OH)2和NaHSO4
(2008?郑州一模)某一反应体系中存在以下五种物质:Na3AsO3、H2O、I2、Na3AsO4、HI
(1)若水是产物,试用这五种物质组成一个合理的反应方程式,配平并标出电子转移的方向和数目: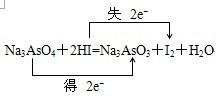
 ;
;
(2)当pH为5~9时,该反应体系中的氧化反应为由HI→I2;当pH<4时,反应向逆反应方向进行,此时体系中的氧化反应为由
(3)物质的氧化性和还原性不仅与溶液的酸碱性有关,还与物质的浓度和反应温度等因素有关.下列各组物质由于浓度不同而发生不同氧化还原反应的是(填序号)
①Cu与HNO3溶液 ②Cu与FeCl3溶液 ③Fe与HCl溶液 ④Zn与H2SO4溶液.
查看习题详情和答案>>
(1)若水是产物,试用这五种物质组成一个合理的反应方程式,配平并标出电子转移的方向和数目:


(2)当pH为5~9时,该反应体系中的氧化反应为由HI→I2;当pH<4时,反应向逆反应方向进行,此时体系中的氧化反应为由
Na3AsO3
Na3AsO3
→Na3AsO4
Na3AsO4
.如果两种情况下反应中转移电子数相等,则两个反应中氧化剂的物质的量之比是1:1
1:1
;(3)物质的氧化性和还原性不仅与溶液的酸碱性有关,还与物质的浓度和反应温度等因素有关.下列各组物质由于浓度不同而发生不同氧化还原反应的是(填序号)
①④
①④
.①Cu与HNO3溶液 ②Cu与FeCl3溶液 ③Fe与HCl溶液 ④Zn与H2SO4溶液.