摘要:9.图30-1两个装置中.溶液体积均为200ml.开始时.电解质溶液的浓度均为0.1mol·.工作一段时间后.测得导线上都通过了0.02mol.若不考虑溶液体积的变化.则下列叙正 确的是( ) 图30-1 A.产生气体体积:①=② B.电极上析出固体质量:①<② C.电极反应式:①中阳极:②中负极: D.溶液的pH变化:①减小,②增大
网址:http://m.1010jiajiao.com/timu3_id_344639[举报]
 (2008?北京)X、Y、Z、W为含有相同电子数的分子或离子,均由原子序数小于10的元素组成,X有5个原子核.通常状况下,W为无色液体.
(2008?北京)X、Y、Z、W为含有相同电子数的分子或离子,均由原子序数小于10的元素组成,X有5个原子核.通常状况下,W为无色液体.已知:X+Y
| △ |
(1)Y的电子式是


(2)液态Z和W的电离相似,都可电离出电子数相同的两种离子,液态Z的电离方程式是
2NH3(l)?NH2-+NH4+
2NH3(l)?NH2-+NH4+
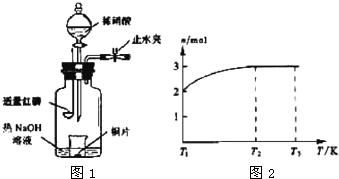
.(3)用图1所示装置制备NO并验证其还原性.有下列主要操作:
a.向广口瓶内注入足量热NaOH溶液,将盛有铜片的小烧杯放入瓶中.
b.关闭止水夹,点燃红磷,伸入瓶中,塞好胶塞.
c.待红磷充分燃烧,一段时间后打开分液漏斗旋塞,向烧杯中滴入少量稀硝酸.
①步骤c后还缺少的一步主要操作是
打开止水夹,通入少量氧气
打开止水夹,通入少量氧气
.②红磷充分燃烧的产物与NaOH溶液反应的离子方程式是
P2O5+6OH-=2PO43-+3H2O
P2O5+6OH-=2PO43-+3H2O
.③步骤c滴入稀硝酸后烧杯中的现象是
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
,反应的离子方程式是Cu片逐渐溶解,有无色气泡产生,溶液由无色变为蓝色
Cu片逐渐溶解,有无色气泡产生,溶液由无色变为蓝色
.(4)一定温度下,将1mol N2O4置于密闭容器中,保持压强不变,升高温度至T1的过程中,气体由无色逐渐变为红棕色.温度由T1继续升高到T2的过程中,气体逐渐变为无色.若保持T2,增大压强,气体逐渐变为红棕色.气体的物质的量n随温度T变化的关系如图2所示.
①温度在T1-T2之间,反应的化学方程式是
2NO2?2NO+O2
2NO2?2NO+O2
.②温度在T2-T3之间,气体的平均相对分子质量是(保留1位小数)
30.7
30.7
. 水合肼作为一种重要的精细化工原料,在农药、医药及有机合成中有广泛用途. 用尿素法制备水合肼,可分为两个阶段,第一阶段为低温氯化阶段,第二阶段为高温水解阶段,总反应方程式为:(NH2)2CO+NaClO+2NaOH→H2N-NH2?H2O+NaCl+Na2CO3.
水合肼作为一种重要的精细化工原料,在农药、医药及有机合成中有广泛用途. 用尿素法制备水合肼,可分为两个阶段,第一阶段为低温氯化阶段,第二阶段为高温水解阶段,总反应方程式为:(NH2)2CO+NaClO+2NaOH→H2N-NH2?H2O+NaCl+Na2CO3.主要副反应:N2H4+2NaClO=N2↑+2H2O+2NaCl△H<0,3NaClO=2NaCl+NaClO3△H>0,CO(NH2)2+2NaOH=2NH3↑+Na2CO3△H>0
【深度氧化】:(NH2)2CO+3NaClO=N2↑+3NaCl+CO2↑+2H2O△H<0
实验步骤:
步骤1.向30%的NaOH溶液中通入Cl2,保持温度在30℃以下,至溶液显浅黄绿色停止通Cl2.
步骤2.静置后取上层清液,检测NaCl0的浓度.
步骤3.倾出上层清液,配制所需浓度的NaClO和NaOH的混合溶液.
步骤4.称取一定质量尿素配成溶液,置于冰水浴.将一定体积步骤3配得的溶液倒入分液漏斗中,慢慢滴加到尿素溶液中,0.5h左右滴完后,继续搅拌0.5h.
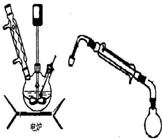
步骤5.将步骤4所得溶液,加入5g KMnO4作催化剂,转移到三口烧瓶(装置见图),边搅拌边急速升温,在108℃回流5min.
步骤6.将回流管换成冷凝管,蒸馏,收集( 108~114℃)馏分,得产品.
(1)步骤1温度需要在30℃以下,其主要目的是
(2)步骤2检测NaClO浓度的目的是
a.确定步骤3中需NaCl0溶液体积及NaOH质量
b.确定步骤4中冰水浴的温度范围
c.确定步骤4中称量尿素的质量及所取次氯酸钠溶液体积关系
d.确定步骤5所需的回流时间
(3)尿素法制备水合肼,第一阶段为反应
(4)步骤5必须急速升温,严格控制回流时间,其目的是
(5)已知水合肼在碱性条件下具有还原性(如:N2H4+2I2=N2+4HI).测定水合肼的质量分数可采用下列步骤:
a.准确称取2.000g试样,经溶解、转移、定容等步骤,配制250mL溶液.
b.移取10.00mL于锥形瓶中,加入20mL水,摇匀.
c.用0.1000mol/L碘溶液滴定至溶液出现微黄色且1 min内不消失,计录消耗碘的标准液的体积.
d.进一步操作与数据处理
①滴定时,碘的标准溶液盛放在
②若本次滴定消耗碘的标准溶液为18.00mL,可测算出产品中N2H4-H2O的质量分数为
③为获得更可靠的滴定结果,步骤d中进一步操作主要是:
 氨气是一种重要的化工原料,但随着工业化进程的加快,氨气也逐渐变成居室里一种重要的污染性气体.
氨气是一种重要的化工原料,但随着工业化进程的加快,氨气也逐渐变成居室里一种重要的污染性气体.(1)液氨和水类似,也能发生电离:NH3+NH3=NH4++NH2-,其离子积常数为l.0×l0-30.现将2.3g金属钠投入1.0L液氨中,则液氨电离平衡
正方向
正方向
移动(填“不”、“正方向”、“逆方向”);待反应结束后,假设溶液的体积不变,所得溶液中NH4+的浓度为1×10-29mol/L
1×10-29mol/L
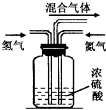
.(2)实验室模拟工业上用氮气和氢气合成氨气时,在反应前将两种气体通过如图装置,该装置的作用有三个:
①将氮气和氢气干燥:
②使氮气和氢气充分混合;
③
通过观察气泡控制氮气和氢气的流量,使氮气和氢气的量达到最佳比例
通过观察气泡控制氮气和氢气的流量,使氮气和氢气的量达到最佳比例
,从而提高氮气和氢气的利用率.(3)实验室可用氨气通过红热的氧化铜制取氮气,写出该反应的化学方程式:
2NH3+3CuO
3Cu+N2+3H2O
| ||
2NH3+3CuO
3Cu+N2+3H2O
.
| ||
(4)家庭空气中的氨主要来自建筑施工中使用的混凝土外加剂,如混凝土防冻剂尿素会和水缓慢发生反应:CO(NH2)2(s)+H2O(g) 2NH3(g)+CO2(g),该反应的平衡常数表达式为K=
| C2(NH3)?C(CO2) |
| C(H2O) |
| C2(NH3)?C(CO2) |
| C(H2O) |
(5)已知:N2(g)+O2(g)=2NO(g);△H=180Kj?mol-l4NH3(g)+5O2(g)=4NO(g)+6H2O(g);△H=-908Kj?mol-l请写出氨气被一氧化氮氧化生成氮气和气态水的热化学方程式:
4NH3(g)+6NO(g)=5N2(g)+6H2O(g)△H=-1808KJ/mol
4NH3(g)+6NO(g)=5N2(g)+6H2O(g)△H=-1808KJ/mol
. 第29届奥运会祥云火炬的外壳材料是高强度的铝镁合金.某课外活动小组欲对铝镁合金进行研究,测定其中镁的质量分数,他们利用盐酸、氢氧化钠溶液设计了三种不同的实验方案:
第29届奥运会祥云火炬的外壳材料是高强度的铝镁合金.某课外活动小组欲对铝镁合金进行研究,测定其中镁的质量分数,他们利用盐酸、氢氧化钠溶液设计了三种不同的实验方案:方案一:铝镁合金
| NaOH溶液 |
方案二:铝镁合金
| 盐酸 |
方案三:铝镁合金
| 盐酸 |
| 过量NaOH溶液 |
| 过滤、洗涤、烧灼、冷却 |
(1)写出方案一中发生反应的离子方程式
2Al+2OH-+2H2O=2AlO2-+3H2↑
2Al+2OH-+2H2O=2AlO2-+3H2↑
.(2)实验小组根据方案二设计了两个实验装置,如图1(图中的铁架台已省略).
你认为选择
乙
乙
(选填甲或乙)装置进行实验更合理,误差更小.(3)用方案三进行实验时,除了称量灼烧产物质量外,还需称量的是
合金样品的质量
合金样品的质量
.(4)拓展研究:在向铝镁合金溶于盐酸后的溶液中加入过量NaOH溶液时,生成沉淀的质量与加入NaOH溶液体积的关系可用数轴关系表示:
请你判断,根据图2数轴申的数据能否求出合金中镁的质量分数?
能
能
(选填“能”或“不能”)下列①②两题选一题作答.
①若不能求出合金中镁的质量分数,请说明理由
不填
不填
.②若能求出合金中镁的质量分数,则镁的质量分数为
30.8%
30.8%
. A、B、C、D、E五种短周期元素,它们的原子序数依次增大;A元素的原子半径最 小;B元素的最高价氧化物对应水化物与其氢化物能生成盐;D与A同主族,且与E同周 期;E元素原子的最外层电子数是其次外层电子数的
A、B、C、D、E五种短周期元素,它们的原子序数依次增大;A元素的原子半径最 小;B元素的最高价氧化物对应水化物与其氢化物能生成盐;D与A同主族,且与E同周 期;E元素原子的最外层电子数是其次外层电子数的| 3 | 4 |
请回答下列问题:
(1)B单质的电子式是
A.比较这两种元素的常见单质是沸点
B.比较这两种元素的单质与氢气化合的难易
C.比较这两种元素的气态氢化物的稳定性
(2)A、B、C、E可形成两种酸式盐(均由四种元素组成),两种酸式盐相互反应的离子方程式为
(3)A、C、E间可形成甲、乙两种微粒,它们均为负一价双原子阴离子,且甲有18个电子,乙有10个电子,则甲与乙反应的离子方程式为
(4)①在火箭推进器中装有液态B2A4和液态A2C2,已知0.4mol液态B2A4和足量液 态A2C2反应,生成气态B2和气态A2C,放出256.6kJ的热量.试写出该反应的热化学方程式
②B2A4是一种可燃性液体,B2A4--空气燃料电池是一种碱性燃料电池,电解质溶液是 20%-30%的KOH溶液,该电池放电时的负极反应式为:
③图是一个电解装置示意图,假设使用B2A4-空气燃料电池作为本装置中的电源,通电前两极铜片的质量相等,通电一段 时间后两极铜片的质量相差12.8g,则通过电路的电子的物质的量为