摘要:18.一种氮的无色氧化物.在密闭容器中加热时.其密度逐渐变小.在200℃时.约为原来的一半,继续加热时.容器里物质的密度继续减小.在600℃时.约为200℃时的2/3(容器内的压强始终是1.01×105帕).当降低温度时.容器内的密度增大.最后仍然得到原来的氮的氧化物.写出上述变化的化学方程式 .
网址:http://m.1010jiajiao.com/timu3_id_343951[举报]
一种氮的无色氧化物,在密闭容器中加热时,其密度逐渐变小,在200℃时,约为原来的一半;继续加热时,容器里物质的密度继续减小,在600℃时,约为200℃时的2/3(容器内的压强始终是1.01×105Pa).当降低温度时,容器内的密度增大,最后仍然得到原来的氮气的无色氧化物.写出上述变化的化学方程式.由低温到200℃时:________,由200℃到600℃时:________.
查看习题详情和答案>>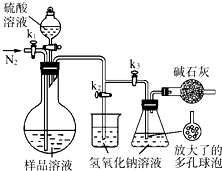 (2013?江苏三模)碳酸钠-过氧化氢加合物(aNa2CO3?bH2O2)具有漂白、杀菌作用.实验室用“醇析法”制备该物质的实验步骤如下:
(2013?江苏三模)碳酸钠-过氧化氢加合物(aNa2CO3?bH2O2)具有漂白、杀菌作用.实验室用“醇析法”制备该物质的实验步骤如下:第1步:取适量碳酸钠溶解于一定量水中,倒入烧瓶中;再加入少量稳定剂(MgCl2和Na2SiO3),搅拌均匀.
第2步:将适量30%的H2O2溶液在搅拌状态下滴入烧瓶中,于15℃左右反应1h.
第3步:反应完毕后再加入适量无水乙醇,静置、结晶,过滤、干燥得产品.
(1)第1步中,稳定剂与水反应生成2种常见的难溶物,其化学方程式为
MgCl2+Na2SiO3+2H2O=2NaCl+Mg(OH)2↓+H2SiO3↓
MgCl2+Na2SiO3+2H2O=2NaCl+Mg(OH)2↓+H2SiO3↓
.(2)第2步中,反应保持为15℃左右可采取的措施是
15℃水浴或冷水浴
15℃水浴或冷水浴
.(3)第3步中,无水乙醇的作用是
降低碳酸钠-过氧化氢化合物的溶解度(有利于晶体析出)
降低碳酸钠-过氧化氢化合物的溶解度(有利于晶体析出)
.(4)H2O2的含量可衡量产品的优劣.现称取m g(约0.5g)样品,用新煮沸过的蒸馏水配制成250mL溶液,取25.0mL于锥形瓶中,先用稀硫酸酸化,再用c mol?L-1 KMnO4溶液滴定至终点.
①配制250mL溶液所需的玻璃仪器有烧杯、玻璃棒、量筒、
(250mL)容量瓶
(250mL)容量瓶
、胶头滴管
胶头滴管
.②滴定终点观察到的现象是
溶液呈浅红色且30s内不褪色
溶液呈浅红色且30s内不褪色
.(5)可模拟用蒸馏法测定样品中碳酸钠的含量.装置如图所示(加热和固定装置已略去),实验步骤如下:
步骤1:按右图所示组装仪器,检查装置气密性.
步骤2:准确量取(4)中所配溶液50mL于烧瓶中.
步骤3:准确量取40.00mL约0.2mol?NaOH溶液2份,分别注入烧杯和锥形瓶中.
步骤4:打开活塞k1、k2,关闭活塞k3,缓缓通入氮气一段时间后,关闭k1、k2,打开k3;经滴液漏斗向烧瓶中加入10mL 3mol?硫酸溶液.
步骤5:加热至烧瓶中的液体沸腾,蒸馏,并保持一段时间.
步骤6:经k1再缓缓通入氮气一段时间.
步骤7:向锥形瓶中加入酸碱指示剂,用c1 mol?H2SO4标准溶液滴定至终点,消耗H2SO4标准溶液V1 mL.
步骤8:将实验步骤1~7重复2次.
①步骤3中,准确移取40.00mL NaOH溶液所需要使用的仪器是
碱式滴定管
碱式滴定管
.②步骤1~7中,确保生成的二氧化碳被氢氧化钠溶液完全吸收的实验步骤是
1,5,6
1,5,6
(填序号).③为获得样品中碳酸钠的含量,还需补充的实验是
用H2SO4标准溶液标定NaOH溶液的浓度
用H2SO4标准溶液标定NaOH溶液的浓度
.乙醇汽油含氧量达35%,使燃料燃烧更加充分,使用车用乙醇汽油,尾气排放的CO
和碳氢化合物平均减少30%以上,有效的降低和减少了有害的尾气排放。但是汽车使用乙醇汽油并不能减少NOx的排放,对NOx的有效消除成为环保领域的重要课题。NOx排入空气中,形成酸雨,造成空气污染。NOx中有一种红棕色气体,其溶于水的方程式是 。
(2)已知NO2和N2O4的结构式分别是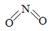 和
和 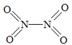 。
。
写出NO2转化N2O4的热化学方程式 。
(3)研究人员在汽车尾气系统中装置催化转化剂,可有效降低NOx的排放。
①写出用CO还原NO生成N2的化学方程式 。
②在实验室中模仿此反应,在一定条件下的密闭容器中,测得NO转化为N2的转化率随温度变化情况和n (NO)/n(CO)比例变化情况如下图。
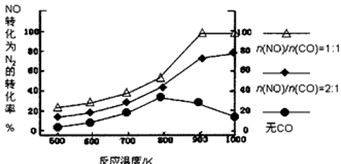
为达到NO转化为N2的最佳转化率,应该选用的温度和n(NO)/n(CO)比例分别为 、 ;该反应的?H 0(填“>”、“<”或“=”)。
(4)用 CxHy(烃)催化还原NOx也可消除氮氧化物生成无污染的物质。CH4与NO 发生反应的化学方程式为 。
和碳氢化合物平均减少30%以上,有效的降低和减少了有害的尾气排放。但是汽车使用乙醇汽油并不能减少NOx的排放,对NOx的有效消除成为环保领域的重要课题。NOx排入空气中,形成酸雨,造成空气污染。NOx中有一种红棕色气体,其溶于水的方程式是 。
(2)已知NO2和N2O4的结构式分别是
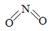 和
和  。
。| 物质 | NO2 | N2O4 | |
| 化学键 | N=O | N—N | N=O |
| 键能(kJ/mol) | 466 | 167 | 438 |
(3)研究人员在汽车尾气系统中装置催化转化剂,可有效降低NOx的排放。
①写出用CO还原NO生成N2的化学方程式 。
②在实验室中模仿此反应,在一定条件下的密闭容器中,测得NO转化为N2的转化率随温度变化情况和n (NO)/n(CO)比例变化情况如下图。

为达到NO转化为N2的最佳转化率,应该选用的温度和n(NO)/n(CO)比例分别为 、 ;该反应的?H 0(填“>”、“<”或“=”)。
(4)用 CxHy(烃)催化还原NOx也可消除氮氧化物生成无污染的物质。CH4与NO 发生反应的化学方程式为 。
乙醇汽油含氧量达35%,使燃料燃烧更加充分,使用车用乙醇汽油,尾气排放的CO和碳氢化合物平均减少30%以上,有效的降低和减少了有害的尾气排放。但是汽车使用乙醇汽油并不能减少NOx的排放,对NOx的有效消除成为环保领域的重要课题。NOx排入空气中,形成酸雨,造成空气污染。NOx中有一种红棕色气体,其溶于水的方程式是 。
(2)已知NO2和N2O4的结构式分别是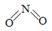 和
和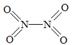 。
。
| 物质 | NO2 | N2O4 | |
| 化学键 | N=O | N—N | N=O |
| 键能(kJ/mol) | 466 | 167 | 438 |
写出NO2转化N2O4的热化学方程式 。
(3)研究人员在汽车尾气系统中装置催化转化剂,可有效降低NOx的排放。
① 写出用CO还原NO生成N2的化学方程式 。
② 在实验室中模仿此反应,在一定条件下的密闭容器中,测得NO转化为N2的转化率随温度变化情况和n (NO)/n(CO)比例变化情况如下图。
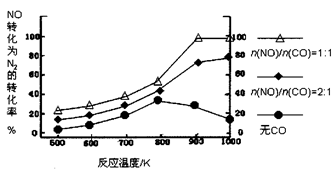
为达到NO转化为N2的最佳转化率,应该选用的温度和n(NO)/n(CO)比例分别为 、 ;该反应的?H 0(填“>”、“<”或“=”)。
(4)用 CxHy(烃)催化还原NOx也可消除氮氧化物生成无污染的物质。CH4与NO发生反应的化学方程式为 。 查看习题详情和答案>>
乙醇汽油含氧量达35%,使燃料燃烧更加充分,使用车用乙醇汽油,尾气排放的CO
和碳氢化合物平均减少30%以上,有效的降低和减少了有害的尾气排放。但是汽车使用乙醇汽油并不能减少NOx的排放,对NOx的有效消除成为环保领域的重要课题。NOx排入空气中,形成酸雨,造成空气污染。NOx中有一种红棕色气体,其溶于水的方程式是 。
(2)已知NO2和N2O4的结构式分别是 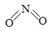 和
和  。
。
| 物质 | NO2 | N2O4 | |
| 化学键 | N=O | N—N | N=O |
| 键能(kJ/mol) | 466 | 167 | 438 |
(3)研究人员在汽车尾气系统中装置催化转化剂,可有效降低NOx的排放。
①写出用CO还原NO生成N2的化学方程式 。
②在实验室中模仿此反应,在一定条件下的密闭容器中,测得NO转化为N2的转化率随温度变化情况和n (NO)/n(CO)比例变化情况如下图。

为达到NO转化为N2的最佳转化率,应该选用的温度和n(NO)/n(CO)比例分别为 、 ;该反应的?H 0(填“>”、“<”或“=”)。
(4)用 CxHy(烃)催化还原NOx也可消除氮氧化物生成无污染的物质。CH4与NO 发生反应的化学方程式为 。 查看习题详情和答案>>