摘要: 3Ca2++6+9OH-=Ca3(PO4)2↓++3+9H2O
网址:http://m.1010jiajiao.com/timu3_id_343890[举报]
CoCl2?6H2O是一种饲料营养强化剂.一种利用水钴矿[主要成分为Co2O3、Co(OH)3,还含少量Fe2O3、Al2O3、MnO等]制取CoCl2?6H2O的工艺流程如下:
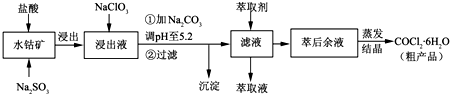
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
(1)写出浸出过程中Co2O3发生反应的离子方程式
(2)NaClO3的作用是
(3)加Na2CO3调pH至5.2所得沉淀为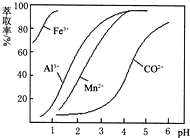
(4)萃取剂对金属离子的萃取率与pH的关系如右图.萃取剂的作用是
A.2.0~2.5 B.3.0~3.5 C.4.0~4.5
(5)为测定粗产品中CoCl2?6H2O含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量.通过计算发现粗产品中CoCl2?6H2O的质量分数大于100%,其原因可能是
查看习题详情和答案>>

已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
Co2O3+SO32-+4H+=2Co2++SO42-+2H2O
Co2O3+SO32-+4H+=2Co2++SO42-+2H2O
.(2)NaClO3的作用是
将Fe2+氧化成Fe3+
将Fe2+氧化成Fe3+
.(3)加Na2CO3调pH至5.2所得沉淀为
Fe(OH)3、Al(OH)3
Fe(OH)3、Al(OH)3
.
(4)萃取剂对金属离子的萃取率与pH的关系如右图.萃取剂的作用是
除去溶液中的Mn2+
除去溶液中的Mn2+
;其使用的适宜pH范围是B
B
.A.2.0~2.5 B.3.0~3.5 C.4.0~4.5
(5)为测定粗产品中CoCl2?6H2O含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量.通过计算发现粗产品中CoCl2?6H2O的质量分数大于100%,其原因可能是
粗产品含有可溶性氯化物或晶体失去了部分结晶水
粗产品含有可溶性氯化物或晶体失去了部分结晶水
.(答一条即可)(2012?杭州一模)2011年8月12日,《云南信息报》首度披露 了云南曲靖铬污染事件,引起全国广泛关注.工业上将制取重铬酸钾(K2Cr2O7)和铬酸酐(CrO3)的剩余废渣称为铬渣,其成分为:SiO2、Al2O3、MgO、Fe2O3、CrO3、K2Cr2O7等.
已知:①重铬酸钾和铬酸酐都易溶于水,这是造成铬污染的主要原因,它们都是强氧化剂,铬酸酐溶于水呈酸性;
②+6价铬易被人体吸收,可致癌:+3价铬不易被人体吸收,毒性小.
③下表为一些金属氢氧化物沉淀的pH参照数据.
回答下列处理铬渣、消除铬污染的有关问题:
(1)将铬渣用稀硫酸浸取、过滤,在浸出液中加入适量的绿矾(FeSO4?7H2O),加入绿矾的目的是
(2)再向浸出液中缓慢加入烧碱,至pH刚好达到4.7,过滤,所得沉淀的化学式是
(3)向(2)中得到的滤液中加入硫酸,调节至呈强酸性,所得的溶液是含
查看习题详情和答案>>
已知:①重铬酸钾和铬酸酐都易溶于水,这是造成铬污染的主要原因,它们都是强氧化剂,铬酸酐溶于水呈酸性;
②+6价铬易被人体吸收,可致癌:+3价铬不易被人体吸收,毒性小.
③下表为一些金属氢氧化物沉淀的pH参照数据.
| 物质 | 开始沉淀 | 完全沉淀 |
| Fe(OH)3 | 2.7 | 3.7 |
| Al(OH)3 | 3.7 | 4.7 |
| Cr(OH)3 | 4.7 | a |
| Fe(OH)2 | 7.6 | 9.6 |
| Mg(OH)2 | 9.6 | 11.1 |
(1)将铬渣用稀硫酸浸取、过滤,在浸出液中加入适量的绿矾(FeSO4?7H2O),加入绿矾的目的是
将高价有毒的
元素含有成无毒的
| +6 |
| Cr |
| +3 |
| Cr |
将高价有毒的
元素含有成无毒的
.| +6 |
| Cr |
| +3 |
| Cr |
(2)再向浸出液中缓慢加入烧碱,至pH刚好达到4.7,过滤,所得沉淀的化学式是
Fe(OH)3、Al(OH)3
Fe(OH)3、Al(OH)3
;常温下,Cr(OH)3的溶度积Ksp=10-32,要使Cr3+完全沉淀[c(Cr3+)降至10-5mol?L-1视为沉淀完全],溶液的pH应调于a=5
5
.(3)向(2)中得到的滤液中加入硫酸,调节至呈强酸性,所得的溶液是含
MgSO4和K2SO4
MgSO4和K2SO4
溶质的溶液.(2013?浦东新区三模)重晶石矿(主要成分为硫酸钡)因为含有Fe2O3、MnO及炭质等杂质而常呈深褐色.工业上将重晶石矿粉碎后与硫酸、铝粉在反应槽中混合加热(即“漂白”),再经水洗等一系列工序制得白色的重晶石填料,广泛用作纸张、油漆等的填充剂.已知MnO是碱性氧化物,Al粉可以将深色的Fe3+转化为浅色的Fe2+.重晶石填料的生产工艺流程为:

(1)在该流程中,为加快“漂白”速度,采取的措施有
(2)硫酸起到了“漂白”的作用.请写出硫酸直接起到该作用时的化学方程式:
(3)二次漂白水洗过滤后,检验滤渣不含Fe2+离子的方法是
(4)二次漂白前,煅烧的主要目的是
(5)工业生产中为了充分利用资源,将滤液经过处理得到化工原料Fe2O3.操作过程是:
①滤液中通入过量Cl2,其目的是
②再加入适量NaOH来调节溶液的pH,其目的是
有关离子开始沉淀及完全沉淀时的pH如下:
(6)最后通过
查看习题详情和答案>>

(1)在该流程中,为加快“漂白”速度,采取的措施有
重晶石和铝都使用粉末
重晶石和铝都使用粉末
、加热
加热
.(2)硫酸起到了“漂白”的作用.请写出硫酸直接起到该作用时的化学方程式:
Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
、MnO+H2SO4=MnSO4+H2O
MnO+H2SO4=MnSO4+H2O
.(3)二次漂白水洗过滤后,检验滤渣不含Fe2+离子的方法是
取最后一次洗涤液于试管中
取最后一次洗涤液于试管中
、先滴加氯水再滴加KSCN溶液无明显变化
先滴加氯水再滴加KSCN溶液无明显变化
.(4)二次漂白前,煅烧的主要目的是
除去炭质
除去炭质
.将煅烧后的固体磨成细粉,使用的是加有刚玉球的振动磨.这说明刚玉具有很高的硬度
硬度
.(5)工业生产中为了充分利用资源,将滤液经过处理得到化工原料Fe2O3.操作过程是:
①滤液中通入过量Cl2,其目的是
将Fe2+转化为Fe3+
将Fe2+转化为Fe3+
.②再加入适量NaOH来调节溶液的pH,其目的是
使Fe3+沉淀完全,而其它离子不发生沉淀
使Fe3+沉淀完全,而其它离子不发生沉淀
,调节溶液的pH范围为2.7-3.7
2.7-3.7
.有关离子开始沉淀及完全沉淀时的pH如下:
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 7.6 | 9.7 |
| Fe3+ | 2.7 | 3.7 |
| Al3+ | 3.8 | 4.7 |
| Mn2+ | 8.3 | 9.8 |
洗涤干燥
洗涤干燥
、高温煅烧
高温煅烧
得到氧化铁.高纯碳酸锰广泛应用于电子工业,是制造高性能磁性材料的主要原料.新工艺采用工业冶铜后的废气SO2进行湿法浸取软锰矿(主要含MnO2,同时含有少量SiO2、Fe2O3、Al2O3)来制备.(已知亚硫酸酸性强于碳酸)
①将过量的SO2气体通入软锰矿浆中进行“浸锰”操作,并控制温度加热反应;
②向浸锰结束后的滤液中加入MnO2、同时通入空气,再用Na2CO3溶液调节pH为3.7后过滤分离;
③调节滤液pH值为6.5~7.2,然后加入NH4HCO3,有浅红色的沉淀生成,过滤洗涤干燥后就可以得到高纯碳酸锰.
工业流程图如下:

已知生成氢氧化物的pH如下表:
请根据题中有关信息回答问题:
(1)“浸锰”后所得混合液中主要存在的金属阳离子有
(2)由图可知,副反应MnSO4+SO2 MnS2O6的△H
MnS2O6的△H
(3)步骤②中加入MnO2和通入空气的作用
(4)③中控制温度为60~70℃,温度不宜太高的原因是
(5)与传统的电解法制MnCO3工艺相比较,新工艺的优点是
查看习题详情和答案>>
①将过量的SO2气体通入软锰矿浆中进行“浸锰”操作,并控制温度加热反应;
②向浸锰结束后的滤液中加入MnO2、同时通入空气,再用Na2CO3溶液调节pH为3.7后过滤分离;
③调节滤液pH值为6.5~7.2,然后加入NH4HCO3,有浅红色的沉淀生成,过滤洗涤干燥后就可以得到高纯碳酸锰.
工业流程图如下:

已知生成氢氧化物的pH如下表:
| 物质 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 |
| 开始沉淀pH | 2.7 | 7.6 | 8.3 |
| 完全沉淀pH | 3.7 | 9.6 | 9.8 |
(1)“浸锰”后所得混合液中主要存在的金属阳离子有
Mn2+、Fe2+、Al3+
Mn2+、Fe2+、Al3+
.(2)由图可知,副反应MnSO4+SO2
 MnS2O6的△H
MnS2O6的△H<
<
0(填>、<或=),为减少MnS2O6 的生成,“浸锰”的适宜温度是150℃
150℃
.(3)步骤②中加入MnO2和通入空气的作用
加入MnO2是为了除去过量的SO2;通入空气将Fe2+氧化成Fe3+便于后来加碳酸钠除去
加入MnO2是为了除去过量的SO2;通入空气将Fe2+氧化成Fe3+便于后来加碳酸钠除去
.(4)③中控制温度为60~70℃,温度不宜太高的原因是
防止NH4HCO3受热分解
防止NH4HCO3受热分解
.(5)与传统的电解法制MnCO3工艺相比较,新工艺的优点是
综合利用了尾气SO2有利于环境保护,同时节约能源
综合利用了尾气SO2有利于环境保护,同时节约能源
(写两点).化学实验室通常用粗锌和稀硫酸反应制氢气,因此在制氢废液中含有大量的硫酸锌.同时,由于粗锌中还含有铁等杂质,使得溶液中混有一定量的硫酸亚铁,为了充分利用制氢废液,常用其制备皓矾(ZnSO4?7H2O).某校化学兴趣小组的同学以制氢气的废液为原料来制取皓矾.制备皓矾的实验流程如图所示.

已知:开始生成氢氧化物沉淀到沉淀完全的pH范围分别为:Fe(OH)3:2.7-3.7Fe(OH)2:7.6-9.6 Zn(OH)2:5.7-8.0试回答下列问题:?
(1)加入的试剂①,供选择使用的有:氨水、NaClO溶液、20%的H2O2、浓硫酸、浓硝酸等,最好选用
(2)加入的试剂②,供选择使用的有:a、Zn粉,b、ZnO,c、Zn(OH)2,d、ZnCO3,e、ZnSO4等,可选用
(3)从晶体1→晶体2,该过程的名称是
(4)在得到皓矾时,向晶体中加入少量酒精洗涤而不用水的原因是
查看习题详情和答案>>

已知:开始生成氢氧化物沉淀到沉淀完全的pH范围分别为:Fe(OH)3:2.7-3.7Fe(OH)2:7.6-9.6 Zn(OH)2:5.7-8.0试回答下列问题:?
(1)加入的试剂①,供选择使用的有:氨水、NaClO溶液、20%的H2O2、浓硫酸、浓硝酸等,最好选用
20%的H2O2
20%的H2O2
,其理由是将制氢废液中的Fe2+氧化成Fe3+,同时避免引入新的杂质
将制氢废液中的Fe2+氧化成Fe3+,同时避免引入新的杂质
;(2)加入的试剂②,供选择使用的有:a、Zn粉,b、ZnO,c、Zn(OH)2,d、ZnCO3,e、ZnSO4等,可选用
bcd
bcd
;(3)从晶体1→晶体2,该过程的名称是
重结晶
重结晶
;(4)在得到皓矾时,向晶体中加入少量酒精洗涤而不用水的原因是
为了冲洗掉晶体表面的杂质离子;防止晶体溶解,影响产率
为了冲洗掉晶体表面的杂质离子;防止晶体溶解,影响产率
.