摘要:(1)HCOOH CO↑+H2O (2) A处(Fe2O3) 由红棕色变黑色 Fe2O3+3CO2Fe+3CO2 B处 变浑浊 CO2+Ca(OH)2 == CaCO3↓+H2O C处 火焰呈淡蓝色 3CO+O2 2CO2 (3)H2C2O4·2H2O CO2↑+CO↑+3H2O (4)用NaOH溶液洗气
网址:http://m.1010jiajiao.com/timu3_id_343409[举报]
(2010?聊城模拟)联合国气候变化大会于2009年12月7~18目在哥本哈根召开.中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~45%.
(1)有效“减碳”的手段之一是节能.下列制氢方法最节能的是
A.电解水制氢:2H2O
2H2↑+O2↑
B.高温使水分解制氢:2H2O
2H2↑+O2↑
C.太阳光催化分解水制氢:2H2O
2H2↑+O2↑
D.天然气制氢:CH4+H2O
CO+3H2
(2)用CO2和氢气合成CH3OCH3(甲醚)是解决能源危机的研究方向之一.
己知:CO(g)+2H2(g)?CH3OH(g)△H=-90.7KJ?mol-1 ①
2CH3OH(g)?CH3OCH3(g)+H2O(g)△H=-23.5KJ ②
CO2(g)+H2(g)△H=-41.2KJ?mol-1 ③
则反应2CO2(g)+6H2(g)→2CH3OH(g)+2H2O(g)的△H=
(3)CO2可转化成有机物实现碳循环:CO2→CH3OH→HCOOH,用离子方程式表示HCOONa溶液呈碱性的原因
,升高温度,Kh
(4)常温下,将0.2mol?L-1HCOOH和0.1mol?L-1NaOH溶液等体积混合,所得溶液的pH<7,说明HC00H的电离程度
查看习题详情和答案>>
(1)有效“减碳”的手段之一是节能.下列制氢方法最节能的是
C
C
(填字母序号).A.电解水制氢:2H2O
| ||
B.高温使水分解制氢:2H2O
| ||
C.太阳光催化分解水制氢:2H2O
| ||
| 催化剂 |
D.天然气制氢:CH4+H2O
| 高温 |
(2)用CO2和氢气合成CH3OCH3(甲醚)是解决能源危机的研究方向之一.
己知:CO(g)+2H2(g)?CH3OH(g)△H=-90.7KJ?mol-1 ①
2CH3OH(g)?CH3OCH3(g)+H2O(g)△H=-23.5KJ ②
CO2(g)+H2(g)△H=-41.2KJ?mol-1 ③
则反应2CO2(g)+6H2(g)→2CH3OH(g)+2H2O(g)的△H=
-122.5KJ?mol-1
-122.5KJ?mol-1
.(3)CO2可转化成有机物实现碳循环:CO2→CH3OH→HCOOH,用离子方程式表示HCOONa溶液呈碱性的原因
HCOO-+H2O=HCOOH+OH-
HCOO-+H2O=HCOOH+OH-
,写出该反应的平衡常数(Kh)表达式:Kh=| C(HCOOH)C(OH-) |
| C(HCOO-) |
| C(HCOOH)C(OH-) |
| C(HCOO-) |
增大
增大
(选填“增大”、“减小”或“不变”).(4)常温下,将0.2mol?L-1HCOOH和0.1mol?L-1NaOH溶液等体积混合,所得溶液的pH<7,说明HC00H的电离程度
大于
大于
HCOONa的水解程度(填“大于”或“小于”).该混合溶液中离子浓度由大到小的顺序是C(HCOO-)>C(Na+)>C(H+)>C(OH-)
C(HCOO-)>C(Na+)>C(H+)>C(OH-)
. (2009?广东)甲酸甲酯水解反应方程式为:
(2009?广东)甲酸甲酯水解反应方程式为:HCOOCH3(l)+H2O(l)
 HCOOH(l)+CH3OH(l)△H>0
HCOOH(l)+CH3OH(l)△H>0某小组通过实验研究该反应(反应过程中体积变化忽略不计).反应体系中各组分的起始量如下表:

甲酸甲酯转化率在温度T1下随反应时间(t)的变化如下图:
(1)根据上述条件,计算不同时间范围内甲酸甲酯的平均反应速率,结果见下表:

请计算15~20min范围内甲酸甲酯的减少量为
0.045
0.045
mol,甲酸甲酯的平均反应速率为0.009
0.009
mol?min-1(不要求写出计算过程).(2)依据以上数据,写出该反应的反应速率在不同阶段的变化规律及其原因:
①反应初期:虽然甲酸甲酯的量较大,但甲酸量很小,催化效果不明显,反应速率较慢.
②反应中期:甲酸量逐渐增多,催化效果显著,反应速率明显增大.
③反应后期:甲酸量增加到一定程度后,浓度对反应速率的影响成主导因素,特别是逆反应速率的增大,使总反应速率逐渐减小,直至为零.
②反应中期:甲酸量逐渐增多,催化效果显著,反应速率明显增大.
③反应后期:甲酸量增加到一定程度后,浓度对反应速率的影响成主导因素,特别是逆反应速率的增大,使总反应速率逐渐减小,直至为零.
①反应初期:虽然甲酸甲酯的量较大,但甲酸量很小,催化效果不明显,反应速率较慢.
②反应中期:甲酸量逐渐增多,催化效果显著,反应速率明显增大.
③反应后期:甲酸量增加到一定程度后,浓度对反应速率的影响成主导因素,特别是逆反应速率的增大,使总反应速率逐渐减小,直至为零.
.②反应中期:甲酸量逐渐增多,催化效果显著,反应速率明显增大.
③反应后期:甲酸量增加到一定程度后,浓度对反应速率的影响成主导因素,特别是逆反应速率的增大,使总反应速率逐渐减小,直至为零.
(3)上述反应的平衡常数表达式为:K=
| c(HCOOH)?c(CH3OH) |
| c(HCOOCH3)?c(H2O) |
| 1 |
| 7 |
| 1 |
| 7 |
(4)其他条件不变,仅改变温度为T2(T2大于T1),在答题卡框图中画出温度T2下甲酸甲酯转化率随反应时间变化的预期结果示意图.
(2013?杭州一模)某种甲酸酯水解反应方程式为:
HCOOR(l)+H2O(l)?HCOOH(l)+ROH (l)△H>0
某小组通过实验研究该反应(反应过程中体积变化忽略不计).反应体系中各组分的起始浓度如下表:
甲酸酯转化率在温度T1下随反应时间(t)的变化如图:
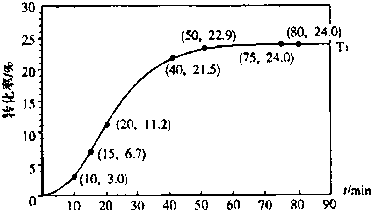
根据上述条件,计算不同时间范围内甲酸醋的平均反应速率,结果见下表:
(1)该反应的平衡常数K 的表达式
(不要求计算);T1温度下平衡体系中.c(ROH )为
(2)15~20min范围内用甲酸酯表示的平均反应速率为
(3)根据题给数据分析,从影响反应速率的角度来看,生成物甲酸在该反应中还起到了
查看习题详情和答案>>
HCOOR(l)+H2O(l)?HCOOH(l)+ROH (l)△H>0
某小组通过实验研究该反应(反应过程中体积变化忽略不计).反应体系中各组分的起始浓度如下表:
| 组分 | HCOOR | H2O | HCOOH } | ROH |
| 物质的量浓度/mol?L-1’ | 1.00 | 1.99 | 0.01 | 0.52 |

根据上述条件,计算不同时间范围内甲酸醋的平均反应速率,结果见下表:
| 反应时间/min | 0~5 | 10~15 | 20~25 | 30~35 | 40~45 | 50~55 | 75~80 |
| 平均速率/10-3mol?L-1?min-1 | 1.9 | 7.4 | 7.8 | 4.4 | 1.6 | 0.8 | 0.0 |
| c(ROH)c(HCOOH) |
| c(HCOOR)c(H2O) |
| c(ROH)c(HCOOH) |
| c(HCOOR)c(H2O) |
0.76
0.76
mol?L一1(2)15~20min范围内用甲酸酯表示的平均反应速率为
0.009
0.009
mol?L-1?min-1,(不要求写出计算过程).(3)根据题给数据分析,从影响反应速率的角度来看,生成物甲酸在该反应中还起到了
催化剂
催化剂
的作用.