摘要:5.在恒温.恒容的密闭容器中发生如下反应:,当H2和Br2的起始浓度均为0.20mol·L-1时.达到平衡时HBr的浓度为0.32mol·L-1.则当H2和Br2的 起始浓度均为0.10mol·L-1时.达平行时H2的浓度(mol·L-1)为 A.0.01 B.0.02 C.0.04 D.0.08
网址:http://m.1010jiajiao.com/timu3_id_343125[举报]
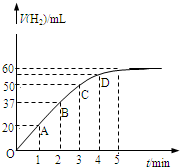 在恒温、恒容的密闭容器中发生如下反应:2HI(g)?H2(g)+I2(g),实验测定,在标准状况下产生氢气的体积和时间的关系如图所示.回答下列问题:
在恒温、恒容的密闭容器中发生如下反应:2HI(g)?H2(g)+I2(g),实验测定,在标准状况下产生氢气的体积和时间的关系如图所示.回答下列问题:(1)A、B、C、D四点对应的化学反应速率由快到慢顺序为
A>B>C>D
A>B>C>D
.(2)解释化学反应速率的大小变化原因
随反应的进行反应物HI的浓度逐渐减小
随反应的进行反应物HI的浓度逐渐减小
.(3)在5min后,收集到的氢气体积不再增加,原因是
该可逆反应达到平衡状态
该可逆反应达到平衡状态
.(4)下列叙述能说明上述反应达到最大限度的是
DE
DE
(填序号)A.HI、H2、I2的物质的量之比为2:1:1
B.混合气体的压强不随时间的变化而变化
C.单位时间内每消耗2mol HI,同时生成1mol H2
D.混合气体的颜色不随时间的变化而变化
E.HI、H2、I2的生成速率之比为2:1:1.
在恒温、恒容的密闭容器中发生如下反应:H2(g)+Br2(g) 2HBr。当H2和Br2的起始浓度均为0.20mol·L-1时,达到平衡时HBr的浓度为0.32mol·L-1,则当H2和Br2的起始浓度均为0.10mol·L-1时,达平衡时H2的浓度为( )
2HBr。当H2和Br2的起始浓度均为0.20mol·L-1时,达到平衡时HBr的浓度为0.32mol·L-1,则当H2和Br2的起始浓度均为0.10mol·L-1时,达平衡时H2的浓度为( )
A.0.01 mol.L-1 B.0.02 mol·L-1
C.0.04 mol·L-1 D.0.08 mol·L-1
查看习题详情和答案>>在恒温、恒容的密闭容器中发生如下反应:2HI(g)?H2(g)+I2(g),实验测定,在标准状况下产生氢气的体积和时间的关系如图所示.回答下列问题:
(1)A、B、C、D四点对应的化学反应速率由快到慢顺序为______.
(2)解释化学反应速率的大小变化原因______.
(3)在5min后,收集到的氢气体积不再增加,原因是______.
(4)下列叙述能说明上述反应达到最大限度的是______(填序号)
A.HI、H2、I2的物质的量之比为2:1:1
B.混合气体的压强不随时间的变化而变化
C.单位时间内每消耗2molHI,同时生成1molH2
D.混合气体的颜色不随时间的变化而变化
E.HI、H2、I2的生成速率之比为2:1:1.

查看习题详情和答案>>
(1)A、B、C、D四点对应的化学反应速率由快到慢顺序为______.
(2)解释化学反应速率的大小变化原因______.
(3)在5min后,收集到的氢气体积不再增加,原因是______.
(4)下列叙述能说明上述反应达到最大限度的是______(填序号)
A.HI、H2、I2的物质的量之比为2:1:1
B.混合气体的压强不随时间的变化而变化
C.单位时间内每消耗2molHI,同时生成1molH2
D.混合气体的颜色不随时间的变化而变化
E.HI、H2、I2的生成速率之比为2:1:1.
