摘要:推导金属元素的化合价与所组成的盐的相对分子质量的关系.必须考虑化合价为奇数或偶数时.其化学式的表达可能有两种不同的情况,在运用抽象字母进行此类计算时.可采用联立方程组消元计算法或由相对分子质量之差速解.见例1.
网址:http://m.1010jiajiao.com/timu3_id_342465[举报]
A【物质结构与性质】纳米技术制成的金属燃料、非金属固体燃料、氢气等已应用到社会生活和高科技领域。
 ⑴A和B的单质单位质量的燃烧热大,可用作燃料。已知A和B为短周期元素,其原子的第一至第四电离能如下表所示:
⑴A和B的单质单位质量的燃烧热大,可用作燃料。已知A和B为短周期元素,其原子的第一至第四电离能如下表所示:| 电离能(kJ/mol) | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |
| B | 738 | 1451 | 7733 | 10540 |
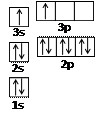
该同学所画的电子排布图违背了 。
②根据价层电子对互斥理论,预测A和氯元素形成的简单分子空间构型为 。
 ⑵氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料。
⑵氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料。①已知金刚石中的C-C的键长为154.45pm,C60中C-C键长为145~140pm,有同学据此认为C60的熔点高于金刚石,你认为是否正确并阐述理由 。
②科学家把C60和K掺杂在一起制造了一种富勒烯化合物,其晶胞如图所示,该物质在低温时是一种超导体。该物质的K原子和C60分子的个数比为 。
③继C60后,科学家又合成了Si60、N60,C、Si、N原子电负性由大到小的顺序是 。Si60分子中每个硅原子只跟相邻的3个硅原子形成共价键,且每个硅原子最外层都满足8电子稳定结构,则Si60分子中π键的数目为 。
B【实验化学】某化学研究性学习小组为测定果汁中Vc含量,设计并进行了以下实验。
Ⅰ 实验原理
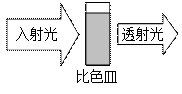
将特定频率的紫外光通过装有溶液的比色皿,一部分被吸收,通过对比入射光强度和透射光强度之间的关系可得到溶液的吸光度(用A表示,可由仪器自动获得)。吸光度A的大小与溶液中特定成分的浓度有关,杂质不产生干扰。溶液的pH对吸光度大小有一定影响。
Ⅱ 实验过程
⑴配制系列标准溶液。分别准确称量质量为1.0mg、1.5mg、2.0mg、2.5mg的标准Vc试剂,放在烧杯中溶解,加入适量的硫酸,再将溶液完全转移到100mL容量瓶中定容。
上述步骤中所用到的玻璃仪器除烧杯、容量瓶外还有 。
⑵较正分光光度计并按顺序测定标准溶液的吸光度。为了减小实验的误差,实验中使用同一个比色皿进行实验,测定下一溶液时应对比色皿进行的操作是 。测定标准溶液按浓度 (填“由大到小”或“由小到大”)的顺序进行。
⑶准确移取10.00mL待测果汁样品到100mL容量瓶中,加入适量的硫酸,再加水定容制得待测液,测定待测液的吸光度。
Ⅲ 数据记录与处理
 ⑷实验中记录到的标准溶液的吸光度与浓度的关系如下表所示,根据所给数据作出标准溶液的吸光度随浓度变化的曲线。
⑷实验中记录到的标准溶液的吸光度与浓度的关系如下表所示,根据所给数据作出标准溶液的吸光度随浓度变化的曲线。| 标准试剂编号 | ① | ② | ③ | ④ | 待测液 |
| 浓度mg/L | 10 | 15 | 20 | 25 | — |
| pH | 6 | 6 | 6 | 6 | 6 |
| 吸光度A | 1.205 | 1.805 | 2.405 | 3.005 | 2.165 |
⑹实验结果与数据讨论
除使用同一个比色皿外,请再提出两个能使实验测定结果更加准确的条件控制方法 。
A.不锈钢是由铁、铬、镍、碳及众多不同元素所组成的合金,铁是主要成分元素,铬是第一主要的合金元素.其中铬的含量不能低于11%,不然就不能生成致密氧化膜CrO3防止腐蚀.
(1)基态碳(C)原子的轨道表示式为______.
(2)[Cr(H2O)4Cl2]Cl?2H2O中Cr的配位数为______;已知CrO5中Cr为+6价,则CrO5的结构式为______.
(3)金属镍粉在CO气流中轻微加热,生成无色挥发性液态Ni(CO)4,呈四面体构型.423K时,Ni(CO)4分解为Ni和CO,从而制得高纯度的Ni粉.试推测:四羰基镍的晶体类型是______,与Ni(CO)4中配体互为等电子的离子是______.
(4)Fe的一种晶体如甲、乙所示,若按甲虚线方向切乙得到A~B图中正确的是______.

(5)据报道,只含镁、镍和碳三种元素的晶体竟然具有超导性.鉴于这三种元素都是常见元素,从而引起广泛关注.该晶体的结构可看作由镁原子和镍原子在一起进行面心立方密堆积,试写出该晶体的化学式______.晶体中每个镁原子周围距离最近的镍原子有______个.


查看习题详情和答案>>
(1)基态碳(C)原子的轨道表示式为______.
(2)[Cr(H2O)4Cl2]Cl?2H2O中Cr的配位数为______;已知CrO5中Cr为+6价,则CrO5的结构式为______.
(3)金属镍粉在CO气流中轻微加热,生成无色挥发性液态Ni(CO)4,呈四面体构型.423K时,Ni(CO)4分解为Ni和CO,从而制得高纯度的Ni粉.试推测:四羰基镍的晶体类型是______,与Ni(CO)4中配体互为等电子的离子是______.
(4)Fe的一种晶体如甲、乙所示,若按甲虚线方向切乙得到A~B图中正确的是______.

(5)据报道,只含镁、镍和碳三种元素的晶体竟然具有超导性.鉴于这三种元素都是常见元素,从而引起广泛关注.该晶体的结构可看作由镁原子和镍原子在一起进行面心立方密堆积,试写出该晶体的化学式______.晶体中每个镁原子周围距离最近的镍原子有______个.


下图是中学教材中元素周期表的一部分,试回答下列问题:
| ① | | | | | ||||||||||||||||||||
| | | | | ② | ③ | ④ | ⑤ | | | |||||||||||||||
| ⑥ | | | | | | | | | | | | ⑦ | ⑧ | | ⑨ | ⑩ | 11 | |||||||
| 12 | | | | | | | | | | | | | 13 | | | | | |||||||
| | | | | | | | | | | | | | 14 | | | 15 | | |||||||
| | | | | | | | | | | | | | | | | | | |||||||
①性质 最不活泼的是 ;
②原子半径最小的是(除稀有气体元素) _ 。简单阴离子半径最大的是 。
③形成的气态氢化物最稳定的是 ;
④最高价氧化物对应的水化物酸性最强的是 ,
⑤在⑤⑩15三种元素形成的阴离子中还原性最强的是 ,
⑥可作半导体的是 (填表中编号)
(2)用电子式表示②与④形成的化合物的形成过程 __。
(3)⑨与12形成的化合物溶于水所克服的微粒间作用力为 。
(4)13在元素周期表中的位置是 ,元素③形成的单质的结构式为 。
(5)________(填化学式)的单质既可以和盐酸又可以和氢氧化钠溶液反应,其单质与氢氧化钠溶液反应的离子方程式是___________________________________________。
(6) “神舟”六号载人飞船内需要有一种化合物来吸收航天员呼出的CO2,你认为该物质应该是由上表中的___ _(填表中编号)元素组成的,用化学方程式表示吸收原理:_________________ ______ 。
(7)设②的原子序数为Z,则14的原子序数为 (用Z表示)。
考查知识点:根据元素周期表,①比较金属性,非金属性,对应粒子还原性及半径的大小;②判断元素在周期表的位置;③化学键 ④位置确定序数;⑤位置推测用途 查看习题详情和答案>>
下图是中学教材中元素周期表的一部分,试回答下列问题:
(1)在上表所列出的短周期元素中(填具体物质化学式)
①性质 最不活泼的是 ;
②原子半径最小的是(除稀有气体元素) _ 。简单阴离子半径最大的是 。
③形成的气态氢化物最稳定的是 ;
④最高价氧化物对应的水化物酸性最强的是 ,
⑤在⑤⑩15三种元素形成的阴离子中还原性最强的是 ,
⑥可作半导体的是 (填表中编号)
(2)用电子式表示②与④形成的化合物的形成过程 __。
(3)⑨与12形成的化合物溶于水所克服的微粒间作用力为 。
(4)13在元素周期表中的位置是 ,元素③形成的单质的结构式为 。
(5)________(填化学式)的单质既可以和盐酸又可以和氢氧化钠溶液反应,其单质与氢氧化钠溶液反应的离子方程式是___________________________________________。
(6) “神舟”六号载人飞船内需要有一种化合物来吸收航天员呼出的CO2,你认为该物质应该是由上表中的___ _(填表中编号)元素组成的,用化学方程式表示吸收原理:_________________ ______ 。
(7)设②的原子序数为Z,则14的原子序数为 (用Z表示)。
考查知识点:根据元素周期表,①比较金属性,非金属性,对应粒子还原性及半径的大小;②判断元素在周期表的位置;③化学键 ④位置确定序数;⑤位置推测用途
| ① | | | | | ||||||||||||||||||||
| | | | | ② | ③ | ④ | ⑤ | | | |||||||||||||||
| ⑥ | | | | | | | | | | | | ⑦ | ⑧ | | ⑨ | ⑩ | 11 | |||||||
| 12 | | | | | | | | | | | | | 13 | | | | | |||||||
| | | | | | | | | | | | | | 14 | | | 15 | | |||||||
| | | | | | | | | | | | | | | | | | | |||||||
①性质 最不活泼的是 ;
②原子半径最小的是(除稀有气体元素) _ 。简单阴离子半径最大的是 。
③形成的气态氢化物最稳定的是 ;
④最高价氧化物对应的水化物酸性最强的是 ,
⑤在⑤⑩15三种元素形成的阴离子中还原性最强的是 ,
⑥可作半导体的是 (填表中编号)
(2)用电子式表示②与④形成的化合物的形成过程 __。
(3)⑨与12形成的化合物溶于水所克服的微粒间作用力为 。
(4)13在元素周期表中的位置是 ,元素③形成的单质的结构式为 。
(5)________(填化学式)的单质既可以和盐酸又可以和氢氧化钠溶液反应,其单质与氢氧化钠溶液反应的离子方程式是___________________________________________。
(6) “神舟”六号载人飞船内需要有一种化合物来吸收航天员呼出的CO2,你认为该物质应该是由上表中的___ _(填表中编号)元素组成的,用化学方程式表示吸收原理:_________________ ______ 。
(7)设②的原子序数为Z,则14的原子序数为 (用Z表示)。
考查知识点:根据元素周期表,①比较金属性,非金属性,对应粒子还原性及半径的大小;②判断元素在周期表的位置;③化学键 ④位置确定序数;⑤位置推测用途
(15分)[物质结构与性质]
I . 固体二氧化碳外形似冰,受热汽化无液体产生,俗称“干冰”,根据干冰晶胞结构回答:
(1)干冰中一个分子周围有__________个紧邻分子。
(2)堆积方式与干冰晶胞类型相同的金属有_________(从“Cu、Mg、K、Po”中选出正确的),其空间利用率为_______。
(3)CO2中心原子的杂化方式为_______,有一种与CO2互为等电子体的离子,能用于鉴别Fe3+ ,写出其电子式______________________。
II. 钇钡铜氧的晶胞结构如图。研究发现,此高温超导体中的铜元素有两种价态,+2价和+3价。
(4)写出Cu3+的电子排布式: 。
(5)根据图示晶胞结构,推算晶体中Y,Cu,Ba和O原子个数比,确定其化学式为: 。
(6)根据(5)所推出的化合物的组成,(该化合物中各元素的化合价为Y +3、Ba +2),计算该物质中+2价和+3价的Cu离子个数比为:_______________。
查看习题详情和答案>>