网址:http://m.1010jiajiao.com/timu3_id_341879[举报]
实验室以空气(O2体积分数20%)为原料,在无碳、无水的环境下,用下图A装置制备臭氧(3O2 2O3)。
2O3)。
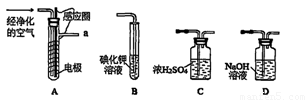
(1)空气通入A装置之前,应先后通过上述装置中的 、 (填装置序号)。
(2)臭氧与碘化钾溶液反应为:2KI+O3+H2O=2KOH+I2+O2。将a处气体通入装置B,溶液中的现象为 。
(3)为测定O2转化为O3的转化率,将装置B中的溶液全部转入另一容器中,加入CC14,经萃取、分液、蒸馏、冷却、称重,得I2固体0.254g。
①萃取操作所用玻璃仪器的名称 。
②若实验时通入空气1.12L(标准状况),O2的转化率为 。
③测定时需在A、B装置间连接装置D,原因是 。
(4)工业上分离O3和O2,可将混合气体液化后再分离,下列分离方法合理的是 (填序号)。
A.过滤 B.分馏 C.分液 D.萃取
(5)臭氧可用于含CN一碱性电镀废水的处理。第i步:CN一转化为OCN-;第ii步:OCN一继续转化为CO32一及两种单质气体。若第ii步转化时,O3与OCN-物质的质量之比为3∶2,该步反应的离子方程式为 。
查看习题详情和答案>>
实验室以空气(O2体积分数20%)为原料,在无碳、无水的环境下,用下图A装置制备臭氧(3O2 2O3)。
2O3)。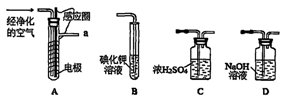
(1)空气通入A装置之前,应先后通过上述装置中的 、 (填装置序号)。
(2)臭氧与碘化钾溶液反应为:2KI+O3+H2O=2KOH+I2+O2。将a处气体通入装置B,溶液中的现象为 。
(3)为测定O2转化为O3的转化率,将装置B中的溶液全部转入另一容器中,加入CC14,经萃取、分液、蒸馏、冷却、称重,得I2固体0.254g。
①萃取操作所用玻璃仪器的名称 。
②若实验时通入空气1.12L(标准状况),O2的转化率为 。
③测定时需在A、B装置间连接装置D,原因是 。
(4)工业上分离O3和O2,可将混合气体液化后再分离,下列分离方法合理的是 (填序号)。
A.过滤 B.分馏 C.分液 D.萃取
(5)臭氧可用于含CN一碱性电镀废水的处理。第i步:CN一转化为OCN-;第ii步:OCN一继续转化为CO32一及两种单质气体。若第ii步转化时,O3与OCN-物质的质量之比为3∶2,该步反应的离子方程式为 。
 2O3)。
2O3)。
(1)空气通入A装置之前,应先后通过上述装置中的 、 (填装置序号)。
(2)臭氧与碘化钾溶液反应为:2KI+O3+H2O=2KOH+I2+O2。将a处气体通入装置B,溶液中的现象为 。
(3)为测定O2转化为O3的转化率,将装置B中的溶液全部转入另一容器中,加入CC14,经萃取、分液、蒸馏、冷却、称重,得I2固体0.254g。
①萃取操作所用玻璃仪器的名称 。
②若实验时通入空气1.12L(标准状况),O2的转化率为 。
③测定时需在A、B装置间连接装置D,原因是 。
(4)工业上分离O3和O2,可将混合气体液化后再分离,下列分离方法合理的是 (填序号)。
A.过滤 B.分馏 C.分液 D.萃取
(5)臭氧可用于含CN一碱性电镀废水的处理。第i步:CN一转化为OCN-;第ii步:OCN一继续转化为CO32一及两种单质气体。若第ii步转化时,O3与OCN-物质的质量之比为3∶2,该步反应的离子方程式为 。
某兴趣小组探究以卤水为原料制取Br2原理.
(1)甲同学设计以卤水为原料制取Br2实验,流程如图1,其中操作1使用的试剂是______,所用的玻璃仪器名称是______.
(2)要想除去液溴中少量Cl2,可在液溴中加入______(填序号)后再萃取分液即可.
①亚硫酸钠溶液 ②浓NaOH溶液 ③氢溴酸
(3)乙同学提出工业从海水中提取溴的过程如图2,其中操作1已获得Br2,操作2又将Br2还原为Br-,其目的为______.

(4)上述操作2用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为______,由此反应可知,除环境保护外,在工业生产中应解决的主要问题是______.为了解从工业溴中提纯溴的方法,他们查阅了有关资料见下表,后设计实验装置如下图:
| 溴 | 物理性质 | 暗红色液体,刺激性气味.室温下易挥发.熔点-7.2℃,沸点59.1℃.密度2.928g?cm-3.稍溶于冷水. |
| 化学性质 | 溶于水生成次溴酸 |

(5)蒸馏装置连接部分都用磨口玻璃接口,而不用橡胶管和橡胶塞连接,是因为:______,图中仪器B的名称:______.
(6)实验装置气密性良好,要达到提纯溴的目的,操作中如何控制关键条件:______.C中液体产物颜色为______. 查看习题详情和答案>>
(1)甲同学设计以卤水为原料制取Br2实验,流程如图1,其中操作1使用的试剂是______,所用的玻璃仪器名称是______.
(2)要想除去液溴中少量Cl2,可在液溴中加入______(填序号)后再萃取分液即可.
①亚硫酸钠溶液 ②浓NaOH溶液 ③氢溴酸
(3)乙同学提出工业从海水中提取溴的过程如图2,其中操作1已获得Br2,操作2又将Br2还原为Br-,其目的为______.

(4)上述操作2用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为______,由此反应可知,除环境保护外,在工业生产中应解决的主要问题是______.为了解从工业溴中提纯溴的方法,他们查阅了有关资料见下表,后设计实验装置如下图:
| 溴 | 物理性质 | 暗红色液体,刺激性气味.室温下易挥发.熔点-7.2℃,沸点59.1℃.密度2.928g?cm-3.稍溶于冷水. |
| 化学性质 | 溶于水生成次溴酸 |

(5)蒸馏装置连接部分都用磨口玻璃接口,而不用橡胶管和橡胶塞连接,是因为:______,图中仪器B的名称:______.
(6)实验装置气密性良好,要达到提纯溴的目的,操作中如何控制关键条件:______.C中液体产物颜色为______.