摘要:氧化性.还原性强弱的判断 (1)氧化性.还原性的强弱取决于得.失电子的难易程度.与得.失电子数目的多少无关.如:Na-e_-------Na+, Al-3e――――Al3+.但根据金属活动表.Na比Al活泼.更易失去电子.所以Na比Al的还原性强. 从元素的价态考虑:最高价态___只有氧化性.如Fe3+.H2SO4.KMnO4等, 最低价态___只有还原性.如金属单质.Cl-.S2_等, 中间价态___既有氧化性又有还原性.如Fe2+.S.Cl2等 (2)常用判断方法 ①根据金属活泼性判断: 金属性越强.单质的还原性越强.其对应离子的氧化性越弱. 单质还原性:按金属活动性顺序表的顺序依次减弱. 离子氧化性:按金属活动性顺序表的顺序依次增强(铁指Fe2+). 如氧化性:Ag+>Hg2+>Fe3+>Cu2+>H+>Fe2+ ②根据非金属的活泼性判断: 非金属性越强.单质的氧化性越强.其对应离子的还原性越弱. 单质氧化性:F2>Cl2>Br2>I2>S 离子还原性:S2_>I->Br->Cl->F- ③通过化学反应比较:氧化剂+还原剂氧化产物+还原产物 氧化性:氧化剂>氧化产物 还原性:还原剂>还原产物 ④通过与同一物质反应的产物比较:如:2Fe+3Cl2 ======2FeCl3 .Fe+S======FeS .可得出氧化性Cl2 >S. ⑤由反应条件的难易比较: 不同氧化剂与同一还原剂反应.反应条件越易.氧化性越强,不同还原剂与同一氧化剂反应.条件越易.还原性越强.如卤素单质与H2的反应.按F2.Cl2.Br2.I2的顺序反应越来越难.反应条件要求越来越高.则可得出氧化性F2>Cl2 >Br2 >I2 . ⑥对同一元素而言.一般价态越高.氧化性越强.如Fe3+>Fe2+>Fe,价态越低.氧化性越弱.如S2―<S<SO2.(特例:氧化性HClO>HClO2>HClO3>HClO4 ) ⑦某些氧化剂的氧化性和还原剂的还原性与下列因素有关: 温度:如浓H2SO4具有强氧化性.热的浓H2SO4比冷的浓H2SO4氧化性要强. 浓度:如硝酸具有强氧化性.硝酸越浓其氧化性越强. 酸碱性:如KMnO4的氧化性随溶液酸性的增强而增强.(一般地.在酸性环境中.KMnO4的还原产物为Mn2+,在中性环境中.KMnO4的还原产物为MnO2,在碱性环境中.KMnO4的还原产物为K2MnO4 .)
网址:http://m.1010jiajiao.com/timu3_id_341740[举报]
氧化还原反应中有这样一个规律:一种氧化剂和不同种还原剂发生氧化还原反应时,该氧化剂应与还原 性最强的物质先反应,而后才能与还原性较弱的物质反应;同理,一种还原剂和不同种氧化剂发生氧化 还原反应时,该还原剂应与氧化性最强的物质先反应,而后才能与氧化性较弱的物质反应。有同学为便于记忆,把这个规律叫做“强强联手”。
(1)实验室有FeCl3、CuCl2、FeCl2的混合溶液,其中Fe3+、Cu2+和Fe2+的物质的量之比为3:2:1,现加入适量铁粉,请写出溶液中可能发生的离子反应: _________________________________。 根据上述离子反应判断三种金属阳离子的氧化性强弱顺序为_______________,当向混合液中加入铁粉时,首先与铁发生反应的离子是________。
(2)加入适量铁粉后,最后溶液中Fe3+、Cu2+和Fe2+的物质的量之比变为1:2:4,则参加反应的铁粉与原溶液Fe2+的物质的量之比为____。
查看习题详情和答案>>
(1)实验室有FeCl3、CuCl2、FeCl2的混合溶液,其中Fe3+、Cu2+和Fe2+的物质的量之比为3:2:1,现加入适量铁粉,请写出溶液中可能发生的离子反应: _________________________________。 根据上述离子反应判断三种金属阳离子的氧化性强弱顺序为_______________,当向混合液中加入铁粉时,首先与铁发生反应的离子是________。
(2)加入适量铁粉后,最后溶液中Fe3+、Cu2+和Fe2+的物质的量之比变为1:2:4,则参加反应的铁粉与原溶液Fe2+的物质的量之比为____。
在氧化还原反应中,氧化过程和还原过程是同时发生的两个半反应.Cu2O-2e-+2H+═2Cu2++H2O是一个半反应式.下列五种物质FeSO4、Fe2(SO4)3、CuSO4、Na2CO3、KI中的一种能使上述半反应顺利发生.
(1)写出并配平该氧化还原反应的离子方程式:______.
(2)向(1)中反应后的溶液里加入酸性高锰酸钾溶液,得还原产物Mn2+(无色),反应的离子方程式为______;判断Cu2+、MnO-、Fe3+的氧化性由强到弱的顺序是______(用离子符号表示).
(3)某同学用上述原理测定一种含Cu2O的矿石中Cu2O的质量分数:称量5.0g矿石溶于足量的硫酸铁和硫酸的混合溶液中,充分反应后,用酸性高锰酸钾溶液滴定,消耗0.100 0mol?L-1的高锰酸钾溶液的体积为100.00mL.
①滴定时,滴定终点的颜色为______.
②该同学测得矿石样品中Cu2O的质量分数为______.
③下列情况使测定结果一定偏高的是______.
A.开始和终点都是仰视读数
B.没有用待装液润洗滴定管
C.称量时,砝码与样品放反了
D.样品中含有较强还原性杂质
E.高锰酸钾溶液中含有N
F.用酸性高锰酸钾溶液润洗锥形瓶.
查看习题详情和答案>>
(1)写出并配平该氧化还原反应的离子方程式:______.
(2)向(1)中反应后的溶液里加入酸性高锰酸钾溶液,得还原产物Mn2+(无色),反应的离子方程式为______;判断Cu2+、MnO-、Fe3+的氧化性由强到弱的顺序是______(用离子符号表示).
(3)某同学用上述原理测定一种含Cu2O的矿石中Cu2O的质量分数:称量5.0g矿石溶于足量的硫酸铁和硫酸的混合溶液中,充分反应后,用酸性高锰酸钾溶液滴定,消耗0.100 0mol?L-1的高锰酸钾溶液的体积为100.00mL.
①滴定时,滴定终点的颜色为______.
②该同学测得矿石样品中Cu2O的质量分数为______.
③下列情况使测定结果一定偏高的是______.
A.开始和终点都是仰视读数
B.没有用待装液润洗滴定管
C.称量时,砝码与样品放反了
D.样品中含有较强还原性杂质
E.高锰酸钾溶液中含有N
| O | -3 |
F.用酸性高锰酸钾溶液润洗锥形瓶.
在氧化还原反应中,氧化过程和还原过程是同时发生的两个半反应.Cu2O-2e-+2H+═2Cu2++H2O是一个半反应式.下列五种物质FeSO4、Fe2(SO4)3、CuSO4、Na2CO3、KI中的一种能使上述半反应顺利发生.
(1)写出并配平该氧化还原反应的离子方程式: .
(2)向(1)中反应后的溶液里加入酸性高锰酸钾溶液,得还原产物Mn2+(无色),反应的离子方程式为 ;判断Cu2+、MnO-、Fe3+的氧化性由强到弱的顺序是 (用离子符号表示).
(3)某同学用上述原理测定一种含Cu2O的矿石中Cu2O的质量分数:称量5.0g矿石溶于足量的硫酸铁和硫酸的混合溶液中,充分反应后,用酸性高锰酸钾溶液滴定,消耗0.100 0mol?L-1的高锰酸钾溶液的体积为100.00mL.
①滴定时,滴定终点的颜色为 .
②该同学测得矿石样品中Cu2O的质量分数为 .
③下列情况使测定结果一定偏高的是 .
A.开始和终点都是仰视读数
B.没有用待装液润洗滴定管
C.称量时,砝码与样品放反了
D.样品中含有较强还原性杂质
E.高锰酸钾溶液中含有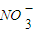
F.用酸性高锰酸钾溶液润洗锥形瓶. 查看习题详情和答案>>
(1)写出并配平该氧化还原反应的离子方程式: .
(2)向(1)中反应后的溶液里加入酸性高锰酸钾溶液,得还原产物Mn2+(无色),反应的离子方程式为 ;判断Cu2+、MnO-、Fe3+的氧化性由强到弱的顺序是 (用离子符号表示).
(3)某同学用上述原理测定一种含Cu2O的矿石中Cu2O的质量分数:称量5.0g矿石溶于足量的硫酸铁和硫酸的混合溶液中,充分反应后,用酸性高锰酸钾溶液滴定,消耗0.100 0mol?L-1的高锰酸钾溶液的体积为100.00mL.
①滴定时,滴定终点的颜色为 .
②该同学测得矿石样品中Cu2O的质量分数为 .
③下列情况使测定结果一定偏高的是 .
A.开始和终点都是仰视读数
B.没有用待装液润洗滴定管
C.称量时,砝码与样品放反了
D.样品中含有较强还原性杂质
E.高锰酸钾溶液中含有
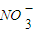
F.用酸性高锰酸钾溶液润洗锥形瓶. 查看习题详情和答案>>