网址:http://m.1010jiajiao.com/timu3_id_341345[举报]
Ⅰ.应用其不稳定性,H2O2可被用来研究催化剂对反应速率的影响.
(1)写出H2O2在MnO2催化下分解的化学方程式
| ||
| ||
(2)H2O2生产过程要严格避免混入Fe2+和Fe3+,否则会发生如下两个反应,加快其分解,且Fe2+和Fe3+各自的量保持不变.
①2Fe2++H2O2+2H+═2Fe3++2H2O
②
(3)从(1)和(2)分析,在下列哪类元素中寻找H2O2分解的催化剂更有研究价值
a.主族元素b.过度元素c.零族元素
Ⅱ.H2O2的水溶液显弱酸性,写出一个用盐酸制取H2O2的化学方程式
Ⅲ.H2O2在使用中通常不会带来污染.
(1)工业上利用Cl2+H2O2═2HCl+O2除氯,在此反应中被氧化的物质是
(2)消除某废液中氰化物(含CN-),完成下列反应:CN-+H2O2
Ⅳ.实验室常用酸性KMnO4溶液测定H2O2的浓度.
取10.00mLH2O2溶液样品(密度近似为1g/mL)于锥形瓶中,加水到50.00mL,当滴入0.10mol/L KMnO4溶液40.00mL后,到达滴定终点.则原样品中H2O2的质量分数是
(已知:2KMnO4+5H2O2+3H2SO4═K2SO4+2MnSO4+5O2↑+8H2O↑)
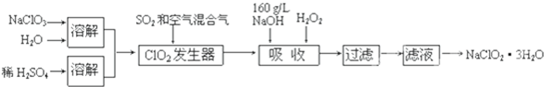
已知:①NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2?3H2O.
②纯ClO2易分解爆炸,一般用稀有气体或空气稀释到10%以下安全.
③160g/L NaOH溶液是指160g NaOH固体溶于水所得溶液的体积为1L.
(1)160g/L NaOH溶液的物质的量浓度为:
(2)发生器中鼓入空气的作用是:
(3)吸收装置内发生反应的化学方程式为:
吸收装置中的温度不能过高,其原因是:
(4)吸收塔中为防止NaClO2被还原成NaCl,所用还原剂的还原性应适中.除H2O2外,还可以选择的还原剂是
(选填序号)a.Na2O2 b.Na2S c.FeCl2
(5)从滤液中得到NaClO2?3H2O粗晶体的实验操作依次是
a.蒸发结晶 b.蒸发浓缩 c.灼烧 d.过滤 e.冷却结晶
2、在氯氧化法处理含CN一的废水过程中,液氯在碱性条件下可以将氰化物氧化成氰酸盐(其毒性仅为氰化物的千分之一),氰酸盐再进一步被氧化为无毒物质.
(1)某厂废水中含KCN,其浓度为650mg?L-1.现用氯氧化法处理,发生如下反应:KCN+2KOH+Cl2=KOCN+2KCl+H2O,再投入过量液氯,可将氰酸盐进一步氯化为氮气.请配平下列化学方程式:
(配平后请在方框内填写每种物质的化学计量数,若为“1”也要写上)
(2)若处理上述废水20L,使KCN完全转化为无毒物质,至少需液氯
 二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂.
二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂.(1)工业上制备ClO2的反应原理常采用:2NaClO3+4HCl=2ClO2↑+Cl2↑+2H2O+2NaCl.
①浓盐酸在反应中显示出来的性质是
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
②若上述反应中产生0.1mol ClO2,则转移电子的物质的量为
(2)目前已开发出用电解法制取ClO2的新工艺.
①如图示意用石墨做电极,在一定条件下电解饱和食盐水制取ClO2.写出阳极产生ClO2的电极反应式:
②电解一段时间,当阴极产生的气体体积为112mL(标准状况)时,停止电解.通过阳离子交换膜的阳离子的物质的量为
(3)ClO2对污水中Fe2+、Mn2+、S2-和CN-等有明显的去除效果.某工厂污水中含CN- a mg/L,现用ClO2将CN-氧化,只生成两种气体,其离子反应方程式为
| 50a |
| 13 |
| 50a |
| 13 |
请回答下列问题:
(1)A、C两元素形成的原子个数比为1:1且呈电中性的微粒的电子式为


(2)A、C、D可形成化合物W,其含有的化学键有
(3)A2和B2在工业上可合成一种重要的原料BA3.
①下列的措施有利于提高B2的转化率的是
A.采用20?50MPa的大气压
B.选用400?500℃的高温
C.使用催化剂
D.及时将BA3液化
②现有甲、乙两个固定体积的容器,在相同的体积和温度下,甲中充入2molBA3,反应达到平衡时,吸收Q1kJ的能量;乙中充入
1mol B2和3mol A2,反应达到平衡时,放出Q2kJ的能量;则合成BA3的热化学方程式为
| 高温高压 |
| 催化剂 |
| 高温高压 |
| 催化剂 |
③现有甲、乙两个体积和温度相同的容器,甲容器维持温度和体积不变,乙容器维持温度和压强不变,甲中充入2mol BA3,乙中充入1mol B2和3mol A2,当反应都达到平衡时,BA3的体积分数甲
(4)化合物甲、乙都由A、B、C三种元素组成,甲为弱碱,乙为强酸;常温下,若两溶液中水的电离程度相同.
①若乙溶液的pH=a,则甲溶液中水电离产生的C(H+)=
(5)用D2C2在酸性条件下处理含CN-的工业废水,将得到一种能够参与大气生态环境循环的气体以及C02等物质,请写出该反应的离子方程式
(15分)氰化物有剧毒,冶金工业会产生大量含氰化物的废水,其中氰化物以CN—等形式存在于废水中。某化学小组同学对含氰化物废水处理进行研究。
I.查阅资料:含氰化物的废水破坏性处理方法。
利用强氧化剂将氰化物氧化为无毒物质,如以TiO2为催化剂用NaClO将CN-离子氧化成CNO-(CN-和CNO-中N元素均为-3价),CNO-在酸性条件下继续与NaClO反应生成N2、CO2、Cl2等。
II.实验验证:破坏性处理CN-的效果。
化学兴趣小组的同学在密闭系统中用图10装置进行实验,以测定CN-被处理的百分率,实验步骤如下:
步骤1:取一定量废水进行加热蒸发、浓缩。
步骤2:取浓缩后含CN-离子的废水与过量NaClO溶液的混合液共200mL(设其中CN-的浓度为0.2mol·L—1)倒入甲中,塞上橡皮塞。
步骤3:
步骤4:打开甲上的橡皮塞和活塞,使甲中溶液全部放入乙中,关闭活塞。
步骤5:打开活塞K,通一段时间N2,关闭活塞K。
步骤6:实验完成后测定干燥管I(含碱石灰)的质量m2(实验前干燥管I(含碱石灰)的质量m1)
回答下列问题:
(1)在破坏性处理方法中,在酸性条件下NaClO和CNO-反应的离子方程式 。
(2)完成步骤3 。
(3)丙装置中的试剂是 ,丁装置的目的是 。
(4)干燥管Ⅱ的作用是 。
(5)请简要说明实验中通入N2的目的是 。
(6)若干燥管Ⅰ中碱石灰增重1.408g,则该实验中测得CN-被处理的百分率为 。