摘要:22.★★★.标准状况下.将下列气体:① HCI ② CI2 ③ NH3 ④ NO⑤ N2O4⑥ NO2与O2的体积比为4:1的混合气体.分别装满试管.倒立与水面上.并充分光照.假如溶质不向外扩散.则所得溶液中溶质的物质的量浓度: (1) 物质的量浓度最大的是 为 moI/L (2) 物质的量浓度最小的是 为 moI/L (3) 物质的量浓度相等的是 为 moI/L
网址:http://m.1010jiajiao.com/timu3_id_341264[举报]
恒温下,将a mol N2与b mol H2的混合气体通入一个固定容积的密闭容器中,发生如下反应:N2(g)+3H2(g)?2NH3(g),反应达平衡时,混合气体的体积为716.8L(标准状况下),其中NH3的含量(体积分数)为25%.计算:
(1)达到平衡时,消耗N2的物质的量,n(N2)=
(2)原混合气体与平衡混合气体的压强之比(写出最简整数比),p(始):p(平)=
查看习题详情和答案>>
(1)达到平衡时,消耗N2的物质的量,n(N2)=
16mol
16mol
(2)原混合气体与平衡混合气体的压强之比(写出最简整数比),p(始):p(平)=
5:4
5:4
.A-F 6种有机物,在一定条件下,按图发生转化.又知烃A的密度(在标准状况下)是氢气的13倍,试回答下列问题:
(1)A.
(2)反应C→D的化学方程式是

查看习题详情和答案>>
(1)A.
CH≡CH
CH≡CH
,B.CH2═CH2
CH2═CH2
,D.CH3CHO
CH3CHO
.(填结构简式)(2)反应C→D的化学方程式是
2CH3CH2OH+O2
2CH3CHO+2H2O
| Cu |
| 催化剂 |
2CH3CH2OH+O2
2CH3CHO+2H2O
;该反应属于| Cu |
| 催化剂 |
氧化
氧化
反应;反应E+C→F的化学方程式是CH3CH2OH+CH3COOH
CH3COOCH2CH3+H2O
| 浓硫酸 |
CH3CH2OH+CH3COOH
CH3COOCH2CH3+H2O
| 浓硫酸 |

可利用下图中的实验装置测定足量铜与适量一定浓度的浓硝酸反应生成的NO气体和NO2气体的物质的量之比(用m表示),其中装置C由广口瓶和量气管组成,量气管由甲、乙两根玻璃管组成,用橡皮管连通,并装入适量水,甲管有刻度(0mL~50mL),乙管可上下移动.回答下列问题:
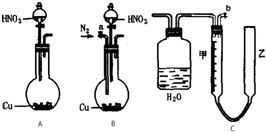
(1)实验中气体(NO和NO2)发生装置应选择
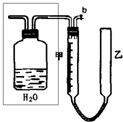
(2)实验中的气体(NO和NO2)通入C装置,请在下图的广口瓶中将导气管画出.
(3)要测定m值,需要将C中的溶液进行中和滴定,由于浓硝酸具有强氧化性,能把酸碱指示剂氧化褪色而影响实验.因此,中和滴定前必须进行的操作是
(4)连接好装置,检查气密性后,应进行两步必要的操作:第一,打开b,向C装置的乙管中加适量水;第二,
(5)实验前甲、乙两管液面在同一水平面上,最后读数时乙管的液面高于甲管的液面.此时应进行的操作是
(6)实验后若量气管中气体的体积(换算成标准状况下)为V(L),C中硝酸的物质的量为 n mol,则用含n和V的式子表示m=
查看习题详情和答案>>

(1)实验中气体(NO和NO2)发生装置应选择
B
B
(填装置序号).(2)实验中的气体(NO和NO2)通入C装置,请在下图的广口瓶中将导气管画出.

(3)要测定m值,需要将C中的溶液进行中和滴定,由于浓硝酸具有强氧化性,能把酸碱指示剂氧化褪色而影响实验.因此,中和滴定前必须进行的操作是
将C中的溶液加适量水稀释
将C中的溶液加适量水稀释
.(4)连接好装置,检查气密性后,应进行两步必要的操作:第一,打开b,向C装置的乙管中加适量水;第二,
打开a,通足量N2,排净装置中的空气
打开a,通足量N2,排净装置中的空气
.(5)实验前甲、乙两管液面在同一水平面上,最后读数时乙管的液面高于甲管的液面.此时应进行的操作是
向下移动乙管,使甲、乙两管液面在同一水平面上
向下移动乙管,使甲、乙两管液面在同一水平面上
.(6)实验后若量气管中气体的体积(换算成标准状况下)为V(L),C中硝酸的物质的量为 n mol,则用含n和V的式子表示m=
(V-11.2n):33.6n
(V-11.2n):33.6n
(结果可不必化简).