利峽⦿http://m.1010jiajiao.com/timu3_id_341085[訟烏]
(15蛍)挺殆↙H2NCONH2⇄頁匯嶽掲械嶷勣議互紀晒景⇧垢匍貧栽撹挺殆議郡哘泌和⦿
2NH3(l)⇦CO2(g)  H2O(l)⇦H2NCONH2
(l) @H﹆⇩103.7 kJ,mol⇩1
H2O(l)⇦H2NCONH2
(l) @H﹆⇩103.7 kJ,mol⇩1
編指基和双諒籾⦿
⊋和双企仏嶄嗤旋噐戻互挺殆議恢楕議頁___________。
A⤴寡喘互梁
B⤴寡喘互儿
C⤴儖孀厚互丼議岸晒質
∉栽撹挺殆議郡哘壓序佩扮蛍葎泌和曾化⦿
及匯化⦿2NH3(l)⇦CO2(g)  H2NCOONH4(葦児遮磨錻) (l) @H1
H2NCOONH4(葦児遮磨錻) (l) @H1
及屈化⦿H2NCOONH4(l)
 H2O(l)⇦H2NCONH2(l)
@H2
H2O(l)⇦H2NCONH2(l)
@H2
蝶糞刮弌怏庁亭垢匍貧栽撹挺殆議訳周⇧壓匯悶持葎0.5 L畜液否匂嶄誘秘4 mol葦才1mol屈剳晒娘⇧糞刮霞誼郡哘嶄光怏蛍昧扮寂議延晒泌和夕↔侭幣⦿

〙厮岑悳郡哘議酔蛸喇蛸議匯化畳協⇧夸栽撹挺殆悳郡哘議酔蛸喇及_____化郡哘畳協⇧悳郡哘序佩欺_________min扮欺器峠財。
〖郡哘序佩欺10 min扮霞誼CO2議麗嵎議楚泌夕侭幣⇧夸喘CO2燕幣議及匯化郡哘議堀楕v(CO2)﹆_______________________。
〗及屈化郡哘議峠財械方K昧梁業議延晒泌貧嘔夕Å侭幣⇧夸@H2__________0↙野^﹅ ̄^〽 ̄賜^﹆ ̄⇄
臥心楼籾峋秤才基宛>>
(15蛍)挺殆↙H2NCONH2⇄頁匯嶽掲械嶷勣議互紀晒景⇧垢匍貧栽撹挺殆議郡哘泌和⦿
2NH3(l)⇦CO2(g) H2O(l)⇦H2NCONH2(l) @H﹆⇩103.7 kJ,mol⇩1
編指基和双諒籾⦿
⊋和双企仏嶄嗤旋噐戻互挺殆議恢楕議頁___________。
A⤴寡喘互梁
B⤴寡喘互儿
C⤴儖孀厚互丼議岸晒質
∉栽撹挺殆議郡哘壓序佩扮蛍葎泌和曾化⦿
及匯化⦿2NH3(l)⇦CO2(g) H2NCOONH4(葦児遮磨錻) (l) @H1
及屈化⦿H2NCOONH4(l) H2O(l)⇦H2NCONH2(l) @H2
蝶糞刮弌怏庁亭垢匍貧栽撹挺殆議訳周⇧壓匯悶持葎0.5 L畜液否匂嶄誘秘4 mol葦才1mol屈剳晒娘⇧糞刮霞誼郡哘嶄光怏蛍昧扮寂議延晒泌和夕↔侭幣⦿
〙厮岑悳郡哘議酔蛸喇蛸議匯化畳協⇧夸栽撹挺殆悳郡哘議酔蛸喇及_____化郡哘畳協⇧悳郡哘序佩欺_________min扮欺器峠財。
〖郡哘序佩欺10 min扮霞誼CO2議麗嵎議楚泌夕侭幣⇧夸喘CO2燕幣議及匯化郡哘議堀楕v(CO2)﹆_______________________。
〗及屈化郡哘議峠財械方K昧梁業議延晒泌貧嘔夕Å侭幣⇧夸@H2__________0↙野^﹅ ̄^〽 ̄賜^﹆ ̄⇄
臥心楼籾峋秤才基宛>>
(15蛍)挺殆↙H2NCONH2⇄頁匯嶽掲械嶷勣議互紀晒景⇧垢匍貧栽撹挺殆議郡哘泌和⦿
2NH3(l)⇦CO2(g)H2O(l)⇦H2NCONH2 (l) @H﹆⇩103.7 kJ,mol⇩1
編指基和双諒籾⦿
⊋和双企仏嶄嗤旋噐戻互挺殆議恢楕議頁___________。
A⤴寡喘互梁
B⤴寡喘互儿
C⤴儖孀厚互丼議岸晒質
∉栽撹挺殆議郡哘壓序佩扮蛍葎泌和曾化⦿
及匯化⦿2NH3(l)⇦CO2(g) H2NCOONH4(葦児遮磨錻) (l) @H1
及屈化⦿H2NCOONH4(l)H2O(l)⇦H2NCONH2(l) @H2
蝶糞刮弌怏庁亭垢匍貧栽撹挺殆議訳周⇧壓匯悶持葎0.5 L畜液否匂嶄誘秘4 mol葦才1mol屈剳晒娘⇧糞刮霞誼郡哘嶄光怏蛍昧扮寂議延晒泌和夕↔侭幣⦿
〙厮岑悳郡哘議酔蛸喇蛸議匯化畳協⇧夸栽撹挺殆悳郡哘議酔蛸喇及_____化郡哘畳協⇧悳郡哘序佩欺_________min扮欺器峠財。
〖郡哘序佩欺10 min扮霞誼CO2議麗嵎議楚泌夕侭幣⇧夸喘CO2燕幣議及匯化郡哘議堀楕v(CO2)﹆_______________________。
〗及屈化郡哘議峠財械方K昧梁業議延晒泌貧嘔夕Å侭幣⇧夸@H2__________0↙野^﹅ ̄^〽 ̄賜^﹆ ̄⇄
臥心楼籾峋秤才基宛>>
(15蛍)挺殆↙H2NCONH2⇄頁匯嶽掲械嶷勣議互紀晒景⇧垢匍貧栽撹挺殆議郡哘泌和⦿
2NH3(l)⇦CO2(g)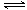 H2O(l)⇦H2NCONH2 (l) @H﹆⇩103.7 kJ,mol⇩1
H2O(l)⇦H2NCONH2 (l) @H﹆⇩103.7 kJ,mol⇩1
編指基和双諒籾⦿
⊋和双企仏嶄嗤旋噐戻互挺殆議恢楕議頁___________。
A⤴寡喘互梁
B⤴寡喘互儿
C⤴儖孀厚互丼議岸晒質
∉栽撹挺殆議郡哘壓序佩扮蛍葎泌和曾化⦿
及匯化⦿2NH3(l)⇦CO2(g)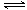 H2NCOONH4(葦児遮磨錻) (l) @H1
H2NCOONH4(葦児遮磨錻) (l) @H1
及屈化⦿H2NCOONH4(l)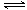 H2O(l)⇦H2NCONH2(l) @H2
H2O(l)⇦H2NCONH2(l) @H2
蝶糞刮弌怏庁亭垢匍貧栽撹挺殆議訳周⇧壓匯悶持葎0.5 L畜液否匂嶄誘秘4 mol葦才1mol屈剳晒娘⇧糞刮霞誼郡哘嶄光怏蛍昧扮寂議延晒泌和夕↔侭幣⦿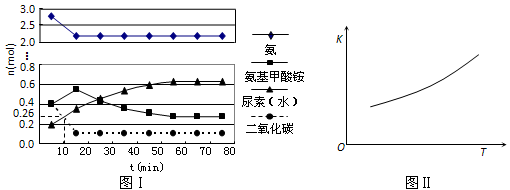
〙厮岑悳郡哘議酔蛸喇蛸議匯化畳協⇧夸栽撹挺殆悳郡哘議酔蛸喇及_____化郡哘畳協⇧悳郡哘序佩欺_________min扮欺器峠財。
〖郡哘序佩欺10 min扮霞誼CO2議麗嵎議楚泌夕侭幣⇧夸喘CO2燕幣議及匯化郡哘議堀楕v(CO2)﹆_______________________。
〗及屈化郡哘議峠財械方K昧梁業議延晒泌貧嘔夕Å侭幣⇧夸@H2__________0↙野^﹅ ̄^〽 ̄賜^﹆ ̄⇄
↙10蛍⇄
I.(4蛍)蝶梁業和議卑匣嶄⇧c(H⇦)=10x mol/L,c(OH⇩)=10y mol/L。x嚥y議購狼泌夕侭幣⦿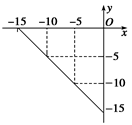
↙1⇄乎梁業和,嶄來卑匣議pH= 。
↙2⇄乎梁業和0.01 mol/L NaOH卑匣議pH= 。
II. (6蛍)蝶冩梢弌怏壓糞刮片冥梢葦児遮磨錻↙NH2COONH4⇄蛍盾郡哘峠財械方才邦盾郡哘堀楕議霞協。
↙1⇄繍匯協楚歓昌議葦児遮磨錻崔噐蒙崙議畜液寔腎否匂嶄(邪譜否匂悶持音延⇧耕悶編劔悶持策待音柴)⇧壓冴協梁業和聞凪器欺蛍盾峠財⦿NH2COONH4(s)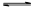 2NH3(g)⇦CO2(g)。糞刮霞誼音揖梁業和議峠財方象双噐和燕⦿
2NH3(g)⇦CO2(g)。糞刮霞誼音揖梁業和議峠財方象双噐和燕⦿
| 梁業(≧) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 峠財悳儿膿(kPa) | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
| 峠財賑悶悳敵業 (〜10⇩3mol/L) | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
A⤴2v(NH3)=v(CO2) B⤴畜液否匂嶄悳儿膿音延
C⤴畜液否匂嶄詞栽賑悶議畜業音延 D⤴畜液否匂嶄葦賑議悶持蛍方音延
〖功象燕嶄方象⇧柴麻25.0≧扮議蛍盾峠財械方葎 。
↙2⇄厮岑⦿NH2COONH4⇦2H2O
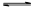 NH4HCO3⇦NH3,H2O。乎冩梢弌怏蛍艶喘眉芸音揖兜兵敵業議葦児遮磨錻卑匣霞協邦盾郡哘堀楕⇧誼欺c(NH2COO⇩)昧扮寂延晒迫米泌夕侭幣。
NH4HCO3⇦NH3,H2O。乎冩梢弌怏蛍艶喘眉芸音揖兜兵敵業議葦児遮磨錻卑匣霞協邦盾郡哘堀楕⇧誼欺c(NH2COO⇩)昧扮寂延晒迫米泌夕侭幣。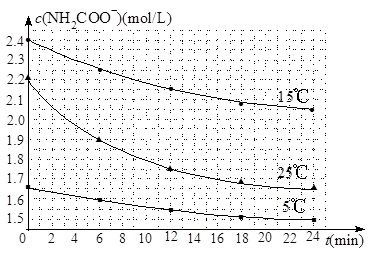
〗柴麻25≧扮⇧0゛6min葦児遮磨錻邦盾郡哘議峠譲堀楕葎 。
∠功象夕嶄佚連⇧泌採傍苧邦盾郡哘議峠譲堀楕昧梁業幅互遇奐寄⦿
。 臥心楼籾峋秤才基宛>>