摘要:3.对试剂瓶的要求 ①一般固体物质保存在广口瓶中.便于用镊子取用. ②一般液体及挥发性物质保存在细口瓶中 ③见光易分解的试剂应保存在棕色瓶中.如:浓HNO3.硝酸银.卤化银.氯水.溴水.碘水和某些有机物试剂.
网址:http://m.1010jiajiao.com/timu3_id_340824[举报]
(2013?江门一模)某工厂废液中含有苯酚、乙酸苯酚酌,实验小组对该废液进行探究,设计如图方案:

己知熔点:乙酸16.6℃、苯酚43℃.沸点:乙酸118℃、苯酚182℃.
(1)写出②的反应化学方程式 +CO2+H2O→
+CO2+H2O→ +NaHCO3;
+NaHCO3; +CO2+H2O→
+CO2+H2O→ +NaHCO3;
+NaHCO3;
(2)②中分离B的操作名称是
(3)现对物质C的性质进行实验探究,请你帮助实验小组按要求完成实验过程记录,在答题卡上填写出实验操作、预期现象和现象解释.
限选试剂:蒸馏水、稀HN03、2moL?L-1 NaOH、0.1mol-L-1 KSCN、酸性KMn04溶液、FeCl3溶液、饱和浪水、紫色石蕊试液.
(4)称取一定量的C试样,用水溶解后全部转移至1000mL容量瓶中定容.取此溶液.25.OOmL,加入KBr03浓度为0.01667moL?L-1,的KBr03+ KBr标准溶液30.OOmL,酸化并放置.待反应完全后,加入过量的KI,再用0.1100moL-L-1,Na2S203标准溶液滴成的12,耗去Na2S203标准溶液11.80mL o则试样中C物质的量的计算表达式为:
(3×0.01667moL?L-1×30.OO×10-3L-
×0.1100mol/Lx11.80x10-3L)×
,
(3×0.01667moL?L-1×30.OO×10-3L-
×0.1100mol/Lx11.80x10-3L)×
,
(部分反应离子方程式:)BrO
+5Br-+6H+═3Br2+3H2O;I2+2S2O
═2I-+S4O
.
查看习题详情和答案>>

己知熔点:乙酸16.6℃、苯酚43℃.沸点:乙酸118℃、苯酚182℃.
(1)写出②的反应化学方程式
 +CO2+H2O→
+CO2+H2O→ +NaHCO3;
+NaHCO3; +CO2+H2O→
+CO2+H2O→ +NaHCO3;
+NaHCO3;(2)②中分离B的操作名称是
分液
分液
(3)现对物质C的性质进行实验探究,请你帮助实验小组按要求完成实验过程记录,在答题卡上填写出实验操作、预期现象和现象解释.
| 实验操作 | 预期现象 | 现象解释 |
| 步骤1:取少量C放入a试管,加入少量蒸馏水,震荡. | 出现白色浑浊 出现白色浑浊 |
苯酚常温下溶解度不大 苯酚常温下溶解度不大 |
| 步骤2:取少量C的稀溶液分装b、c两只试管,往b试管 滴入过量饱和溴水,振荡. 滴入过量饱和溴水,振荡. |
产生白色沉淀 | 苯酚与溴发生取代反应,生成三溴苯酚白色沉淀. 苯酚与溴发生取代反应,生成三溴苯酚白色沉淀. |
| 步骤3:往c试管 滴入几滴FeCl3溶液,振荡 滴入几滴FeCl3溶液,振荡 |
溶液变为紫色 溶液变为紫色 |
C与加入的试剂发生显色反应. |
(4)称取一定量的C试样,用水溶解后全部转移至1000mL容量瓶中定容.取此溶液.25.OOmL,加入KBr03浓度为0.01667moL?L-1,的KBr03+ KBr标准溶液30.OOmL,酸化并放置.待反应完全后,加入过量的KI,再用0.1100moL-L-1,Na2S203标准溶液滴成的12,耗去Na2S203标准溶液11.80mL o则试样中C物质的量的计算表达式为:
| 1 |
| 3 |
| 1 |
| 2 |
| 1000mL |
| 25.00mL |
| 1 |
| 3 |
| 1 |
| 2 |
| 1000mL |
| 25.00mL |
(部分反应离子方程式:)BrO
- 3 |
2- 3 |
2- 6 |
 用98%的浓H2SO4(ρ=1.84g/cm3)配制480mL0.5mol/L的稀H2SO4,请按要求填空:
用98%的浓H2SO4(ρ=1.84g/cm3)配制480mL0.5mol/L的稀H2SO4,请按要求填空:(1)所用浓H2SO4的物质的量浓度为
18.4mol/L
18.4mol/L
,配制时所需浓硫酸的体积为5.4
5.4
mL.(均保留一位小数)(2)实验中需要用到的定量仪器有
10mL量筒、500mL容量瓶
10mL量筒、500mL容量瓶
.(3)实验中玻璃棒的作用
搅拌、引流
搅拌、引流
(4)若实验中出现下列现象,对所配溶液的浓度有什么影响?(填“偏高”、“偏低”或“无影响”)
①用量筒量取所需浓硫酸倒入烧杯后,再用水洗量筒2~3次,洗液倒入烧杯中
偏高
偏高
②浓硫酸溶解后未冷至室温即进行转移、定容.
偏高
偏高
③定容时仰视刻度线.
偏低
偏低
(5)若定容时液面高于刻度线应采取的措施是
重新配制
重新配制
.(6)若实验操作全部无误,最后所得的溶液应存放在试剂瓶中,并贴上标签,请你帮助把标签上的内容写一下(如下图)


 用98%的浓H2SO4(ρ=1.84g/cm3)配制 240mL0.5mol/L的稀H2SO4,请按要求填空:
用98%的浓H2SO4(ρ=1.84g/cm3)配制 240mL0.5mol/L的稀H2SO4,请按要求填空:(1)请写出该实验的实验步骤
①
计算
计算
,②量取
量取
,③溶解转移
溶解转移
,④洗涤转移
洗涤转移
,⑤定容摇匀
定容摇匀
.(2)所用浓H2SO4的物质的量浓度为
18.4mol/L
18.4mol/L
,配制时所需浓硫酸的体积为6.8
6.8
mL.(均保留一位小数)(3)实验中需要用到的定量仪器有(包括规格)
10mL量筒、250mL容量瓶
10mL量筒、250mL容量瓶
(4)若实验中出现下列现象对所配溶液的浓度有什么影响?(填“偏高”、“偏低”或“无影响”)
①浓硫酸溶解后未冷至室温即进行转移、定容.(
偏高
偏高
)②定容时俯视刻度线.(偏高
偏高
)(5)若定容时液面高于刻度线应采取的措施是
重新配制
重新配制
.(6)若实验操作全部无误,最后所得的溶液应存放在试剂瓶中,并贴上标签,请你帮助把标签上的内容写一下(如图).


实验室有一瓶Na2SO3固体,可能含有NaCl、Na2SO4、BaCl2、K2CO3、K2SO4中的一种或几种杂质,通过下列实验确定该样品的成分及Na2SO3的质量分数.
①取少量样品于试管中,加水振荡,未见沉淀生成;
②透过蓝色钴玻璃观察,焰色反应无紫色;
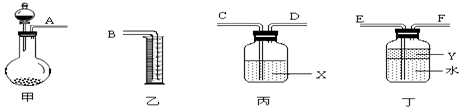
③用右图所示仪器进行合理组装,测定产生气体的体积(SO2在硫酸中的溶解忽略不计)
请回答下列问题:
(1)按气流从左到右方向,正确的连接顺序为:A接 , 接 , 接B.
(2)利用所组装置,由分液漏斗向圆底烧瓶中滴加10mL水,将排入量筒中 mL液体.
(3)液体X是 ,其作用是 .
(4)Y的作用是防止产生的气体溶于水,下列所给试剂符合要求的是 .
A.苯B.四氯化碳C.酒精D.汽油
若称取样品3.00g,加入10.0mol/L的硫酸至过量(共5mL),产生无色气体,排入量筒中液体的体积为229mL(标准状况).
(5)对获得准确的气体体积无益的操作有 (填序号)
①检查装置的气密性;
②连通乙、丁的导管要预先注满水;
③读数时视线与量筒内凹液面最低点相平;
④恢复到室温后再上下调整量筒位置,使乙、丁两液面相平;
⑤在甲装置胶塞上再连接一个导管,通入N2将系统中SO2全部排出.
(6)向逸出气体后的溶液中加入稍过量的BaCl2溶液,过滤、洗涤、干燥,得到白色沉淀13.98g.根据实验所得现象及数据,可知:样品中Na2SO3的质量分数是 ,含有的杂质是 .
查看习题详情和答案>>

①取少量样品于试管中,加水振荡,未见沉淀生成;
②透过蓝色钴玻璃观察,焰色反应无紫色;
③用右图所示仪器进行合理组装,测定产生气体的体积(SO2在硫酸中的溶解忽略不计)
请回答下列问题:
(1)按气流从左到右方向,正确的连接顺序为:A接
(2)利用所组装置,由分液漏斗向圆底烧瓶中滴加10mL水,将排入量筒中
(3)液体X是
(4)Y的作用是防止产生的气体溶于水,下列所给试剂符合要求的是
A.苯B.四氯化碳C.酒精D.汽油
若称取样品3.00g,加入10.0mol/L的硫酸至过量(共5mL),产生无色气体,排入量筒中液体的体积为229mL(标准状况).
(5)对获得准确的气体体积无益的操作有
①检查装置的气密性;
②连通乙、丁的导管要预先注满水;
③读数时视线与量筒内凹液面最低点相平;
④恢复到室温后再上下调整量筒位置,使乙、丁两液面相平;
⑤在甲装置胶塞上再连接一个导管,通入N2将系统中SO2全部排出.
(6)向逸出气体后的溶液中加入稍过量的BaCl2溶液,过滤、洗涤、干燥,得到白色沉淀13.98g.根据实验所得现象及数据,可知:样品中Na2SO3的质量分数是
(21分)用98%的浓H2SO4(ρ=1.84g/cm3)配制 240mL0.5mol/L的稀H2SO4,请按要求填空:
(1)请写出该实验的实验步骤
① ,② ,③ ,④ ,⑤ 。
(2)所用浓H2SO4的物质的量浓度为 ,配制时所需浓硫酸的体积为 mL。(均保留一位小数)
(3)实验中需要用到的定量仪器有(包括规格)
(4)若实验中出现下列现象对所配溶液的浓度有什么影响?(填“偏高”、“偏低”或“无影响”)
①浓硫酸溶解后未冷至室温即进行转移、定容。( )
②定容时俯视刻度线。( )
(5)若定容时液面高于刻度线应采取的措施是 。
(6)若实验操作全部无误,最后所得的溶液应存放在试剂瓶中,并贴上标签,请你帮助把标签上的内容写一下(如右图)。

查看习题详情和答案>>