网址:http://m.1010jiajiao.com/timu3_id_339779[举报]
(10分)
(1)在上面元素周期表中全部是金属元素的区域为___________。
| A.a | B.b | C.c | D.d |
该化合物的电子式是 。
(3)表格中九种元素能形成最高价氧化物对应的水化物中,碱性最强的是________(用化合物的化学式表示,下同),酸性最强的是__________,属于两性氢氧化物的是__________。
(4)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等。
①用元素符号将甲、乙两元素填写在上面元素周期表中对应的位置。
②甲、乙两元素相比较,金属性较强的是 ________(填名称),可以验证该结论的实验是_______。(填编号)
a将在空气中放置已久的这两种元素的块状单质分别放入热水中;
b将这两种元素的单质粉末分别和同浓度的盐酸反应;
c将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液;
d比较这两种元素的气态氢化物的稳定性。 查看习题详情和答案>>
部分阳离子以氢氧化物沉淀时溶液pH
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mg(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 11.2 |
| 温度0C | 10 | 30 | 40 |
| CaSO4 | 0.19 | 0.21 | 0.21 |
(1)滤渣B的主要成分是:
(2)从滤液A得到滤液C,能否用氨水代替NaClO?
(3)从滤液C中获得产品经过3个操作步骤,分别是
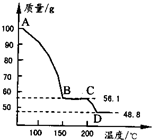
(4)将一定质量的MgSO4.7H2O放在坩埚中加热测得不同温度阶段剩余固体质量如图所示.
据图写出CD段反应的化学方程式
| ||
| ||
部分阳离子以氢氧化物沉淀时溶液pH
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mg(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 11.2 |
| 温度0C | 10 | 30 | 40 |
| CaSO4 | 0.19 | 0.21 | 0.21 |
(1)滤渣B的主要成分是:______.
(2)从滤液A得到滤液C,能否用氨水代替NaClO?______,什么理由______,其中加热煮沸的目的是______.
(3)从滤液C中获得产品经过3个操作步骤,分别是______,______,______.
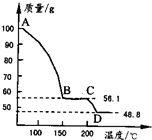
(4)将一定质量的MgSO4.7H2O放在坩埚中加热测得不同温度阶段剩余固体质量如图所示.
据图写出CD段反应的化学方程式______.
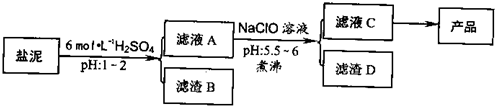
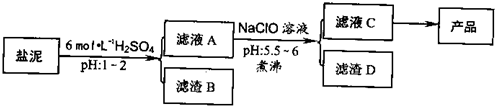
氯碱厂废渣(盐泥)中含有镁钙铁铝的硅酸盐和碳酸盐,其中含镁(以MgO计)约10%,钙(以CaO计)约15%,铁(Ⅱ、Ⅲ)和铝等的含量低于1%。氯碱厂从盐泥中提取MgSO4.7H2O的流程如下:

部分阳离子以氢氧化物沉淀时溶液pH
沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mg(OH)2 |
pH | 5.2 | 3.2 | 9.7 | 11.2 |
溶解度表
温度0C | 10 | 30 | 40 |
CaSO4 | 0.19 | 0.21 | 0.21 |
回答下列问题:
(1)滤渣B的主要成分是:__________________
 (2)从滤渣A得到滤液C,能否用氨水代替NaClO?_________,说明理由________,其中加热煮沸的目的是_________________
(2)从滤渣A得到滤液C,能否用氨水代替NaClO?_________,说明理由________,其中加热煮沸的目的是_________________
(3)从滤液C中获得产品经过3个操作步骤,分别是________,________,_______
(4)将一定质量的MgSO4.7H2O放在坩埚中加热测得不同温度阶段剩余固体质量如右图所示。据图写出CD段反应的化学方程式__________________。
查看习题详情和答案>>(12分) 锌锰废电池经处理后,生产并回收硫酸锌及碳酸锰,其中生产工业级碳酸锰工艺如下:

试回答下列问题
(1)锰在元素周期表中第 周期,第 族。
(2)步骤1和步骤2是将MnO2等转化为MnO并溶于硫酸,其中步骤2中的氢气,是另一个流程产生的副产品,请写出产生氢气的反应方程式 。
(3) 步骤3和步骤4都是除杂质
①X是一种“绿色”氧化剂,则X是____________(填化学式)。
②步骤3是除去杂质Fe2+。请用文字和必要的方程式简述除去Fe2+的方法 (已知三种离子沉淀的pH范围为Fe3+:2.7~3.7,Mn2+:8.6~10.1,Fe2+:7.6~9.6 。)
___________________________________________________________________________。
③步骤4中主要反应方程式为:MeSO4+BaS=MeS↓+BaSO4↓(Me主要为Pb、Cd、Hg等),则其除去杂质的原理是______________________________________________。
(4) 已知进行步骤5的操作时,溶液3(主要成分为MnSO4)会产生大量无色无味的气泡,则步骤5反应的化学方程式为 。
查看习题详情和答案>>