摘要:31.(1)2C+SiO2 2CO↑+Si (2)蒸馏或分馏 (3)①浓H2SO4.使滴入烧瓶中的SiHCl3气化 ②有固体生成.在反应温度下普通玻璃会软化. 10000-11000C SiHCl3+H2 Si+3HCl ③排尽装置中的空气 ④b.d
网址:http://m.1010jiajiao.com/timu3_id_339030[举报]
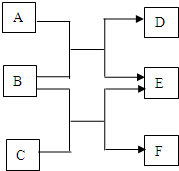 A、B、C、D、E、F六种物质均是由短周期元素组成的中学常见的化学物质.它们之间的转化关系如下图.
A、B、C、D、E、F六种物质均是由短周期元素组成的中学常见的化学物质.它们之间的转化关系如下图.(1)若A、C、E均为氧化物,且E为有毒气体,B、D、F均为非金属单质,且D为气体,则:
①F的晶体类型为
原子晶体
原子晶体
; 1molC中含有4
4
mol共价键;②B与C反应生成E和F的化学方程式为
2C+SiO2
Si+2CO
| ||
2C+SiO2
Si+2CO
| ||
(2)若A、C、E皆为氢化物,三者皆为极性分子,其中A的相对分子质量最小;D、E、F皆为氧化物,且D、F皆为有毒气体.则:
①A、C、E三种氢化物沸点从高到低的顺序为
H2O>NH3>H2S
H2O>NH3>H2S
(填化学式);②A和F在水溶液中充入O2充分反应生成一种正盐,该反应的化学方程式为
2SO2+4NH3+2H2O+O2=2(NH4)2SO4
2SO2+4NH3+2H2O+O2=2(NH4)2SO4
(3)若B是由短周期元素组成的离子化合物,A、C为氧化物,E为气体单质,D、F是均有三种元素组成的离子化合物,它们的水溶液均呈碱性,相同浓度时D溶液的pH大于F.
①写出B的电子式


②B和C反应生成E和F的化学方程式
2Na2O2+2CO2=Na2CO3+O2
2Na2O2+2CO2=Na2CO3+O2
,列举该反应的一种用途呼吸面具和潜水艇中做为氧气的来源
呼吸面具和潜水艇中做为氧气的来源
.已知CO和H2的混合气体称为水煤气,可由碳(C)与水蒸气(H2O)在高温下反应生成.如下图:
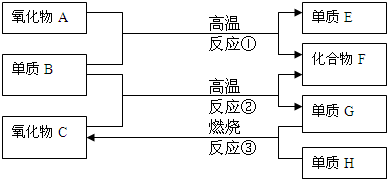
已知:单质E可作为半导体材料,化合物F是有毒的氧化物,C为液态.据此,请填空:
(1)氧化物A是
(2)化合物F是
(3)反应①的化学方程式是
(4)反应②的化学方程式是
(5)反应③的化学方程式是
查看习题详情和答案>>

已知:单质E可作为半导体材料,化合物F是有毒的氧化物,C为液态.据此,请填空:
(1)氧化物A是
SiO2
SiO2
(2)化合物F是
CO
CO
(3)反应①的化学方程式是
2C+SiO2
2CO+Si
| ||
2C+SiO2
2CO+Si
| ||
(4)反应②的化学方程式是
C+H2O
CO+H2
| ||
C+H2O
CO+H2
| ||
(5)反应③的化学方程式是
2H2+O2
2H2O
| ||
2H2+O2
2H2O
.
| ||
(2009?合肥三模)某些元素的性质或原子结构信息如下表所示:
(1)写出A单质与浓HNO3加热反应的化学方程式:
(2)写出B元素在周期表中的位置
(3)写出A与D的氧化物在高温下反应的化学方程式
(4)写出B、D形成的化合物与NaOH溶液反应的离子方程式:
(5)比较A、B、D三元素原子的第一电离能的大小
查看习题详情和答案>>
| A(短周期) | B(短周期) | C | D(短周期) |
| 原子最外层上p电子数等于次外层电子数 | 原子最外层有两个未成对电子,其单质为人类生存必须物质 | 单质为生活中常见的金属材料,有紫红色金属光泽 | 单质是常见的半导体材料,广泛应用于IT行业 |
C+4HNO3(浓)
CO2↑+4NO2↑+2H2O
| ||
C+4HNO3(浓)
CO2↑+4NO2↑+2H2O
.
| ||
(2)写出B元素在周期表中的位置
第二周期ⅥA族
第二周期ⅥA族
,写出C元素基态原子的电子排布式1s22s22p63s23p63d104s1
1s22s22p63s23p63d104s1
.(3)写出A与D的氧化物在高温下反应的化学方程式
2C+SiO2
2CO+Si
| ||
2C+SiO2
2CO+Si
.
| ||
(4)写出B、D形成的化合物与NaOH溶液反应的离子方程式:
SiO2+2OH-═SiO32-+H2O
SiO2+2OH-═SiO32-+H2O
.(5)比较A、B、D三元素原子的第一电离能的大小
O>C>Si
O>C>Si
(由大到小用元素符号表示)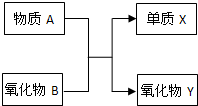 元素及其化合物的知识是“化学I”的重点内容. A、B、X、Y均为中学阶段的常见物质,它们之间的转化关系如图所示:
元素及其化合物的知识是“化学I”的重点内容. A、B、X、Y均为中学阶段的常见物质,它们之间的转化关系如图所示:试写出符合下列条件的化学方程式:
(1)若物质A为氧化物:
3CO+Fe2O3
3CO2+2Fe
| ||
3CO+Fe2O3
3CO2+2Fe
;
| ||
(2)若A为金属单质,B为金属氧化物:
2Al+Fe2O3
2Fe+Al2O3
| ||
2Al+Fe2O3
2Fe+Al2O3
;
| ||
(3)若A为金属单质,B为非金属氧化物:
2Mg+CO2
2MgO+C
| ||
2Mg+CO2
2MgO+C
;
| ||
(4)若A和X均为非金属单质:
2C+SiO2
Si+2CO↑
| ||
2C+SiO2
Si+2CO↑
.
| ||