网址:http://m.1010jiajiao.com/timu3_id_338952[举报]
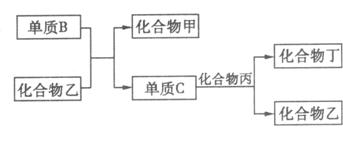
(1)根据以上条件,可以确定A、B、C、D四种元素中三种,不能被确定的第四种元
素是___________,写出转化关系图中已确认的反应的化学方程式:____________________。
(2)下列四个补充条件中的任何一个都可以进一步确定第四种元素,但其中一个条件推断的第四种元素与其余三个条件推断出的第四种元素不同,则此条件是________________________。
A.化合物甲与丙、乙与丙均能够发生反应
B.化合物甲、乙、丙都是无色物质,其中只有甲有刺激性气味
C.通常情况下乙和丁不发生反应,若将乙、了、单质C混合,立即发生反应
D.单质C和化合物丁不能共存
依据该条件推断,第四种元素在周期表中的位置为___________。
(3)由(2)中的另外三个补充条件推断出的第四种元素所形成化合物丙的空间构型为______________________。
查看习题详情和答案>>| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能分别是: I1=738kJ/mol I2=1451kJ/mol I3=7733kJ/mol I4=10540kJ/mol |
| D原子核外所有p轨道全满或半满 |
| E元素的主族序数与周期数的差为4 |
| F是前四周期中电负性最小的元素 |
| G在周期表的第七列 |
(1)已知BA5为离子化合物,写出其电子式


(2)B基态原子中能量最高的电子,其电子云在空间有
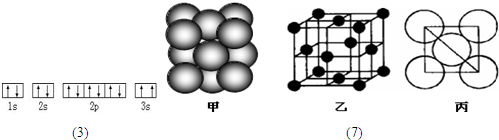
(3)某同学根据上述信息,推断C基态原子的核外电子排布如图:该同学所画的电子排布图违背了
(4)G位于
(5)DE3中心原子的杂化方式为
(6)检验F元素的方法是
(7)若某单质晶体中原子的堆积方式如图甲所示,其晶胞特征如图乙所示,原子之间相互位置关系的平面图如图丙所示.则晶胞中该原子的配位数为
一般测定样品中成分含量的实验应重复2―3次。为了测定某氢氧化钠固体中混有的碳酸钠的质量分数,甲、乙、丙三位同学分别设计了如下实验方案:
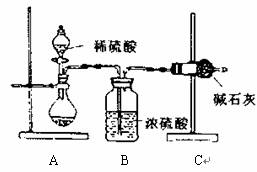
Ⅰ.甲同学的方案如上图所示:
(1)根据甲同学的实验装置图分析,在每次实验过程中所进行的称量操作至少要进行
次;
(2)甲同学重复测定了三次,得到碳酸钠的质量分数的数据存在较大的偏差,你认为可能的原因是 (填序号)。
A.装置内原有空气中的二氧化碳气体也被碱石灰吸收;
B.装置外空气中的水蒸气和二氧化碳被碱石灰吸收;
C.反应完成后,装置中的二氧化碳没有全部被碱石灰吸收;
D.加入稀硫酸的量不足
Ⅱ.乙同学的方案是:从下图所提供的装置中选择实验装置,代替甲同学实验的B、C,通过测定放出的二氧化碳的体积(不考虑二氧化碳溶于水)来计算。
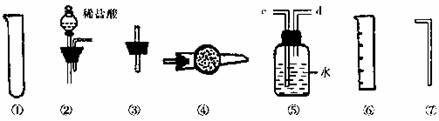
(1)选择最简装置的连接顺序为 ;
(2)产生的气体从装置⑤的 端进入。
Ⅲ.丙同学的方案是:称取样品mg,并溶解,加入过量氯化钡溶液,过滤、洗涤、烘干、称量,得固体ng。
(1)混合物中碳酸钠的质量分数为(用m、n表示) ;
(2)Ca2+、Ba2+都可以使CO32-沉淀完全。乙同学能否使用氯化钙溶液代替氯化钡溶液?
为什么? 。
查看习题详情和答案>>在研究性学习中,某实验小组进行了铜与稀硝酸反应的实验探究.有三位学生设计了以下三种实验方案.如图所示:

(1)写出稀硝酸与铜反应的化学方程式______.
(2)甲同学用图1装置进行实验,在圆底烧瓶中加入20mL 6mol/L HNO3和2g薄铜片,在反应开始时,可观察到水槽内的导管中水面先慢慢上升到一定高度,此后又回落,然后有气泡从导管口冒出.试说明产生上述现象的原因______.
(3)乙同学将甲的实验进行了改进,采用了图2装置进行实验.
①在实验中,要使B中的气体始终保持无色,其操作是______.
②如果开启a和c,关闭b,装置里液面上空间的体积为VmL,空气中氧气的体积分数为21%,实验在标准状况下进行,全部氧气通过反应转化为硝酸;实验开始时加入的铜为mg,实验完毕后剩余的铜为ng,所得溶液体积也是VmL.则所得溶液的物质的量浓度是______.
(4)丙同学采用图3装置进行实验,将活塞打开,从U形管的长管口注入稀硝酸,一直注到U形管短管中充满液体时,立即关闭活塞.铜与稀硝酸开始反应产生NO气体.
①当______时反应、自动停止,在______处观察到无色的NO气体.
②为了证明Cu与稀HNO3反应生成的气体是NO,而不是N2,需要的简单操作是______.
③图3装置与图1、图2装置相比,优点是______.
查看习题详情和答案>>

(1)写出稀硝酸与铜反应的化学方程式______.
(2)甲同学用图1装置进行实验,在圆底烧瓶中加入20mL 6mol/L HNO3和2g薄铜片,在反应开始时,可观察到水槽内的导管中水面先慢慢上升到一定高度,此后又回落,然后有气泡从导管口冒出.试说明产生上述现象的原因______.
(3)乙同学将甲的实验进行了改进,采用了图2装置进行实验.
①在实验中,要使B中的气体始终保持无色,其操作是______.
②如果开启a和c,关闭b,装置里液面上空间的体积为VmL,空气中氧气的体积分数为21%,实验在标准状况下进行,全部氧气通过反应转化为硝酸;实验开始时加入的铜为mg,实验完毕后剩余的铜为ng,所得溶液体积也是VmL.则所得溶液的物质的量浓度是______.
(4)丙同学采用图3装置进行实验,将活塞打开,从U形管的长管口注入稀硝酸,一直注到U形管短管中充满液体时,立即关闭活塞.铜与稀硝酸开始反应产生NO气体.
①当______时反应、自动停止,在______处观察到无色的NO气体.
②为了证明Cu与稀HNO3反应生成的气体是NO,而不是N2,需要的简单操作是______.
③图3装置与图1、图2装置相比,优点是______.