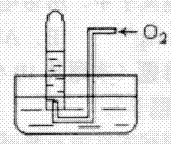
摘要:65.按右图进行实验.试管内装有12mLNO.然后间歇而缓慢 地通入8mLO2.下面有关实验最终状态的描述正确的是( ) A.试管内气体呈棕红色 B.试管内气体为无色是NO C.试管内气体为无色是O2 D.试管内液面高度上升
网址:http://m.1010jiajiao.com/timu3_id_338452[举报]
某同学利用下图所示的实验装置进行铁跟水蒸气反应的实验,并继续研究铁及其化合物的部分性质.
请回答下列问题:
(1)硬质试管中发生反应的化学方程式为
(2)该同学欲确定反应后硬质试管中固体物质的成分,设计了如下实验方案:
①待硬质试管冷却后,取少许其中的固体物质溶于稀硫酸得溶液B;
②取少量溶液B滴加KSCN溶液,若溶液变红色则说明硬质试管中固体物质的成分是
(3)该同学按上述实验方案进行了实验,结果溶液未变红色,原因是:
(4)该同学马上另取少量溶液B,使其跟NaOH溶液反应.若按右图所示的操作,可观察到生成白色沉淀,迅速变成灰绿色,最后变成红褐色的现象,请写出与上述现象相关的反应的化学方程式:
(5)一段时间后,该同学发现(3)中未变红的溶液变成红色,说明Fe2+具有

查看习题详情和答案>>
请回答下列问题:
(1)硬质试管中发生反应的化学方程式为
3Fe+4H2O(g)=Fe3O4+4H2
3Fe+4H2O(g)=Fe3O4+4H2
.(2)该同学欲确定反应后硬质试管中固体物质的成分,设计了如下实验方案:
①待硬质试管冷却后,取少许其中的固体物质溶于稀硫酸得溶液B;
②取少量溶液B滴加KSCN溶液,若溶液变红色则说明硬质试管中固体物质的成分是
一定有Fe3O4,可能有Fe
一定有Fe3O4,可能有Fe
,若溶液未变红色则说明硬质试管中固体物质的成分是Fe3O4和Fe
Fe3O4和Fe
.(3)该同学按上述实验方案进行了实验,结果溶液未变红色,原因是:
Fe+2Fe3+=3Fe2+
Fe+2Fe3+=3Fe2+
(用离子方程式表示).(4)该同学马上另取少量溶液B,使其跟NaOH溶液反应.若按右图所示的操作,可观察到生成白色沉淀,迅速变成灰绿色,最后变成红褐色的现象,请写出与上述现象相关的反应的化学方程式:
FeSO4+2NaOH=Fe(OH)2↓+Na2SO4;4Fe(OH)2+O2+2H2O=4Fe(OH)3
FeSO4+2NaOH=Fe(OH)2↓+Na2SO4;4Fe(OH)2+O2+2H2O=4Fe(OH)3
.(5)一段时间后,该同学发现(3)中未变红的溶液变成红色,说明Fe2+具有
还原
还原
性.由此可知,实验室中FeSO4溶液要临时配制并加少量铁粉的原因是Fe2+易被空气中的氧气氧化而变质
Fe2+易被空气中的氧气氧化而变质
.
某课题小组同学测量液态奶含氮量的实验过程如下:
原理:液态奶
(NH4)2SO4溶液
NH3
(NH4)2B4O7
步骤:
①在烧杯中加入10.00mL液态奶和辅助试剂,加热充分反应;
②将反应液转移到大试管中;
③按右图装置用水蒸气将NH3吹出,并用H3BO3溶液吸收(加热装置未画出);
④取下锥形瓶,滴加指示剂,用0.1000mol?L-1盐酸标准液滴定;
⑤重复测定数次,再用10.00mL蒸馏水代替液态奶进行上述操作.
数据记录如下:
回答下列问题:
(1)滴定时(NH4)2B4O7重新转化为H3BO3,反应的离子方程式为
(2)步骤③的实验装置中需要加热的仪器是
(3)不做空白对照实验对实验结果有何影响
(4)计算10.00mL液态奶中的含氮量应代人计算的盐酸体积是
查看习题详情和答案>>
原理:液态奶
| 辅助试剂 |
| 加热 |
| NaOH溶液 |
| 吹出 |
| H3BO3 |
| 吸收 |
步骤:

①在烧杯中加入10.00mL液态奶和辅助试剂,加热充分反应;
②将反应液转移到大试管中;
③按右图装置用水蒸气将NH3吹出,并用H3BO3溶液吸收(加热装置未画出);
④取下锥形瓶,滴加指示剂,用0.1000mol?L-1盐酸标准液滴定;
⑤重复测定数次,再用10.00mL蒸馏水代替液态奶进行上述操作.
数据记录如下:
| 实验编号 | 样品和辅助试剂 | 消耗盐酸体积/mL |
| 1 | 10.00mL液态奶、0.2g催化剂、20mL浓硫酸 | 33.45 |
| 2 | 10.00mL液态奶、0.2g催化剂、20mL浓硫酸 | 25.50 |
| 3 | 10.00mL液态奶、0.2g催化剂、20mL浓硫酸 | 33.55 |
| 4 | 10.00mL液态奶、0.2g催化剂、20mL浓硫酸 | 33.50 |
| 5 | 10.00mL液态奶、0.2g催化剂、20mL浓硫酸 | 1.50 |
(1)滴定时(NH4)2B4O7重新转化为H3BO3,反应的离子方程式为
B4O72-+2H++5H2O=4H3BO3
B4O72-+2H++5H2O=4H3BO3
.(2)步骤③的实验装置中需要加热的仪器是
圆底烧瓶
圆底烧瓶
(填仪器名称),长导管的作用是防止装置中压力过大而发生危险,防止冷却时发生倒吸,起到安全管的作用
防止装置中压力过大而发生危险,防止冷却时发生倒吸,起到安全管的作用
.(3)不做空白对照实验对实验结果有何影响
偏高
偏高
(填“无影响”,或“偏高”,或“偏低”).(4)计算10.00mL液态奶中的含氮量应代人计算的盐酸体积是
32.00
32.00
mL,该液态奶的含氮量4.480
4.480
mg?mL-1.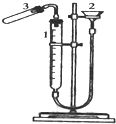 利用右图装置测定金属镁的相对原子质量.请根据要求回答有关问题:(所提供试剂有:0.48克镁带、18.4mol?L-1的H2SO4、2.0mol?L-1的H2SO4)
利用右图装置测定金属镁的相对原子质量.请根据要求回答有关问题:(所提供试剂有:0.48克镁带、18.4mol?L-1的H2SO4、2.0mol?L-1的H2SO4)实验方法如下:
(1)加药品前要检查该装置的气密性,较简便单的方法是:
向漏斗中加入一定量的水,若量气管内水面低于漏斗中的水面,且数分钟(或一段时间)保持不变,则气密性良好
向漏斗中加入一定量的水,若量气管内水面低于漏斗中的水面,且数分钟(或一段时间)保持不变,则气密性良好
.(2)气密性检验后,按以下步骤进行实验,请回答有关问题:
①装硫酸.取下试管,加入
2.0mol?L-1
2.0mol?L-1
mol/L的H2SO4且体积应大于10
10
ml.②放置镁条.为保证产生的氢气不泄漏,应将镁条放置在
试管口的上部,不与硫酸接触
试管口的上部,不与硫酸接触
.③记下量气管起始读数V1. ④将试管竖直,使镁条滑到试管中与酸反应;
⑤记下镁条反应完后的量气管读数V2.如何读数才能减少误差
待试管冷却至室温,调节漏斗高度,使两端管内液面保持相平
待试管冷却至室温,调节漏斗高度,使两端管内液面保持相平
.(3)经测定镁与酸反应产生H2的体积为V L(已折算成标准状况),则镁的相对原子质量的表达式为(相对原子质量用M表示):.
(4)如果测得的值比实际值偏大,请你分析产生误差偏大的可能原因(假设在测得外界温度、压强以及在换算、计算过程中都没有错误.至少写2条)①②.
 实验室可利用乙醇、铜或铜的化合物制备乙醛,右图是某兴趣小组设计的实验装置,右边的反应装置相同,而左边的气体发生装置不同,试管C中装有水(加热装置未画出).试回答:
实验室可利用乙醇、铜或铜的化合物制备乙醛,右图是某兴趣小组设计的实验装置,右边的反应装置相同,而左边的气体发生装置不同,试管C中装有水(加热装置未画出).试回答:(1)在仪器组装完成后,加装试剂前必须要进行的操作是
检查装置气密性
检查装置气密性
;(2)两套装置中的A、B处都需加热,A处用水浴加热,B处用
酒精灯
酒精灯
加热,A处用水浴加热的主要优点是试管受热均匀,产生的气流速度平稳
试管受热均匀,产生的气流速度平稳
(3)若按甲装置进行实验,B管处装铜粉,则通入A管的X是
空气或氧气
空气或氧气
,B中反应的化学方程式为2CH3CH2OH+O2
2CH3CHO+2H2O
| Cu |
| △ |
2CH3CH2OH+O2
2CH3CHO+2H2O
.| Cu |
| △ |
(4)若按乙装置进行实验,则B管中应装
氧化铜
氧化铜
,B中反应的化学方程式为CH3CH2OH+CuO
Cu+CH3CHO+H2O
| △ |
CH3CH2OH+CuO
Cu+CH3CHO+H2O
.| △ |
(5)实验结束后,将C试管中的溶液滴入新制的氢氧化铜溶液中并加热,可观察到的现象
有红色沉淀生成
有红色沉淀生成
,写出该过程的化学方程式CH3CHO+2Cu(OH)2
CH3COOH+Cu2O↓+2H2O
| △ |
CH3CHO+2Cu(OH)2
CH3COOH+Cu2O↓+2H2O
.| △ |
 A.49mL B.30mL
A.49mL B.30mL