摘要:标准状况下.向3 mol·L-1的NaOH溶液100mL中缓缓通入4.48LCO2气体.充分反应后溶液中离子浓度大小排列顺序正确的是 A.c(Na+) > c(CO32-) > c(HCO3-) > c (OH-) > c(H+) B.c(Na+) > c(CO32-) = c(HCO3-) > c (OH-) > c(H+) C.c(Na+) > c(HCO3-) > c (OH-) > c(CO32-) > c(H+) D.c(Na+) > c(HCO3-) > c(CO32-) > c (OH-) > c(H+)
网址:http://m.1010jiajiao.com/timu3_id_338200[举报]
|
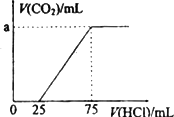
取一定量的NaOH溶液通入CO2后,再继续向该溶液中逐滴加入0.1 mol/L的盐酸,标准状况下产生的CO2的体积与所加盐酸体积之间的关系如下图所示,下列有关说法正确的是
| |
| [ ] | |
A. |
原溶液中NaOH的物质的量为0.75 mol |
B. |
通入CO2后所得的溶液溶质成分为NaOH和Na2CO3 |
C. |
通入CO2后所得的溶液中含有2.5×10-3 mol NaHCO3 |
D. |
纵坐标中a的数值为224 |
将2.5 g碳酸钠、碳酸氢钠和氢氧化钠的固体混合物完全溶解于水,制成稀溶液,然后向该溶液中逐滴加入1 mol·L-1的盐酸,所加入盐酸的体积与产生CO2的体积(标准状况)关系如下图所示:

(1)写出OA段所发生反应的离子方程式________.
(2)当加入35 mL盐酸时,产生CO2的体积为________mL(标准状况).
(3)原混合物中NaOH的质量为________g,碳酸钠的质量分数为________.
将2.5 g碳酸钠、碳酸氢钠和氢氧化钠的固体混合物完全溶解于水,制成稀溶液,然后向该溶液中逐滴加入1 mol·L-1的盐酸,所加入盐酸的体积与产生CO2的体积(标准状况)关系如下图所示:

(1)写出OA段所发生反应的离子方程式________、________.
(2)当加入35 mL盐酸时,产生CO2的体积为________mL(标准状况).
(3)原混合物中NaOH的质量为________g,碳酸钠的质量分数为________.