摘要:将例题中的“KOH(aq) 改为:稀H2SO4.其他同例题.试回答前(4)问.
网址:http://m.1010jiajiao.com/timu3_id_338083[举报]
今欲用NaOH固体配制450mL 0.8mol/L的NaOH溶液.根据题意填空:
(1)配制该溶液应选用
(2)用托盘天平称取
(3)将称好的NaOH固体放至烧杯中,倒入适量蒸馏水,用玻璃棒搅拌至完全溶解.待
(4)用少量蒸馏水洗涤烧杯
(5)向容量瓶中加入蒸馏水,到离刻度线
查看习题详情和答案>>
(1)配制该溶液应选用
500
500
mL容量瓶.(2)用托盘天平称取
16.0
16.0
克固体NaOH.(3)将称好的NaOH固体放至烧杯中,倒入适量蒸馏水,用玻璃棒搅拌至完全溶解.待
冷却
冷却
后,将烧杯中的溶液用玻璃棒
玻璃棒
引流转移至容量瓶.(4)用少量蒸馏水洗涤烧杯
2-3
2-3
次,洗涤液转移到容量瓶中
转移到容量瓶中
,轻轻摇动容量瓶,使溶液混和均匀.(5)向容量瓶中加入蒸馏水,到离刻度线
1-2cm
1-2cm
时,改用胶头滴管
胶头滴管
加蒸馏水至液面与刻度线相切.配制400mL0.1mol/L的Na2CO3溶液:
(1)计算:需无水Na2CO3
(3)溶解:所需仪器
(4)转移:将烧杯中的溶液沿
(5)定容:当往容量瓶里加蒸馏水时,距刻度线
过多,改用
(6)不能配制任意体积的一定物质的量浓度的溶液,这是因为
(7)溶液注入容量瓶前需恢复到室温,这是因为
(8)用胶头滴管定容后再振荡,出现液面底于刻度线时不要再加水,这是因为
(9)如果加水定容时超出了刻度线,不能将超出部分再吸走,须
(10)如果摇匀时不小心洒出几滴,不能再加水至刻度,必须重新配制,这是因为
(11)溶质溶解后转移至容量瓶时,必须用少量蒸馏水将烧杯及玻璃棒洗涤2-3次,并将洗涤液一并倒入容量瓶,这是因为
查看习题详情和答案>>
(1)计算:需无水Na2CO3
5.3
5.3
g. (2)称量:用天平称量无水Na2CO35.3
5.3
g.(3)溶解:所需仪器
烧杯、玻璃棒
烧杯、玻璃棒
.(4)转移:将烧杯中的溶液沿
玻璃棒
玻璃棒
小心地引流到容量瓶
容量瓶
中.(5)定容:当往容量瓶里加蒸馏水时,距刻度线
1-2
1-2
cm处停止,为避免加水的体积过多,改用
胶头滴管
胶头滴管
加蒸馏水到溶液的凹液面
凹液面
正好与刻度线相切
相切
,这个操作叫做定容.(6)不能配制任意体积的一定物质的量浓度的溶液,这是因为
容量瓶的容积固定
容量瓶的容积固定
.(7)溶液注入容量瓶前需恢复到室温,这是因为
溶液有热胀冷缩的性质,如果不冷却到室温,会导致溶液的体积偏小,配制溶液的浓度偏高.
溶液有热胀冷缩的性质,如果不冷却到室温,会导致溶液的体积偏小,配制溶液的浓度偏高.
.(8)用胶头滴管定容后再振荡,出现液面底于刻度线时不要再加水,这是因为
再加水导致溶液的体积偏大,配制溶液的浓度偏小.
再加水导致溶液的体积偏大,配制溶液的浓度偏小.
.(9)如果加水定容时超出了刻度线,不能将超出部分再吸走,须
重新配制
重新配制
.(10)如果摇匀时不小心洒出几滴,不能再加水至刻度,必须重新配制,这是因为
再加水至刻度导致溶质的物质的量偏小,配制溶液的浓度偏低.
再加水至刻度导致溶质的物质的量偏小,配制溶液的浓度偏低.
.(11)溶质溶解后转移至容量瓶时,必须用少量蒸馏水将烧杯及玻璃棒洗涤2-3次,并将洗涤液一并倒入容量瓶,这是因为
如果不将洗涤液倒入容量瓶会导致溶质的物质的量偏小,配制溶液的浓度偏低.
如果不将洗涤液倒入容量瓶会导致溶质的物质的量偏小,配制溶液的浓度偏低.
.某同学按下列步骤配制500mL 0.200mol/L KCl 溶液:
①将烧杯中的溶液转移至500mL 容量瓶中 ②称量KCl 固体 ③向容量瓶中加蒸馏水至刻度线 ④计算所需KCl的质量 ⑤将KCl加入100mL 烧杯中,并加适量水
(1)需要KCl 的质量为
(2)配制上述溶液除需要天平、烧杯、量筒外,还需要的仪器有
(3)实验的先后顺序应为
(4)进行③的实验操作时若加蒸馏水时不慎超过了刻度,会使所配溶液的物质的量浓度
查看习题详情和答案>>
①将烧杯中的溶液转移至500mL 容量瓶中 ②称量KCl 固体 ③向容量瓶中加蒸馏水至刻度线 ④计算所需KCl的质量 ⑤将KCl加入100mL 烧杯中,并加适量水
(1)需要KCl 的质量为
7.5g
7.5g
.(2)配制上述溶液除需要天平、烧杯、量筒外,还需要的仪器有
药匙
药匙
、玻璃棒
玻璃棒
、500mL容量瓶、胶头滴管
500mL容量瓶、胶头滴管
.(3)实验的先后顺序应为
④②⑤①③
④②⑤①③
(填写序号) (4)进行③的实验操作时若加蒸馏水时不慎超过了刻度,会使所配溶液的物质的量浓度
偏小
偏小
.在定容后俯视刻度线使所配溶液的物质的量浓度偏大
偏大
.固氮有三种方式:生物固氮、工业合成氨和放电条件下氮气与氧气化合.全世界工业合成氮肥中的氮只占固氮总量的20%,其余绝大多数是通过生物固氮进行的,最常见的是豆科植物根部的根瘤菌,能将大气中游离态的氮经固氮酶的作用生成氮的化合物,以利于植物利用.
(1)根瘤菌与豆科植物的关系在生物学上称为
(2)根瘤菌之所以有固氮作用,是因为它有独特的固氮酶,而最根本原因是它含有独特的
(3)日本科学家把固氮基因转移到水稻根际微生物中,通过指导合成固氮所需的
(4)这种生物固氮与工业合成氨比较,它是在
(5)俗话说“雷雨发庄稼”,因为电闪雷鸣的雨天,氮气在空气中发生一系列的反应,产生了植物可利用的含氮化合物,写出有关的三个反应方程式
查看习题详情和答案>>
(1)根瘤菌与豆科植物的关系在生物学上称为
共生
共生
;(2)根瘤菌之所以有固氮作用,是因为它有独特的固氮酶,而最根本原因是它含有独特的
固氮基因
固氮基因
;(3)日本科学家把固氮基因转移到水稻根际微生物中,通过指导合成固氮所需的
固氮酶
固氮酶
进而引起固氮作用.更为理想的是直接将固氮基因转移到稻、麦等粮食及经济作物的细胞中,让植物本身直接固氮,这样可以免施氮肥.如果这种愿望实现的话说,那么固氮基因中遗传信息表达途径为固氮基因→信使RNA→固氮酶
固氮基因→信使RNA→固氮酶
;(4)这种生物固氮与工业合成氨比较,它是在
常温、常压
常温、常压
条件下进行的,从而节省了大量的器材、设备和能源;(5)俗话说“雷雨发庄稼”,因为电闪雷鸣的雨天,氮气在空气中发生一系列的反应,产生了植物可利用的含氮化合物,写出有关的三个反应方程式
N2+O2=2NO
N2+O2=2NO
、2NO+O2=2NO2
2NO+O2=2NO2
、3NO2+H2O=2HNO3+NO
3NO2+H2O=2HNO3+NO
.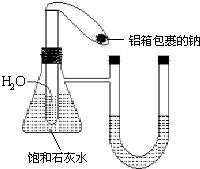 在如图所示的装置中,锥形瓶中装有饱和石灰水,小试管中装有一定量的水,气球中有一小块用铝箔包着的钠,整套装置气密性良好,未反应前U形管两端液面相平.现将气球中的金属钠放入小试管中与水反应.
在如图所示的装置中,锥形瓶中装有饱和石灰水,小试管中装有一定量的水,气球中有一小块用铝箔包着的钠,整套装置气密性良好,未反应前U形管两端液面相平.现将气球中的金属钠放入小试管中与水反应.(1)观察到的现象是:①
有气体产生,是气球膨胀
有气体产生,是气球膨胀
;②U型管右边液面上升,左边液面下降
U型管右边液面上升,左边液面下降
; ③饱和石灰水中会有沉淀生成
饱和石灰水中会有沉淀生成
.(2)产生上述现象的原因是
钠与水反应产生氢气会使气球膨胀;同时又热量放出,使周围空气膨胀,则
U型管左边液面下降,右边液面上升;由于Ca(OH)2的溶解度随温度的升高而降低,则有沉淀产生
U型管左边液面下降,右边液面上升;由于Ca(OH)2的溶解度随温度的升高而降低,则有沉淀产生
钠与水反应产生氢气会使气球膨胀;同时又热量放出,使周围空气膨胀,则
U型管左边液面下降,右边液面上升;由于Ca(OH)2的溶解度随温度的升高而降低,则有沉淀产生
.U型管左边液面下降,右边液面上升;由于Ca(OH)2的溶解度随温度的升高而降低,则有沉淀产生
(3)写出钠与水反应的离子方程式
2Na+2H2O=2Na++2OH-+H2↑
2Na+2H2O=2Na++2OH-+H2↑
.