摘要:在氧化钠与过氧化钠的晶体中.阳离子与阴离子的个数比进行比较.前者和后者的关系正确的是 [ ] A.大于B.小于C.等于D.无法比较
网址:http://m.1010jiajiao.com/timu3_id_337886[举报]
[化学--选修2:化学与技术]
工业上通常采用碱法从铝土矿制取Al2O3,如图为碱法制取Al2O3的工艺流程.已知铝土矿中含有的杂质主要是氧化铁、含硅化合物.
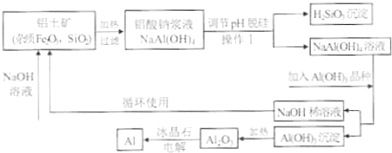
回答下列问题:
(1)操作I的名称是 ;得到的H2SiO3沉淀经过处理可得到硅胶,写出硅胶的一种用途 .
(2)工业上将Al2O3投入熔融的冰晶石,通过电解制备金属铝,冰晶石的作用是 .铝电解槽的阳极材料为碳块,需要定期更换,说明原因 .
(3)工业上用NaOH溶液溶解铝上矿,是利用了Al2O3的 性.
(4)写出铝土矿中杂质与加入的氢氧化钠溶液反应的离子方程式 .
(5)往铝酸钠[NaAl(OH)4]溶液中加入晶种Al(OH)3,通过结晶析出氢氧化铝,写出析出氢氧化铝的离子方程式 .
(6)氢氧化铝在不同温度下分解产物不同,已知:
2Al(OH)3
Al2O3?H2O+2H2O↑ Al2O3?H2O
Al2O3+H2O↑
现有一定温度下加热氢氧化铝得到的固体产物,经测定其中氢元素含量为1.0%,判断固体产物的成分是 .
查看习题详情和答案>>
工业上通常采用碱法从铝土矿制取Al2O3,如图为碱法制取Al2O3的工艺流程.已知铝土矿中含有的杂质主要是氧化铁、含硅化合物.

回答下列问题:
(1)操作I的名称是
(2)工业上将Al2O3投入熔融的冰晶石,通过电解制备金属铝,冰晶石的作用是
(3)工业上用NaOH溶液溶解铝上矿,是利用了Al2O3的
(4)写出铝土矿中杂质与加入的氢氧化钠溶液反应的离子方程式
(5)往铝酸钠[NaAl(OH)4]溶液中加入晶种Al(OH)3,通过结晶析出氢氧化铝,写出析出氢氧化铝的离子方程式
(6)氢氧化铝在不同温度下分解产物不同,已知:
2Al(OH)3
| ||
| ||
现有一定温度下加热氢氧化铝得到的固体产物,经测定其中氢元素含量为1.0%,判断固体产物的成分是
一定温度范围内用氯化钠熔浸钾长石(主要成份为KAlSi3O8)可制得氯化钾,主要反应是:
NaCl(l)+KAlSi3O8(s)?KCl(l)+NaAlSi3O8(s).
(1)上述反应涉及的第三周期元素中,离子半径最小的是 (用元素符号表示).Cl原子与Si原子可以形成的五核分子,其化学键长和键角都相等,则该物质为 分子(填“极性”或“非极性”).
(2)表示原子或离子结构的化学用语有:原子结构示意图、核外电子排布式、轨道表示式.从中选择最详尽描述核外电子运动状态的方式,来表示氧离子核外电子的运动状态: .
(3)上述元素的最高价氧化物对应水化物中,既能与强酸又能与强碱反应,其原因在于: (用电离方程式表示).
(4)Al与Cl可以形成分子晶体AlCl3,关于AlCl3溶液的说法错误的是 .
A.水溶液中离子浓度大小:c(Cl-)>c(Al3+)>c(H+)>c(OH-)
B.升高温度,AlCl3水溶液pH减小,c(Al3+)减小
C.c(Al3+)+c(H+)=c(Cl-)+c(OH-)
D.c(Cl-)=3c(Al3+)+3c(AlO2-)
(5)不能用于比较Na与Al金属性相对强弱的事实是 .
A.最高价氧化物对应水化物的碱性 B.Na和AlCl3溶液反应
C.单质与H2O反应的难易程度 D.比较同浓度NaCl和AlCl3的pH值
(6)Na和O2反应形成Na2O和Na2O2的混合物,阴阳离子的个数比为 .用电子式表示Na2O2的形成过程: .
查看习题详情和答案>>
NaCl(l)+KAlSi3O8(s)?KCl(l)+NaAlSi3O8(s).
(1)上述反应涉及的第三周期元素中,离子半径最小的是
(2)表示原子或离子结构的化学用语有:原子结构示意图、核外电子排布式、轨道表示式.从中选择最详尽描述核外电子运动状态的方式,来表示氧离子核外电子的运动状态:
(3)上述元素的最高价氧化物对应水化物中,既能与强酸又能与强碱反应,其原因在于:
(4)Al与Cl可以形成分子晶体AlCl3,关于AlCl3溶液的说法错误的是
A.水溶液中离子浓度大小:c(Cl-)>c(Al3+)>c(H+)>c(OH-)
B.升高温度,AlCl3水溶液pH减小,c(Al3+)减小
C.c(Al3+)+c(H+)=c(Cl-)+c(OH-)
D.c(Cl-)=3c(Al3+)+3c(AlO2-)
(5)不能用于比较Na与Al金属性相对强弱的事实是
A.最高价氧化物对应水化物的碱性 B.Na和AlCl3溶液反应
C.单质与H2O反应的难易程度 D.比较同浓度NaCl和AlCl3的pH值
(6)Na和O2反应形成Na2O和Na2O2的混合物,阴阳离子的个数比为